如图所示,将白磷和红磷分装于Y形试管的两个支管中,管口系牢小气球将两个支管同时伸入相同深度的热水中。请回答下列问题:
(1)燃烧的是 (填“a”、“b“或“c”)处,该处燃着的磷会很快熄灭,原因可能是 (填序号)。
A.温度降低
B.氧气耗尽
C.试管内产生了二氧化碳气体
D.着火点升高
(2)管口的小气球可以防止 (填名称)进入空气,从而使该实验绿色化。
(3)热水的作用是 和 。

A~G是均含有一种相同元素的物质,其中A、B、C、D是不同类别的物质且相对分子质量(化学式量)依次减小,G与碱反应有气体生成。它们之间有如图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“﹣”表示相连两种物质能发生化学反应,部分反应物、生成物及反应条件已略去)。
(l)从物质的分类分析,物质A属于 (填“酸”、“碱”、“盐”或“氧化物”)。
(2)D、E是由相同的元素组成的物质,E的化学式是 。
(3)写出下列反应的化学方程式
D→C: ;B→G: 。

海水“晒盐”得到的粗盐,含有氯化镁、氯化钙、硫酸钠等可溶性杂质,必须对其进行分离和提纯,才能用于工业生产和人们的日常生活.某实验小组设计如下流程除去粗盐中的可溶性杂质,得到氯化钠晶体.请回答下列问题.

(1)步骤II加入的物质有:①过量的碳酸钠溶液、②过量的氢氧化钠溶液、③过量的氯化钡溶液,正确的加入顺序有三种,请你把它写出来(用物质前的序号表示),第一种: ;第二种: ;第三种: .
(2)步骤 IV的实验操作是 .
(3)工业上电解饱和氯化钠溶液可制得烧碱,同时还有氯气和氢气生成.该反应的化学方程式为 .
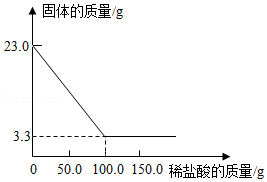
取碳酸钡和硫酸钡的混合物23.0g于烧杯中,将150.0g的稀盐酸平均分三次加入烧杯中,加入稀盐酸的质量与烧杯中固体的质量关系如图所示,计算:
(1)该混合物中硫酸钡的质量为 g
(2)恰好完全反应时所得溶液中溶质的质量分数(精确至0.1%)
自来水厂的生活用水常用氯气来杀菌消毒.氯气是一种黄绿色有刺激性气味的气体,把氯气通入水中生成两种酸,其中一种酸有强氧化性,可杀菌消毒,该酸性质不稳定,见光分解产产生O2.
(1)根据上述信息写出氯气的一种物理性质: .
(2)C12+H2O=HCl+X,X的化学式为 .
空气中氧气含量的测定如图所示:
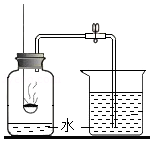
(l)燃烧匙内盛放的药品是 .
(2)集气瓶内水面上升不到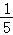 的原因可能是 (答一条即可).
的原因可能是 (答一条即可).
A、B、C、D、E分别是二氧化碳、氧化铁、木炭、稀盐酸和氢氧化钙溶液中的某一种物质。“﹣”表示相邻物质可以发生化学反应,“→”表示A物质可以一步反应转化为E。
(1)物质A的化学式为 ,物质D的一种用途 。
(2)B与C反应的现象为 ,该反应的化学方程式为 。
(3)上述化学反应没有涉及的基本反应类型是 。

水是生命之源,也是人类最宝贵的资源。请回答下列有关问题:
(1)活性炭常用于净水,是利用其 。
(2)建设新农村后,村民已经用上自来水,加入 可检验自来水是否为硬水。日常生活中通过 的方法可降低水的硬度。
(3)实验室通常用如图装置来电解水,该装置中,A试管的电极与电源的 极相连;当A试管中产生的气体体积为l0mL时,B试管中产生的气体体积为 。
(4)下列做法有利于节水的是 (填字母序号)。
A.农业上改漫灌为滴灌 B.用大量水冲洗汽车 C.用淘米水浇花 D.用洗衣服水冲厕所。
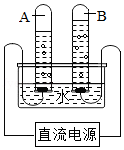
图是实验室常用的实验装置,请回答下列问题:

(1)仪器a的名称是
(2)实验室用氯酸钾制取并收集较纯净的氧气所选的装置是 (填字母,下同),发生反应的化学方程式为 ,停止加热时应先将导管移出水面,再熄灭酒精灯,其理由是 .
(3)实验室常用 装置来制取并收集二氧化碳,检验二氧化碳气体常用 (填试剂名称)溶液.
(4)已知氨气的密度比空气小,且极易溶于水,实验室常用加热氢氧化钙固体和氯化铵固体的方法制取氨气,要制取并收集干燥的氨气,所选装置的正确连接顺序是 .
A﹣F是初中化学常见的物质,且均含有同一种元素,它们相互间的关系如图所示,已知A、B、C、D、E是不同类别的物质,其中C是Na2CO3,E中含有钙元素,F是相对分子质量最小的氧化物(注:图中反应条件及部分反应物,生成物已省略,“﹣”表示反应关系,“→”表示转化关系),请回答:
(1)写出下列物质的化学式:B ,D ,F 。
(2)写出E物质的一种用途 。
(3)写出F→A的化学方程式 。

ClO2被国际上公认为安全、无毒的绿色消毒剂,具有杀菌能力强,对人体及动物危害性很小、对环境不造成二次污染等特点而备受人们的青睐,它在不同的浓度时,由黄绿色到橙黄色变化的气体;遇热水反应生成次氯酸(HClO)、氯气和氧气;见光分解。根据上述信息,回答下列问题:
(1)ClO2是由 元素(填元素名称)和氧元素组成,它属于 (填“单质”或“化合物”)
(2)ClO2的物理性质是 (填一种即可)
(3)请写出ClO2与热水反应的化学方程式 ; 反应前后Cl元素的化合价由+4价变为 价和零价。
小甜利用石灰石和稀盐酸进行如下实验,操作过程和数据如图所示(样品中的杂质不与酸反应也不溶于水)。
(1)20g石灰石样品中CaCO 3的质量为 g。
(2)列式计算不饱和溶液A的溶质质量分数(结果准确到0.1%)。

根据如图装置,结合所学化学知识回答问题。
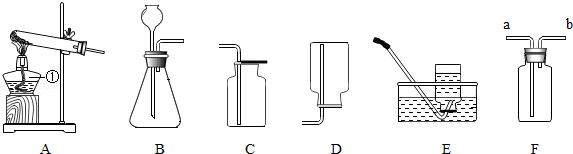
(1)标号仪器①的名称是 ;
(2)用过氧化氢溶液和二氧化锰制取氧气,反应的化学方程式是: 。其中二氧化锰是 ,若选用F装置收集氧气,气体应该从 口进入(填"a"或"b");
(3)实验室选择装置B和C制取二氧化碳,反应的化学方程式是 ,验满的方法是 ,若将收集的气体通入紫色石蕊溶液中,产生的现象是 ;
(4)我县近年逐步采用天然气取暖。天然气的主要成分是甲烷,楠楠同学通过查阅资料,如果实验室可用无水醋酸钠固体和固体碱石灰加热制取甲烷。通常情况下甲烷的密度比空气小,难溶于水。实验室制取甲烷选择的发生装置是 (填字母),欲收集干燥的甲烷气体可选用 装置(从A﹣E中选择);甲烷的使用,有效地改善了空气质量,其完全燃烧的化学方程式是 。
粗盐中MgCl2、CaCl2等杂质,提纯粗盐的工艺流程如图所示。

回答下列问题:
(1)氢氧化钠有强烈的腐蚀性,如果不慎沾到皮肤上,要用大量的水冲洗,再涂上 ;
(2)步骤②加入过量的碳酸钠溶液的作用是 ;
(3)操作a的名称是 ;
(4)步骤④中,要用玻璃棒不断搅拌,其目的是 。