某兴趣小组为探究锡纸中的金属成分(锡纸中以一种金属为主,其它成分对实验无干扰),开展了以下探究活动。
【提出问题】锡纸中的金属是什么?
【建立猜想】根据锡纸有银白色金属光泽,并结合金属活动性、价格等因素,猜想其中的金属可能是锌、铁、铝、锡中的一种。
【探究过程】
步骤 |
活动内容 |
收集证据 |
分析并得出结论 |
步骤一 |
①查阅资料:金属锌在室温下很脆 |
锡纸未破损 |
锡纸中金属不是锌 |
②取锡纸反复折叠 |
|||
步骤二 |
用磁铁靠近锡纸 |
锡纸没有被磁铁吸引 |
锡纸中金属不是 |
步骤三 |
①取锡纸条放入浓度为20%的盐酸中除去可能存在的氧化膜。当观察到 现象时,取出锡纸条并用蒸馏水清洗。 ②将处理过的锡纸条放入试管中,加入饱和硫酸锌溶液,静置观察。 |
②中锡纸条表面无明显现象 |
说明锡纸中的金属活动性比锌弱,则锡纸中金属不是铝,而是锡。 |
【交流评价】
小科对实验结论提出质疑:“无明显现象”并不代表没有发生反应,因为铝与硫酸锌反应[2Al+3ZnSO4=3Zn+Al2(SO4)3]生成的金属锌为银白色,与铝颜色相同,因此无法得出结论。请在不改变反应原理的前提下运用定量方法完善实验方案,并根据预期结果得出相应结论: ;
。
【继续探究】运用完善后的方案进行实验,分析实验结果,得出初步结论:锡纸中金属是铝。
1674年,英国化学家约翰•梅猷为测定空气中的氧气含量开展如下实验(装置如图甲)。
I.将一根长度等于玻璃钟罩最宽部分直径的铁棒橫放在钟罩里,把装有稀硝酸的陶罐通过铁钩挂在铁棒上,用绳索将小铁块悬挂在陶罐的正上方(铁块的升降通过在钟罩外拉动或放松绳索来实现)。

Ⅱ.调整水槽中初始水位如图乙,再使铁块浸入稀硝酸中,观察到铁块表面迅速产生大量气泡,钟罩内水面下降。[稀硝酸有强氧化性,能与铁发生如下反应:4HNO3+Fe═Fe(NO3)3+NO↑+2H2O]
Ⅲ.当水位降至接近钟罩口时(如图丙),立即取出铁块,以防气体外逸。
IV.等待一段时间后,水面稳定在如图丁的位置。(一氧化氮会与氧气等物质发生如下反应:4NO+3O2+2?=4HNO3)
分析与评价:
(1)步骤Ⅳ中的“?”处应填 。
(2)从图丙到图丁过程中,钟罩内水位上升的原因是 。(忽略温度变化的影响)
(3)小科重复了上述实验,虽实验时装置气密性良好,且钟罩内液面上方气体体积均能精确测量(即测定气体体积的误差忽略不计),但经过多次实验测定,发现每次测得空气的含氧量都小于 ,原因是 。
氯霉素属于广谱抗生素,能杀灭细菌,但摄入过多容易导致血液疾病,所以国家严令禁止在食品中使用。今年,广州市有关部门在抽检中发现,有些不法商向黄金贝、花蛤等海产品中添加氯霉素,来延长海鲜的存活期。这种滥用氯霉素的现象引起了市民的警觉。
(1)氯霉素性质稳定,不易分解,这种性质属于 (填”物理”或“化学”)性质。
(2)氯霉素(化学式为C11H12Cl2N2O5)中碳元素和氧元素的质量比为 。
常温下,铁在潮湿的空气中容易生锈,产物主要为Fe2O3•nH2O;铁丝在氧气中燃烧,产物为黑色Fe3O4.
【提出问题】铁在空气中用酒精灯加热时,是否与空气中氧气发生反应?产物是什么?
【查阅资料】①常见的铁的氧化物有三种:FeO、Fe2O3、Fe3O4,其中Fe3O4是磁性物质。
②FeCl3溶液呈黄色,FeCl2溶液呈浅绿色。
【探究】①按图连接实验装置,检查★。向试管内加入铁粉,针筒活塞停在A刻度。
②加热铁粉的过程中,活塞发生移动。停止加热后,活塞逐渐向左移动,最终停在B刻度。
③用细线吊着洁净铁钉靠近加热后的固体粉末,发现没有粉末被铁钉吸上来。
④向试管内加入盐酸,发现有气泡产生,溶液立即出现黄色。
⑤另取一些未加热过的铁粉加入到盛有盐酸的试管内,发现有气泡产生,溶液变为浅绿色。经检验,步骤④、⑤产生的气体相同。
【实验结论与反思】
(1)步骤①中“★”处应填: 。
(2)步骤④、⑤中产生的气体是 。
(3)本实验探究的结论是:铁粉在空气中用酒精灯加热时,与空气中氧气发生反应,产物是 。
(4)结合已学知识和本次探究分析可得,铁与氧气反应的产物受反应温度,氧气的 等因素影响。
某小组用耐强碱的反应管等仪器组装成如图实验装置,以研究铜酸钠(NaCuO2)跟H2的反应,实验中观察到如下现象:①固体中出现紫红色物质,②试管中无水硫酸铜由白色变为蓝色。
回答: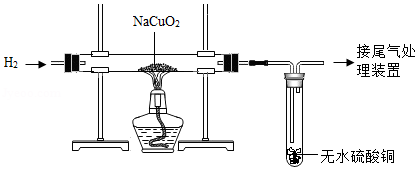
(1)经检验紫红色物质是一种金属单质,完成下列反应的化学方程式:
2NaCuO2+3H2 2NaOH+ + 。
(2)若实验过程中包含下列步骤(没有根据操作顺序排列):①停止通H2;②通纯净H2排净装置里空气;③点燃酒精灯加热;④熄灭酒精灯停止加热。正确的操作顺序是 。
(3)根据题干中给出的实验现象 (选填“①”或“②”),可直接判断氢气发生了化学变化。
(4)完全反应后,为了测定固体产物中Cu的质量,要用蒸馏水多次洗涤后晾干、称量。在洗涤环节中判断洗涤干净的操作方法是 。
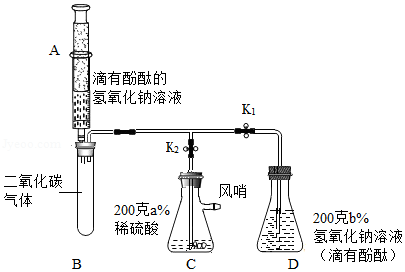
某兴趣小组做了如下实验:
①在止水夹K1、K2处于关闭状态时,将针筒A中溶液挤入试管B中,接着打开止水夹K1,发现D中的部分溶液被吸入试管B中,充分反应后,试管B留下的溶液也显红色;
②打开止水夹K2,风哨振动鸣叫,C中的部分溶液被吸入B和D中,反应后B、D中溶液都变为无色。
回答:
(1)步骤①中,充分反应后,试管B里的CO2最终转化为 (填化学式)和水。
(2)解释步骤②中“风哨振动鸣叫”的原因 。
(3)实验开始时C、D中两种溶液中溶质质量分数大小关系为:a% b%(选填“>”“=”“<”)
某化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,设计实验探究:
[提出问题]甲烷燃烧后生成哪些物质?
[查阅资料]①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;②白色无水CuSO4粉末遇水变蓝色;③CO与人体内的血红蛋白结合,会造成人中毒缺氧。
[猜想与假设]猜想一:CO2、H2O;猜想二:CO、H2O;猜想三:CO2、CO、H2O
[实验探究]将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置(部分夹持、固定装置省略)进行验证:
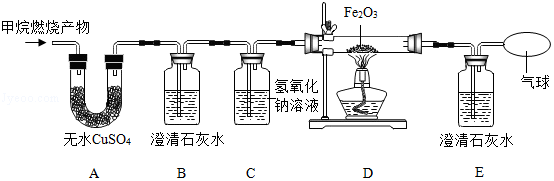
(1)实验过程中观察到A中白色粉末变为蓝色,B、E中澄清石灰水变浑浊,D中红棕色粉末变成黑色,由此推断猜想 成立。
(2)实验过程中B装置的作用是 ;该反应的化学方程式是 。
(3)D装置中发生反应的化学方程式是 。
(4)实验过程中用纯净O2而不用空气的原因是 。
(5)实验过程中B、C装置的顺序不能颠倒,原因是 。
[反思与交流]日常生活中,使用含碳燃料定要注意通风,防止 中毒。
结合下列化学实验装置,回答有关问题。
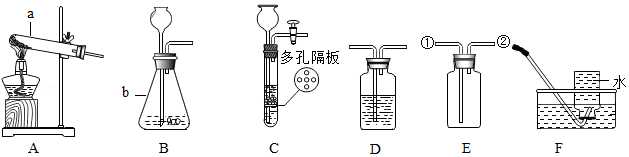
(1)写出图中标有字母的仪器的名称:a ,b 。
(2)实验室用氯酸钾制取氧气时应选择 (填代号)作为发生装置。常温下,下列收集氧气的方法不可行的是 (填字母序号)。
a.向上排空气法
b.向下排空气法
c.排水法
(3)用装置E收集实验室制取的二氧化碳,气体应从 (填“①”或“②”)端进入。
(4)实验室常用装置C代替装置B制取气体,装置C的优点是 。
浓硫酸与木炭在加热条件下可发生反应产生水和化学式为XO2型的气体。某化学课外兴趣小组的同学对XO2型气体的成分进行了实验探究。
[猜想]
(1)根据反应物组成元素及生成物的化学式类型,提出以下猜想:
猜想1 |
猜想2 |
猜想3 |
只有CO2 |
只有 SO2 |
CO2和SO2都有 |
[查阅资料]将SO2、CO2气体分别通入下列溶液中产生的有关现象如表:
气体 溶液 |
SO2 |
CO2 |
品红溶液 |
褪色 |
不褪色 |
氯水(黄绿色) |
褪色 |
不褪色 |
澄清石灰水 |
浑浊 |
浑浊 |
[实验探究]
实验一:
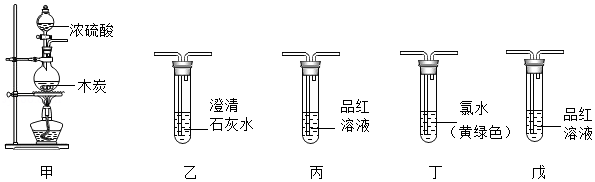
(2)将装置按甲→丙→(尾气处理)连接并进行实验。实验过程中观察到丙中溶液褪色,证明 不成立(填“猜想1”、“猜想2”或“猜想3”)。
实验二:
(3)将装置按甲→乙→(尾气处理)连接并进行实验。实验过程中观察到乙中澄清石灰水变浑浊。根据此现象能否确定CO2 的存在,理由是 。
实验三:
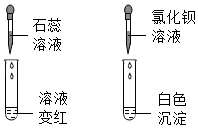
(4)将装置按甲→丙→丁→戊→乙→(尾气处理)连接并进行实验。实验过程中观察到丙、丁中溶液均褪色,戊中溶液颜色无变化,乙中澄清石灰水变浑浊。
①将反应后丁中溶液分成两等份分别置于两支试管中,并按如图所示操作进行实验。根据图中实验现象可判断反应后丁中溶液存在的离子有 。
②丁中溶液的作用是 。
[实验结论]
(5) (填“猜想1”、“猜想2”或“猜想3”)成立。
[问题讨论]
(6)在实验三中,若去掉装置戊,对实验结论 (填“有”或“无”)影响,理由是 。
某实验小组用KClO3和MnO2制取氧气,然后从制取后的残留固体中回收MnO2并用于实验室制取氯气(Cl2 )。部分实验装置如图所示。回答下列问题:
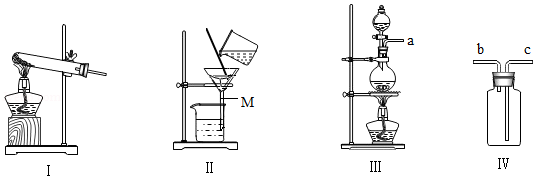
(1)写出装置Ⅰ中制取O2 的化学反应方程式: 。
(2)将制取氧气后的残留固体冷却、转移、 (填操作名称)、过滤、洗涤和干燥,即回收到MnO2.过滤装置Ⅱ中,仪器M的名称是 。
(3)将回收到的MnO2用于实验室制取Cl2.反应原理为:MnO2+4HCl(浓)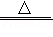 MnCl2+Cl2↑+2H2O,实验装置为Ⅲ和Ⅳ,实验时,将a口连接 (填“b”或“c”)口收集Cl2,收集到的Cl2中的杂质有 (填化学式)。
MnCl2+Cl2↑+2H2O,实验装置为Ⅲ和Ⅳ,实验时,将a口连接 (填“b”或“c”)口收集Cl2,收集到的Cl2中的杂质有 (填化学式)。
(4)洁厕灵(主要成分为盐酸)与“84”消毒液(主要成分为NaClO)混合也会反应生成Cl2:2HCl+NaClO═R+Cl2↑+H2O,生成物R的化学式为 。
阅读短文后回答下列问题。
燃料电池(Fuelcell),是一种使用燃料进行化学反应产生电能的装置,最早于1839年由英国的Grove发明。燃料的选择性非常多,包括纯氢气(H2)、甲醇(CH3OH)、乙醇(CH3CH2OH)、天然气,甚至于现在运用最广泛的汽油,都可以作为燃料电池的燃料。这是目前其他所有动力来源无法做到的。而以燃料电池做为汽车的动力,已被公认是二十一世纪必然的趋势。2017年,我国共有8个品牌的10款车型燃料电池汽车在产,总产量为1272辆,2018年国产燃料电池汽车已经超过3000辆。
燃料电池是以特殊催化剂作电极使燃料与氧气发生反应,生成二氧化碳和水。因其不需推动涡轮等发电器具,也不需将水加热至水蒸气再经散热变回水,所以能量转换效率高达70%左右,足足比一般发电方法高出了约40%;优点还不只如此,其二氧化碳排放量比一般方法低许多,且水又是无害的生成物,所以燃料电池是一种高效、低污染装置。
燃料电池主要由正极、负极、电解质溶液和外部电路4部分组成,其正极和负极分别通入燃料气和氧气(空气),负极上燃料气放出电子,外电路传导电子到正极并与氧气结合生成离子,在电场作用下,离子通过电解质转移到负极上再与燃料气进行反应,最后形成回路产生电能。与此同时,因为燃料自身的反应及电池存在的内阻,燃料电池也要排出一定的热量,以保持电池恒定的工作温度。如图是甲烷燃料电池的工作原理示意图。
(1)燃料电池是将 能转化为电能的装置。
(2)下列说法错误的是
A.化学反应放出的能量可以是光能、热能、电能等
B.燃料电池可以广泛用于新能源汽车
C.氢燃料电池汽车所需要的H2可电解水生成
D.燃料电池都要排放CO2气体
(3)写出甲醇完全燃烧的化学方程式 。
(4)甲烷燃料电池释放能量的总反应化学方程式是 。

某化学兴趣小组用实验室常用药品(或溶液)对“NaOH溶液与稀盐酸是否恰好完全反应”进行探究。
[知识卡片]:氯化钠溶液显中性,氯化铜易溶于水。
[实验探究]:
(1)方案Ⅰ:某同学先向试管中加入约2mLNaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。
①实验结论 。
②从微观的角度分析,该反应的实质是 。
③在滴入稀盐酸的过程中,若观察到有少量气泡出现。请分析产生气泡的可能原因 (用化学方程式表示)。
(2)方案Ⅱ:
实验步骤 |
实验现象 |
结论 |
取2mLNaOH溶液于试管中,滴入一定量的稀盐酸,振荡后加入镁条 |
若 |
稀盐酸过量 |
若没有明显现象 |
NaOH溶液与稀盐酸恰好完全反应 |
[实验反思]:
(3)另有同学提出方案Ⅱ不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是 。
(4)除以上方案外,下列哪些物质单独使用,也能证明“NaOH 溶液与稀盐酸是否恰好完全反应” (填序号)。
A.铜片 B.pH试纸 C.氧化铜 D.紫色石蕊试液
草酸(H2C2O4)存在于自然界的植物中,在170℃以上易分解。某校化学兴趣小组为确定草酸分解产物,做如下探究。
[提出问题]草酸的分解产物是什么?
[猜想与假设]猜想①CO CO2
猜想②CO H2O
猜想③CO2 H2O H2
猜想④CO CO2 H2O
经小组同学分析得出上述猜想 一定是错误的。
[查阅资料]无水硫酸铜是一种白色固体,遇水会变成蓝色。
[进行实验]该小组同学设计了如图的实验过程(部份固定装置已略去)。
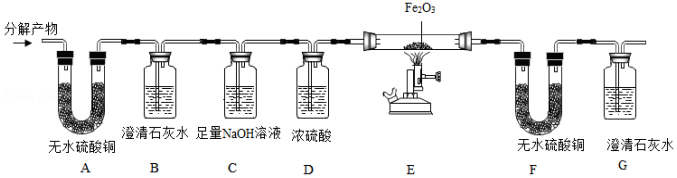
实验步骤 |
实验现象 |
实验结论 |
将分解产物从左至右 依次通过各装置 |
A中无水硫酸铜变蓝 B中澄清石灰水变浑浊 |
猜想②错误 |
F中无水硫酸铜 G中澄清石灰水变浑浊 |
猜想④正确 |
|
问题解答 |
(1)装置C的作用 (2)写出装置E中发生反应的化学方程式 |
|
[交流反思]为防止污染环境,该实验应增加尾气处理装置。
根据如图实验装置,回答问题:
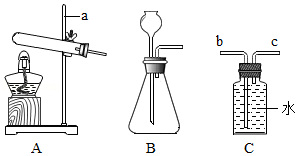
(1)写出图中标有a的仪器名称 ;
(2)写出实验室用B装置制取氧气的化学方程式 ;
(3)若用装置C收集氧气,则氧气应从 (填“b”或“c”)端进入。