某化学兴趣小组的同学在老师的带领下参观如图所示的炼铁厂。小新想用自己所学知识来测定产品中铁的质量分数,征得工人师傅同意,带回一小块生铁样品。称得该样品6.0g,放入烧杯中,向其中逐滴加入稀盐酸,当滴入54.0g稀盐酸时,反应不再产生气泡(假设杂质不参与反应),称得烧杯内剩余物质的总质量为59.8g。(铁与稀盐酸反应的化学方程式为Fe+2HCl=FeCl2+H2↑)
请你帮小新完成有关计算(结果保留一位小数):
(1)实验产生氢气的质量是 g。
(2)生铁样品中铁的质量分数。
为探究一种混合物是由铜粉与镁粉、铁粉、锌粉中的哪一种金属组成。某同学进行了如下实验:称量8.0 g该混合物粉末放入烧杯中→将140 g 14%的稀硫酸平均分成四份依次加入该烧杯中→充分反应后测定剩余固体质量→数据处理:将测得剩余固体质量与加入稀硫酸的质量关系绘制成右图。试计算:
⑴该混合物是由铜粉和____组成的。
⑵加入105 g稀硫酸充分反应后,所得溶液的
质量。
某学习小组的同学在学习了Na2CO3、NaHCO3的性质后,了解到它们都能与盐酸反应产生CO2气体,那么如何鉴别Na2CO3和NaHCO3呢?带着这样的疑问,他们进行了下列探究:
【查阅资料】(1)Ca(HCO3)2可溶于水;
(2)NaHCO3固体受热分解生成碳酸钠、二氧化碳和水。
【猜 想】(1)甲同学认为可用澄清石灰水鉴别Na2CO3和NaHCO3溶液。
(2)乙同学认为可用CaCl2溶液鉴别Na2CO3和NaHCO3溶液。
甲、乙两同学的猜想是依据澄清石灰水、CaCl2溶液分别与Na2CO3溶液反应均有沉淀产生;又知道Ca(HCO3)2可溶于水,因此猜测澄清石灰水、CaCl2溶液分别与NaHCO3溶液混合不会产生沉淀,从而鉴别出两种溶液。
(3)丙同学认为固体Na2CO3、NaHCO3可用加热的方法鉴别。
【实验探究】(1)甲同学在两支分别盛有少量Na2CO3、NaHCO3溶液的试管中,各加入澄清石灰水,观察到两支试管中的现象相同,均产生了白色沉淀,实验结果与猜想不一致,即不能用澄清石灰水鉴别Na2CO3和NaHCO3溶液。
(2)乙同学将CaCl2溶液加入到分别盛有少量Na2CO3、NaHCO3溶液的试管中,发现两支试管中也都产生了白色沉淀,实验结果出乎意料,但根据观察到的其他实验现象,他认为仍可用CaCl2溶
液鉴别Na2CO3和NaHCO3溶液。
(3)丙同学分别取了一定量的Na2CO3、NaHCO3固体于大试管中加热(如图所示):
① 加热Na2CO3时,开始即见小试管中有少量气泡产生,继续加热,气泡逐渐减少,未见澄清石灰水变浑浊,
② 加热NaHCO3时,丙同学观察到实验现象与①不同,证实了自己的猜想是合理的。
【问题讨论】(1)小组同学对上述实验展开了讨论,对甲同学的两个实验进行了比较,并从物质在溶液中解离出不同离子的微观角度分析了原因(如图1、图2)。请写出Na2CO3与澄清石灰水发生反应的化学方程式 ;写出NaHCO3与澄清石灰水混合时参与反应的离子: 。
图1:澄清石灰水与Na2CO3溶液反应 
图2澄清石灰水与NaHCO3溶液反应
(2)乙同学的两个实验中,大家对CaCl2与Na2CO3溶液的反应比较熟悉,而对CaCl2与NaHCO3溶液混合产生的现象难以理解,同学们又进一步查阅了资料,了解到CaCl2与NaHCO3溶液可发生如下反应:CaCl2+2NaHCO3=CaCO3↓+2NaCl+CO2↑+H2O,因而同学们知道了乙同学是通过观察到 现象来鉴别Na2CO3和NaHCO3溶液的。
至于CaCl2与NaHCO3溶液为什么能发生上述反应,老师指出其反应原理较复杂,有待于今后学习中进一步探究。
(3)丙同学在加热Na2CO3固体时,开始产生少量气泡的原因是 ;根据你分析:Na2CO3受热 分解(填“易”或“不易”)。在加热NaHCO3固体时,丙同学观察到的实验现象是 (任写一种)。
【拓展应用】(1)固体Na2CO3中混有少量NaHCO3,可通过 方法除去。
(2)把105g氯化钙溶液与100g5.3%的碳酸钠溶液混合,恰好完全反应,则反应所得溶液中溶质的质量分数是多少?(写出完整的解题过程)。
无土栽培黄瓜的营养液的配方中,含有质量分数为0.2%的尿素溶液 [尿素的化学式为CO(NH2)2 ]。请通过计算,回答下列问题:
(1)尿素的相对分子质量为__________________。
(2)尿素中氮元素的质量分数为______________(精确到0.1%)。
(3)若用50 kg溶质的质量分数为2%的尿素溶液加水稀释,可得溶质的质量分数为0.2%的尿素溶液________kg。
鸡蛋壳的主要成分是碳酸钙,为了测定蛋壳中碳酸钙的质量分数,小刚和小勇同学进行了如下实验。请回答相关问题:(1)他俩将蛋壳洗净、干燥并捣碎放在烧杯里,然后往烧杯中加入足量盐酸,在蛋壳上很快就有许多小气泡产生,将收集到的气体通入澄清石灰水中,石灰水变浑浊。据此可判断,收集到的气体中含有 。
(2)实验过程和测定的相关实验数据如下所示: 小刚根据“蛋壳残渣质量为4.3g”,求得蛋壳中碳酸钙的质量分数为 ;
小刚根据“蛋壳残渣质量为4.3g”,求得蛋壳中碳酸钙的质量分数为 ;
小勇根据“反应过程中减少的质量”,也求得了蛋壳中碳酸钙的质量分数并计算出了盐酸的溶质质量分数,请你写出小勇的计算过程和结果。
(3)小刚和小勇根据不同的数据求得蛋壳中碳酸钙的质量分数有明显差别,请你分析其中可能的原因。
有一包白色粉末A,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验(实验流程如图):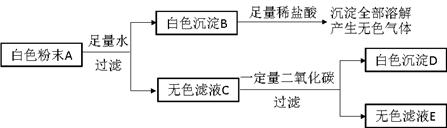
(1)取白色粉末A,向其中加入足量水,充分搅拌后过滤,得到白色沉淀B和无色滤液C。由此可判断,原白色粉末中一定不含有 。
(2)向白色沉淀B中加入足量稀盐酸,沉淀全部溶解,并产生无色气体。由此可判断,原白色粉末中一定含有 。
(3)向无色滤液C中通入一定量二氧化碳,充分反应后过滤,得到白色沉淀D和无色滤液E,由此可判断,原白色粉末中一定还含有 。
(4)若流程图中白色粉末A为20g,白色沉淀D为9.85g,无色滤液E中只含一种溶质。
①无色滤液E中的溶质为 ;
②通过计算确定20g白色粉末A中所含各物质的质量。
(请写出计算及推理过程)
金属过氧化物等可作宇宙飞船或潜水艇中的氧气再生剂,如:过氧化钠(Na2O2)在常温下能与人呼出的二氧化碳反应生成氧气,化学方程式为:2Na2O2+2CO2===2Na2CO3+O2。为了验证该反应中氧气的产生,某兴趣小组的同学设计了如图所示的实验。
(1)A装置中所发生反应的化学方程式为 ;
实验室确定气体发生装置时应考虑的因素是 ;
检查A装置的气密性的方法是:将A装置中导气管上的胶皮管用弹簧夹夹住,往长颈漏斗中注入水至液面高出漏斗颈的下端管口,若能观察到
现象,即可证明装置不漏气。
(2)表明二氧化碳没有被过氧化钠完全吸收的现象是 。
(3)用向上排空气法收集氧气,并用带火星的木条放在集气瓶口检验氧气是否收集满,
这是利用了氧气的哪些性质?
(4)如果用脱脂棉包裹一定量的Na2O2固体,然后向其中通入CO2,脱脂棉很快就燃烧
此现象说明该反应过程中能量是如何变化的?
(5)常温下水也能与Na2O2反应,生成氧气和氢氧化钠,写出该反应的化学方程式。
若要检验干燥的二氧化碳能否与过氧化钠反应生成氧气,以上实验装置应如何改进?
(6)实验室中的过氧化钠如果保存不当,容易与空气中的CO2和水蒸汽发生反应变质。今称取10g过氧化钠样品(杂质不参加反应)放人烧杯中,向其中加入10g水,二者完全反应后。称量烧杯中剩余物质的总质量为18.4g(不包括烧杯的质量,且气体的溶解忽略不计)。试计算过氧化钠样品中杂质的质量分数。
实验室有一瓶未知浓度的BaCl2溶液,某同学取出150g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液。反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图甲所示。请计算:
(1)配制26.5%的Na2CO3溶液80g,需要Na2CO3固体 g。
(2)BaCl2溶液的溶质质量分数是多少?(写出计算过程,结果保留到0.1%)
小明同学在某化工厂进行社会实践,技术员与小明一起分析由氯化钙和氯化钠组成的产品中氯化钠的含量。现取13.4g固体样品,全部溶于96. 6g水中,向所得的混合溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系。求:
(1)当氯化钙与碳酸钠恰好完全反应时,消耗10.6%的碳酸 钠溶液的质量是 g。
(2)样品中氯化钠的质量是多少?
(3)当氯化钙与碳酸钠恰好完全反应时,过滤,所得溶液中溶质的质量分数是多少?
某品牌补钙剂的主要成分是碳酸钙(杂质不含钙元素),向12g这种补钙剂样品中逐渐加入稀盐酸,盐酸质量和生成气体的质量如下表所示(杂质可溶于水,不和盐酸反应),第三次加入盐酸后,所得溶液中氯化钙的质量分数为20% 。求这份补钙剂含钙的质量分数。
| |
第一次 |
第二次 |
第三次 |
| 加入稀盐酸的质量 |
18.25g |
36.5g |
47.9g |
| 生成气体的质量 |
2.2g |
4.4g |
4.4g |
(8分)某兴趣小组的同学为分析一种石灰石样品中碳酸钙的质量分数,取20g样品放入烧杯,把60g稀盐酸分三次加入烧杯,使其充分反应(样品中所含杂质既不溶于水也不与稀盐酸反应),实验流程及数据如下(所有实验数据都不包括烧杯的质量,且不考虑H2O和HCl的挥发;操作X包括搅拌、过滤、洗涤、干燥、称量):
请回答:
(1)CaCO3中Ca与C的质量比为 ;
(2)实验时判断已充分反应的现象是 :其中a为 g;样品中碳酸钙的质量分数为 ;
(3)第三次反应过滤后所得溶液的pH 7(填“>”、“<”或“=”);为使该溶液
显中性且得到尽可能多的CaCl2,最后可向烧杯中加入过量的 (填序号)
| A.CaO | B.CaCO3 | C.Ca(OH)2 | D.CaCl2 |
(4)计算所用稀盐酸中溶质的质量分数(写出计算过程)
可能用到的相对原子质量:Ca:40 Cl:35.5 H:1 O:16 C:12
48、南漳华新水泥厂生产的水泥畅销各地,生产的原料之一有石灰石。某化学兴趣小组对石灰石进行探究。取该石灰石样品16g,把200g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水也不与稀盐酸反应)。请计算:
| 序号 |
加入稀盐酸的质量/g |
乘余固体质量/g |
| 第1次 |
50 |
11 |
| 第2次 |
50 |
6 |
| 第3次 |
50 |
4.8 |
| 第4次 |
50 |
m |
⑴上表中m的数值为 ;
⑵整个过程中参加反应的稀盐酸质量为 g(注意包括稀盐酸中的水);
⑶求第2次反应完毕后所得溶液溶质的质量分数(写出解题过程,结果精确到0.1﹪)
(6分)某实验小组要测定混有氯化钠的纯碱样品中Na2CO3的质量分数。取12g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡,共消耗稀盐酸72.4g,测得反应后溶液的质量为80g。请帮助实验小组完成以下计算:生成二氧化碳的质量。
反应后所得溶液中溶质的质量分数是多少?
某化学研究小组对当地的石灰石样品进行了研究.称取石灰石样品8g,把40g稀盐酸分四次加入样品中,测得实验数据见下表(假设石灰石样品中杂质不溶于水、不与盐酸反应,二氧化碳不溶解).试计算:
| 实验序号 |
第1次 |
第2次 |
第3次 |
第4次 |
| 加入稀盐酸的质量/g |
10 |
10 |
10 |
10 |
| 剩余固体物质的质量/g |
5.5 |
m |
1.6 |
1.6 |
m= g.
石灰石样品中CaCO3的质量分数。
计算稀盐酸的溶质质量分数