[江苏]2012届江苏省南京市白下区中考一模化学试题
下列物质的用途主要利用其化学性质的是
| A.氧气用于医疗急救 | B.干冰用于人工降雨 |
| C.铜、铝用于制作导线 | D.汽油用于衣物除油污 |
下列化肥中,属于复合肥料的是
| A.NH4H2PO4 | B.NH4NO3 | C.K2SO4 | D.Ca(H2PO4)2 |
某化学学习小组讨论辨析以下说法:①纯净水和矿泉水都是纯净物;②用活性炭可将硬水进行软化;③太阳能、风能和天然气都是可再生能源;④霉变的大米只要洗干净就可放心食用;⑤合金的强度和硬度一般比组成它们的纯金属更高、抗腐蚀性能更好;⑥回收利用废旧金属不仅可以节约金属资源,还可以减少对环境的污染。其中正确的是
| A.⑤⑥ | B.③⑤⑥ | C.②④⑤ | D.①②③④ |
早在春秋战国时期,我国就开始生产和使用铁器。下列有关铁的说法中正确的是
| A.铁是地壳中含量最丰富的金属元素 |
| B.高炉炼铁是利用焦炭在高温下把铁从铁矿石里还原出来 |
| C.铁生锈是铁与空气中的氧气、水蒸气等发生化学反应的过程 |
| D.铁丝能在空气中剧烈燃烧,火星四射,生成氧化铁 |
下图为“××泉水”商标的一部分,下列说法正确的是
| A.该“泉水”中不含任何化学物质 |
| B.其中钙、镁、钾等是指这些元素的单质 |
| C.该“泉水”常温下呈弱酸性 |
| D.商标中体积的单位“ml”书写不规范 |
小明对蜡烛及其燃烧进行探究,下列说法不正确的是
| A.从蜡烛上切一小块石蜡放入水中,石蜡浮在水面,说明石蜡的密度比水小 |
| B.取冷而干燥的小烧杯罩在蜡烛火焰上方,有水雾出现,说明石蜡中含有氢、氧元素 |
| C.在密闭容器中,蜡烛燃烧一段时间后熄灭,说明可燃物燃烧需要氧气 |
| D.用扇子可扇灭蜡烛火焰,说明将温度降至可燃物的着火点以下即可灭火 |
2012年2月29日,国务院同意发布新修订的《环境空气质量标准》,新标准增加了PM2.5监测指标。PM2.5是指大气中直径小于或等于2.5微米的颗粒物,主要来自于化石燃料的燃烧。下列有关化石燃料的说法不正确的是
| A.化石燃料是不可再生能源 |
| B.化石燃料完全燃烧时对空气不会产生污染 |
| C.石油是由沸点不同的化合物组成的混合物 |
| D.将煤隔绝空气加热使其分解成焦炭、煤焦油、煤气等的过程是化学变化 |
一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性强的金属首先被腐蚀。造船工业为了避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属是
| A.银块 | B.铜块 | C.锡块 | D.锌块 |
自来水消毒过程中常会发生甲、乙化学反应,其反应的微观过程可用下图表示:
下列说法正确的是
| A.物质D属于氧化物 |
| B.物质C在水溶液中以分子形式存在 |
| C.甲是复分解反应 |
| D.实验室可用过氧化氢溶液和二氧化锰制取氧气 |
在水溶液中可以大量共存的一组离子是
| A.H+、K+、OH- | B.Na+、H+、HCO3- |
| C.H+、NH4+、Cl- | D.Cu2+、NO3-、OH- |
除去下列物质中的少量杂质,所用试剂及方法不正确的是
| 选项 |
物质 |
杂质 |
试剂及方法 |
| A. |
NaCl 固体 |
泥沙 |
加水溶解、过滤、蒸发 |
| B. |
KNO3 溶液 |
Ba(NO3)2 |
滴加适量K2SO4溶液、过滤 |
| C. |
Na2SO4溶液 |
Na2CO3 |
滴加稀盐酸至不再产生气泡 |
| D. |
N2 |
O2 |
通过红热的铜丝 |
汽车用铅蓄电池中需要质量分数为28%的稀硫酸。若在实验室中用10g质量分数为98%的浓硫酸(密度为1.84 g/cm3)配制28%的稀硫酸,下列做法或说法正确的是(水的密度近似看作1g/cm3)
| A.将25mL水慢慢倒入盛有5.4mL浓硫酸的量筒中,并用玻璃棒不断搅拌 |
| B.将10g98%的浓硫酸沿烧杯壁慢慢注入盛有25mL水的烧杯中,并用玻璃棒不断搅拌 |
| C.若其他操作正确,量取25mL水时俯视读数,则所配稀硫酸中溶质的质量分数小于28% |
| D.配制该溶液时,若有浓硫酸沾到手上应立即用氢氧化钠溶液中和 |
β一胡萝卜素(C40H56)是一种天然的植物色素,它广泛存在于黄绿色蔬菜和水果中,一定条件下在人体内能够转化为维生素A(C20H30O)。下列有关说法正确的是
| A.维生素A中碳、氢、氧三种元素的质量比为20︰30︰1 |
| B.维生素A的相对分子质量为286g |
| C.维生素是人体必需的营养物质 |
| D.β一胡萝卜素由40个碳原子和56个氢原子构成 |
如图所示,在小烧杯乙和丙中分别放入不同的物质后,立即用大烧杯甲罩住小烧杯乙和丙,放置一段时间。下列有关说法不正确的是
| A.若乙和丙中分别放入浓盐酸和石蕊溶液,丙中溶液会变红 |
| B.若乙和丙中分别放入浓氨水和酚酞溶液,丙中溶液会变蓝 |
| C.若乙和丙中分别放入浓盐酸和硝酸银溶液,丙中会产生白色沉淀 |
| D.若乙和丙中分别放入水和浓硫酸,丙中溶质的质量分数会变小 |
把某稀硫酸分为等体积的两份,分别加入等质量的甲、乙两种金属粉末(甲、乙在生成物中均为+2价),反应后金属都没有剩余,产生H2的质量随时间变化的趋势如图。
下列说法正确的是
| A.甲的活动性比乙强 | B.甲的相对原子质量比乙小 |
| C.反应消耗等质量的硫酸 | D.反应消耗等质量的金属 |
两种不含结晶水的固体物质a、b的溶解度曲线如图,下列说法正确的是
| A.b的溶解度小于a的溶解度 |
| B.分别将t2℃时a、b两种物质的溶液降温至t1℃,肯定都有晶体析出 |
| C.在t2℃时,用a、b两种固体和水分别配制等质量的两种物质的饱和溶液,需要量取相同体积的水 |
| D.要从含有少量a的b溶液中得到较多的b晶体,通常可采用降温结晶的方法 |
A和B可发生反应:3A+2B ==A3B2,某学生做了3次该实验(每次均充分反应),反应前A和B的质量之和都是12g。有关实验数据见下表,x︰y的值可能为
| 序号 |
反应前A的质量 |
反应前B的质量 |
反应后A3B2的质量 |
| ① |
10g |
2g |
6g |
| ② |
4g |
8g |
6g |
| ③ |
xg |
yg |
9g |
A.3︰1 B.3︰2 C.l︰2 D.1︰1
现有六种物质:①小苏打、②水银、③盐酸、④酒精、⑤氮气、⑥石墨。
请选择相应物质的序号填空:
(1)空气中含量最多的气体是 (2)属于有机物的是
(3)医用体温计里的物质通常是 (4)可用于制铅笔芯的是
(5)发酵粉的主要成分之一是 (6)人体胃液中含有的酸是
酸性氧化物有对应的酸,碱性氧化物有对应的碱,如下表:
| 酸性氧化物 CO2 |
对应的酸 H2CO3 |
| 碱性氧化物 CaO |
对应的碱 Ca(OH)2 |
(1)酸性氧化物CO2和对应的酸H2CO3中,碳元素的化合价均为 ;碱性氧化物CaO和对应的碱Ca(OH)2中,钙元素的化合价均为 。
(2)与H2SO4对应的酸性氧化物为 (填化学式,下同);与Na2O对应的碱为 。
二氧化碳在生活和生产中具有广泛的用途。
(1)从宏观组成角度看,二氧化碳是由 组成的;从微观构成角度看,二氧化碳是由 构成的。
(2)化学反应在生成新物质的同时,还伴随着能量的变化,而能量的变化通常表现为热量的变化。例如,二氧化碳与碳的反应 热量(选填“吸收”或“放出”)。
(3)反应物相同时,若条件不同,产物有可能不同。例如,CO2+H2O===H2CO3,
6CO2+6H2O  6O2+ 。
6O2+ 。
(4)有二氧化碳生成的反应很多(如下图所示),请按要求写出一个化学方程式:
①有二氧化碳生成的置换反应: ;
②有二氧化碳生成的其他反应(不属于基本反应类型): 。
(5)过量排放二氧化碳到大气中,会引起 效应,使全球变暖。请写出一条防止该效应进一步增强的措施: 。
下表是元素周期表中部分元素的原子结构示意图,请回答有关问题:
| 周期 族 |
ⅠA (读作“第一主族”) |
ⅡA (读作“第二主族”) |
ⅢA (读作“第三主族”) |
| 第2周期 |
 |
 |
 |
| 第3周期 |
 |
 |
X |
| 第4周期 |
Y |
 |
 |
(1)1869年, 发现了元素周期律并编制了元素周期表(选填“拉瓦锡”或“门捷列夫”)。
(2)钠离子的核外电子数为 。
(3)经分析发现,元素的周期序数与原子的电子层数、元素的主族序数与原子的最外层电子数有着密切的关系。请推断X原子的最外层电子数为 ,Y原子的电子层数为 。
(4)若镓(Ga)元素与氯元素只能组成一种属于盐的化合物,该化合物的化学式为 。
根据下列装置图,回答有关问题: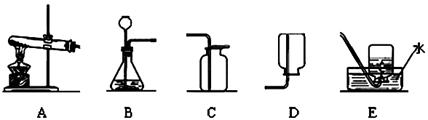
(1)利用上图中A、C装置的组合可以制取某种气体,实验室制取该气体的化学方程式是 ,验满方法是 。
(2)实验室通常利用上图中 装置的组合制取二氧化碳(选填字母),该反应的化学方程式为 。
①为了得到纯净、干燥的二氧化碳气体,除杂装置(如下图)的导管按气流方向连接顺序是 (选填字母)。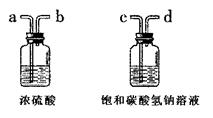
A.a→b→c→d B.b→a→c→d
C.c→d→a→b D.d→c→b→a
②常用澄清石灰水检验二氧化碳的存在,该反应的化学方程式为 ;若二氧化碳过量,二氧化碳又会与碳酸钙、水反应生成易溶的碳酸氢钙[Ca(HCO3)2],该反应的化学方程式为 。向含有氢氧化钙14.8g的石灰水里缓缓通入一定量二氧化碳,充分反应后若生成10g沉淀,则通入二氧化碳的质量可能为 (选填字母)。
A.4.4g B.8.8g C.13.2g D.17.6g
A—I为初中化学中常见的物质。已知A为金属氧化物,C为大理石的主要成分,D为蓝色沉淀,G、I均为只含有一种溶质的溶液。“→”表示物质间存在着相互转化的关系(部分生成物未标出),如下图所示。请回答下列问题:
(1)写出化学式:A ,D 。
(2)写出B与I反应的化学方程式: 。
(3)已知H为一定量锌粉和铁粉的混合物,与溶液G充分反应后过滤。向滤渣E中加入稀盐酸,有无色气体放出,则滤渣E中一定含有 ,滤液F中一定含有的金属阳离子是 。
市售“管道通”能使堵塞的管道畅通。小华通过实验对“管道通”中的物质成分进行了探究。
【提出问题】“管道通”中含有什么物质?
【查阅资料】(1)下水管里的淤积物主要为油污、食物残渣、毛发等。
(2)氢氧化钠是强碱,能去除油污、腐蚀毛发等,可用于疏通管道。
(3)铝粉为银灰色固体,铝与酸、碱溶液都能反应放出氢气,并放出大量热。例如,铝与盐酸反应的化学方程式是 , 铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH +2H2O====2NaAlO2 +3H2↑ 。
【猜想与验证】小华打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末。
| 实验操作 |
实验现象 |
| ① 将几粒白色固体颗粒放在表面皿上,放置一会儿 |
|
| ② 将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁 |
|
| ③ 向操作②得到的溶液中放入一段羊毛线,加热一段时间 |
羊毛线逐渐消失 |
猜想Ⅰ:白色固体颗粒为氢氧化钠。
结论:白色固体颗粒为氢氧化钠。
猜想Ⅱ:银灰色粉末为铝粉。
| 实验操作 |
实验现象 |
①按照下图安装两套装置 |
|
| ②向两套装置的试管1中分别依次加入银灰色粉末和稀盐酸、银灰色粉末和 |
都产生无色气体,试管1外壁温度明显升高 |
| ③待导管口有气泡均匀持续冒出时,收集一试管气体,验纯(两套装置操作相同) |
验纯时的操作和现象: |
| ④在导管口点燃气体(两套装置操作相同) |
都产生淡蓝色火焰 |
结论:银灰色粉末为铝粉。
【交流与反思】(1)老师告诉小华,氢氧化钾和氢氧化钠的性质非常相似。因此,要确认猜想Ⅰ是否正确,还需要学习如何检验钠元素的存在。
(2)使用管道通时,先将其中银灰色粉末添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水后立即堵上管道口,管道内迅速发生反应。请写出一个使用“管道通”时的注意事项:
。
氯化钡是一种可溶性重金属盐,广泛应用于化工领域。用毒重石(主要成分为BaCO3)制备氯化钡晶体工艺流程如下图:
(1)毒重石要进行粉碎的目的是 。若所得滤液1仍浑浊,则应采取的操作是 。
(2)滤液2中可循环利用的物质除水外还有 。洗涤氯化钡晶体最适宜的洗涤剂是
(选填字母)。
A.30℃水 B.30℃饱和氯化钠溶液 C.30℃饱和氯化钡溶液
(3)滤渣水洗的目的是 和 。
有一包白色粉末A,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验(实验流程如图):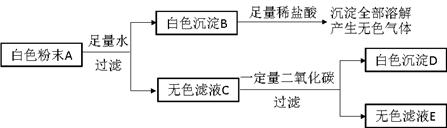
(1)取白色粉末A,向其中加入足量水,充分搅拌后过滤,得到白色沉淀B和无色滤液C。由此可判断,原白色粉末中一定不含有 。
(2)向白色沉淀B中加入足量稀盐酸,沉淀全部溶解,并产生无色气体。由此可判断,原白色粉末中一定含有 。
(3)向无色滤液C中通入一定量二氧化碳,充分反应后过滤,得到白色沉淀D和无色滤液E,由此可判断,原白色粉末中一定还含有 。
(4)若流程图中白色粉末A为20g,白色沉淀D为9.85g,无色滤液E中只含一种溶质。
①无色滤液E中的溶质为 ;
②通过计算确定20g白色粉末A中所含各物质的质量。
(请写出计算及推理过程)


 粤公网安备 44130202000953号
粤公网安备 44130202000953号