生活中处处有化学。
(一)请用下列物质的序号填空:
①小苏打 ②干冰 ③活性炭 ④熟石灰 ⑤硝酸钾 ⑥碳酸钙
(1)常用作人工降雨的是 ,
(2)可用作补钙剂的是 ,
(3)常用来改良酸性土壤的碱是 ,
(4)可用作复合肥的是 ,
(5)可用于净化自来水的是 ,
(6)常用作发酵粉的是 。
(二)盐城悦达汽车正以其优良的性价比得到了越来越多消费者的喜爱,其发动机既可以使用汽油,也可能使用目前国家推广使用的乙醇汽油。在汽油中加入适量乙醇就得到乙醇汽油。
(1)乙醇(C2H5OH)在空气中充分燃烧的化学方程式为 。
(2)关于乙醇汽油的下列说法中不正确的是 (填序号)。
| A.乙醇属于不可再生能源 | B.乙醇汽油是纯净物 |
| C.使用乙醇汽油可减少大气污染 | D.使用乙醇汽油可节省石油资源 |
(三)盐城机场航站楼使用了钢架结构
(1)钢属于 (“纯净物”或“混合物”)
(2)铁锈蚀是铁与空气中的 (填化学式)等物质作用的结果,防止钢铁锈蚀可采用的方法有 (写任意一种)。
(3)下图中,可表示金属铁的是 。

海洋中蕴含丰富的资源.
(1)海水淡化是解决淡水资源不足的重要方法.下列方法中,可以使海水变为淡水的是 (填字母序号).
A.滤纸过滤 B.吸附
C.沉降 D.蒸馏
(2)从海水中提炼出来的重水(D2O)可作原子能反应堆的中子减速剂和热传热介质.重水中重氢原子(D)的相对原子质量是2,则重水中氢元素的质量分数为 .
(3)从海水中制备纯碱和金属镁的流程如图所示:
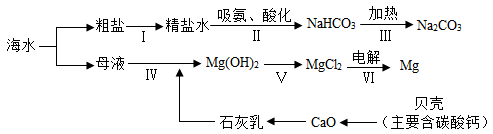
回答下列问题:
①步骤Ⅴ中所加试剂是 .
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下了物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为 (填字序号).
A.适量的盐酸
B.稍过量的Na2CO3溶液
C.稍过量的Ba(OH)2溶液
③第Ⅲ歩反应的化学方程式是 .
④在海边用贝壳作原料制生石灰,比用石灰石作原料的优点是 (写一条).
以化合价位纵坐标,物质的类别为横坐标所绘制的图象叫价类图、如图为硫的价类图,请分析该图后填空:

(1)E点表示的是二氧化硫,写出它的一条物理性质 ;
(2)如图中可表示K2SO4,这种盐的点是 (填字母);
(3)A点表示的物质类别是 ;
(4)写出由B点表示的化合物与氢氧化钠溶液反应的化学方程式
某一无色透明的溶液,可能含有Na2SO4、NaOH、Na2CO3、Ca(OH)2中的一种或几种,向其中加入氯化钡溶液,产生白色沉淀,再加稀硝酸,沉淀全部消失。则溶液中一定存在 ,一定不存在 ____、_____ ,可能存在 。
依据下列物质的用途填空(填字母)
| A.活性炭 | B.石墨 |
| C.生石灰 | D.小苏打 |
(1) 制铅笔芯.
(2) 是发酵粉的主要成分
(3) 去除冰箱异味
(4) 作食品干燥剂.
某地曾发生了一起亚硝酸钠中毒事件。亚硝酸钠外观酷似食盐且有咸味,亚硝酸钠和食盐的有关资料如下:
| 项 目 |
亚硝酸钠(NaNO2) |
氯化钠(NaCl) |
| 水溶性 |
易溶, |
易溶, |
| 熔 点 |
271℃ |
801℃ |
| 沸 点 |
320℃会分解,放出有臭味的气体 |
1413℃ |
| 跟盐酸作用 |
放出红棕色的气体NO2 |
无反应 |
(1)根据上表,请你写出亚硝酸钠的两个物理性质:
① ② ;
(2)检验亚硝酸钠的方法可以是: 。
现有一包固体混合物A,其中可能含有硝酸铵、硫酸钾、硝酸铜、氯化钠四种物质中的一种或多种.现按图所示进行检验,出现的现象如图中所述(假设过程中所有发生的反应都恰好完全反应).请你依据实验过程和产生的现象做出分析与判断:
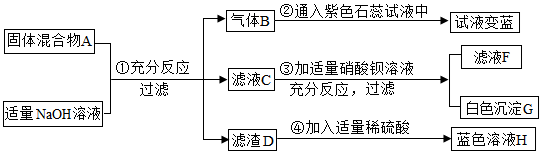
(1)气体B的化学式是 .
(2)步骤④发生反应的化学方程式 .
(3)通过上述现象判断,该固体混合物A中一定含有的物质是 ;不能确定是否含有的物质是 ,如果要证明混合物A中确实含有该物质,可用滤液F继续实验.请简要说出继续实验的操作步骤和现象 .
某白色固体可能是煅烧碳酸钙后的剩余物,为确定其成分,进行如下实验:

① 高温煅烧碳酸钙的化学方程式是 ;
② 分离B中难溶物的操作Ⅰ是 ;
③ 操作Ⅱ的目的是 ,D中白色固体可能是 ;
④ 为达到实验目的,还应进行的操作是 。
A、B、C是初中化学常见的三种物质且组成中都含有碳元素,在工业上,A广泛用于玻璃、造纸和洗涤剂的生产,B是氧化物,C为难溶性固体,A、C所属物质类别相同(“→”表示由一种物质转化成另一种物质,图中部分反应物、生成物及反应条件已略去),请回答下列问题:
(1)写出A、B的化学式:A ,B .
(2)写出A转化为C的化学方程式 ,该反应所属的基本反应类型为 .
右图是某同学做“粗盐的提纯”实验时的过滤装置图;

(1)写出标号的仪器名称:a (1) ,b (2)__
(2)图中明显缺少一种玻璃仪器,请写出需要补充的仪器名称是 (3) ,其作用 (4) 。
(3)过滤后的滤液在进行蒸发时也要用到上述补充的仪器,这种仪器在蒸发过程中的作用是 (5) 。
(4)某同学过滤后发现滤液依然浑浊,除了滤纸可能破损以外,请你再写出一种造成滤液浑浊的原因 (6) 。
(5)以下混合物能用“溶解-过滤”操作进行分离的是____(7)_____。
A.食盐和白糖 B.面粉和味精
C.食盐和味精 D.豆油和水
(6)“粗盐的提纯”实验步骤是:称量粗盐、__(8)__、__(9)___、__(10)___、称量精盐、计算。
称取5.0g粗盐,最终得到4.7g精盐,则精盐的产率是 (11) 。(用百分数表示)
(7)各小组的产率及评价如下:
| 组别 |
1 |
2 |
3 |
4 |
| 产率 |
75% |
83% |
88% |
72% |
| 教师对产率的评价 |
偏低 |
偏高 |
偏高 |
偏低 |
下列各组同学对造成产率偏高或偏低的原因分析,正确的是 (12) (填编号)。
A、第1组:烧杯里的食盐未溶解完就开始过滤
B、第2组:蒸发时,有固体物质飞溅
C、第3组:滤液浑浊就开始蒸发
D、第4组:蒸发时,精盐中还含有水分
(8)、为鉴别食盐水和蒸馏水,甲同学认为可用蒸发水分的方法。将所取的两种液体蒸干,留有固体物质,对应的液体是食盐水;没有固体物质残留的,对应的液体是蒸馏水。他选用的一组仪器是_____(13)_____。
A. 试管、酒精灯、漏斗、玻璃棒
B. 酒精灯、蒸发皿、铁架台(带铁圈)、玻璃棒
C. 托盘天平、酒精灯、量筒、玻璃棒
D. 烧杯、铁架台(带铁圈)、酒精灯、玻璃棒
某化工厂不断排放废气、废水(含硫酸),严重污染周边环境。
(1)排放在空气中的 是形成酸雨的主要物质。
(2)周边农民常用 来改良酸性土壤。
(3)用(2)中选用的物质还能降低废水的酸性,反应的方程式是 。
(4)环保部门责令该厂停产整顿,下列整改措施合理的是 。
A.加高烟囱,将废气排向高空
B.改进工艺,减少废水、废气的产生
C.将废水排放在湖中稀释
D.将废气循环利用
A与B有如下的反应:A+B→C+D
(1)若C为厨房内常用的调味品,A是人体胃液的主要成分,可帮助消化,则A是 ;若A、B两溶液恰好完全反应,则反应后溶液的pH 7(填“<”、“>”或“=”);写出A、B两溶液反应的化学方程式 .
(2)若B常用来改良酸性土壤;D是重要的化工原料且俗名叫苛性钠;B与CO2反应也能生成C;则A是 ,C的用途是 (只写一种).写出A溶液与B溶液反应的化学方程式
某金属冶炼厂的管道烟泥中含有炭黑及金属铜和锌。综合实践活动小组的同学设计了从管道烟泥中回收金属铜的实验方案,实验过程如图所示:

请回答:
(1)步骤①中,过滤操作使用了玻璃棒,其作用是 ;在过滤时,实践活动小组的同学发现 过滤速度很慢,原因可能是 (填一种可能的情况)。滤液B中的溶质有 (填一种)。
(2)步骤④中,所加入的金属X是当今世界上产量最高用途最广泛的金属,该反应的化学方程式是____________________
(3)除去不纯铜中的杂质金属X,可选用的试剂有 (填一种)。
(4)在进行“反应①”“反应③”“反应④”操作时,可将反应物加入 中(填仪器名称),然后_______________(填操作名称),使反应充分进行。
精盐(NaCl)和纯碱(Na2CO3)是两种常见之物。
(1)用化学方法区别这两种固体,可以选择下列哪一种物质?答:
| A.白酒 | B.米醋 | C.纯净水 | D.酱油 |
(2)王军同学不慎在精盐中混入了少量纯碱,他想重新得到精盐,设计了以下两个实验方案:

你认为合理的实验方案是 ,反应的化学方程式为_____________
说明另一方案不合理的理由:
海水是资源的宝库,海水淡化可获得淡水和浓海水.浓海水中主要离子的浓度如下:
| 离子 |
Na+ |
Mg2+ |
Cl﹣ |
SO42﹣ |
| 浓度/g/L |
63.7 |
28.8 |
144.6 |
46.4 |
从浓海水中提取金属镁的一段工艺流程如图所示:

(1)补全由贝壳生产石灰乳的相应转化中所需的条件或反应物:
贝壳 生石灰
生石灰 石灰乳
石灰乳
(2)写出反应1的化学方程式: .
(3)滤液X中溶质的主要成分有 (填化学式).
(4)物质Y的名称是 .
(5)将MgCl2溶液在一定条件下蒸发结晶、熔融电解可制得金属镁.则2L浓海水理论上可得到金属镁的质量为 g.