一包白色粉末可能含有 、 、 、 、 、 中的一种或几种,为判断其组成,进行如下实验:①取少量该白色粉末溶于水,产生白色沉淀,上层清液为无色;②取上层清液滴在pH试纸上,pH>7;③过滤,往得到的白色沉淀中滴入稀盐酸,白色沉淀部分溶解。则该白色粉末中一定含有,一定没有,可能含有。
(8分)现有一包固体混合物,可能含有Na2SO4、Na2CO3、NaCl、NaNO3中的两种或两种以上。小红想知道混合物的成分,便和实验小组同学共同设计完成了以下实验。A的溶液常用作干燥剂。
(1)写出A、B、D的化学式A________;B____________;D________。
(2)向样品溶液中加入A的稀溶液,所发生反应的化学方程式__________________,反应的
基本类型是________。
(3)实验结束了,小红得知混合物的组成可能是①__________;②__________;③__________。
氢氧化钠是重要的化工原料,在保存的过程中如果密封不严容易变质。今年以来,化工原料市场供不应求,各种化工原料价格持续上扬。某化工厂为了增加效益,计划将一批库存的氢氧化钠投入市场。如果你是质检员,请你按以下方案抽取样品对该批氢氧化钠进行检验,看是否变质。
【实验方案】

【推断和结论】
(1)若现象
为有气泡产生,则加入的
溶液可能是,说明氢氧化钠已经变质。
(2)为了进一步探究该产品变质的程度,再取少量样品,加入的
是过量的
溶液(
溶液呈中性),现象
为有白色沉淀,现象
为无色酚酞试液变红色,则证明该批产品(填"部分"或"完全")变质。
【反 思】久置的氢氧化钠变质的原因是(用化学方程式表示).
(7分)下图是对生成氯化钠反应关系的归纳与整理。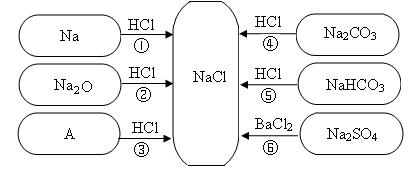
请回答下列问题:
(1)物质A是常见的碱,写出A的化学式:______。
(2)写出反应①的化学方程式:___________________。
(3)说出NaHC03在医疗上的一种用途:______________ 。
(4)反应③、④、⑤、⑥能够进行的原因是_______________。
(5)实验室配制200g 8%的NaCl溶液,需要水的质量是___________g,配制过程中为了加快NaCl的溶解,可以采取的措施是_____________。
一包白色粉末,由
、
、
、
、
中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验:
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液。则原白色粉末中一定不含有。
(2)取实验(1)滤出的白以沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体。则原白色粉末中一定含有。根据上述实验可推断:原白色粉末的组成有种可能。为进一步探究原白色粉末的组成,取实验(1)得到的滤液,向其中通入二氧化碳,产生白色沉淀,则可推断原白色粉末中一定还含有。
(10湛江22).(8分)某学校化学兴趣小组用NaCl固体(含有的杂质CaO)来配制一定质量分数的NaCl溶液,实验的流程图如下: 
请回答:
(1)写出适量HCl加入到溶液B中所发生反应的化学方程式为__________________________。
(2)操作2的名称是__________,在溶液A中加入过量碳酸钠的目的是________________。
(3)若要配制100g质量分数为10%的氯化钠溶液,除了用到天平、烧杯、量筒外,还需用到的玻璃仪器是__________,其作用是______________________________。
实验室有一瓶无色溶液,标签模糊,依稀可见
.为探究该溶液中是否有硫酸根,化学兴趣小组的同学设计以下甲、乙方案,并取样品实验、记录相关现象.

请根据上述信息,完成下列问题:
(1)方案甲得出的结论是:不能确定无色溶液中是否含有硫酸根.理由是.
(2)方案乙得出的结论是:无色溶液中含有硫酸根.则加入足量稀
的作用是;如果加入稀
有气泡产生,则可能发生反应的化学方程式是。(写1个)
(3)另取无色溶液少许,滴入紫色石蕊试液,溶液变红.若溶液中只含有一种阳离子,则方案乙中产生白色沉淀的化学方程式为。
(10芜湖12).某化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。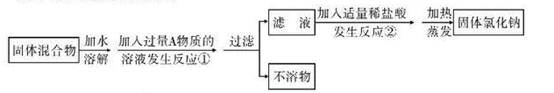
(1)写出A物质的化学式: ,写出A物质的俗称: 。
(2)写出反应②的化学方程式: 。
(3)反应①中加入过量A物质的目的是 。
反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度 (填“有”或“没有”)影响。
(4)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果 (填“增大”、“不变”或“减小”)。
某粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2,小青同学设计了以下实验方案来除去可溶性杂质。 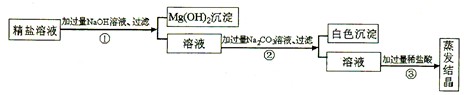
步骤①的化学方程式为_______________________________________。
步骤②中得到的白色沉淀是_________________________ (填化学式)
步骤③中加稀盐酸是为了除去溶液中的___________________。
| A.CaCl2 | B.MgCl2 | C.NaOH | D.Na2CO3 |
(8分)有某固体混合物,已知其中可能含有Na2CO3、CaCO3、CuSO4、FeCl3四种物质中的两种或多种。按下图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应)
试根据实验过程和发生的现象填写以下空白:
(1)常温下,气体A水溶液的pH ____________7(填“大于”“小于”“等于”之一)。
(2)该固体混合物中,一定不存在的物质是(写化学式)_____________________________,理由是:_______________________________。
(3)在滤液E中,一定大量存在的阴离子是(写离子符号)_____________________。
(4)写出过程③中一定发生反应的化学方程式______________________________________。
(5)写出过程①中发生反应的一个化学方程式_______________________ 。
以电解食盐水为基础制取氯气、氢氧化钠等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不符合电解要求,因此必须经过精制。以粗盐为原料的“氯碱工业”流程如下: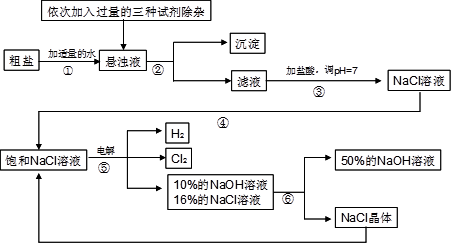
(1)氯气、氢氧化钠在工业上有广泛的用途。下列关于氢氧化钠的描述中,不正确的是 。
| A.能去除油污,可做厨房清洁剂 | B.易溶于水,溶解时放出大量的热 |
| C.水溶液能使石蕊溶液变红 | D.可用作某些气体的干燥剂 |
(2)操作②的名称是 ,该操作所需的玻璃仪器是 ;操作④的名称是 ,该操作需玻棒不断搅拌,这是为了防止 。
(3)操作①②间除杂质时所加的三种试剂是NaOH溶液、Na2CO3溶液、BaCl2溶液(均过量),其顺序要求是:Na2CO3溶液必须在BaCl2溶液之 (填“前”或“后”)加入。有同学提出用 溶液代替BaCl2溶液可达到同样的目的。
(4)电解饱和NaCl溶液的化学方程式是 。
(5)该流程中可以循环利用的物质是 。
在元旦联欢晚会上,被誉为化学魔术师的晓慧同学为同学们表演了一组化学魔术,在三支盛有液体的玻璃杯中,分别倒入用酒瓶装的一种液体,同学们看到下列奇特现象:A杯中变成了“红葡萄酒”(变为红色);B杯变成了“汽水”(产生大量的气泡);C杯中变成了“牛奶”(有白色沉淀)。请你来揭开魔术秘密:
(1)酒瓶中的液体可能是 。
(2)B杯中产生的气体是 。
(3)写出C杯中发生的化学方程式 。
(10肇庆市21).海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等。综合利用海水制备金属镁的流程如下图所示: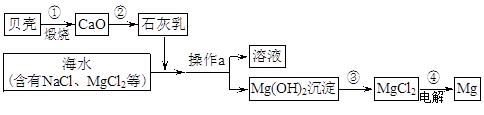
(1)贝壳主要成分的化学式是 。  (2)操作a的名称是 ,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、 。
(2)操作a的名称是 ,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、 。
(3)工业冶炼镁常用电解MgCl2的方法,反应为:MgCl2 Mg+ 。
(4)写出第②、③两步反应的化学方程式:
② ,③ 。
比较、分析、归纳是学习化学的重要方法。通过比较可以发现相同的反应物在不同外界条件下,会发生不同的反应。请参照示例归纳反应规律:
| 组别 |
化学方程式 |
规律 |
| 示例 |
 |
反应物相同时,反应物的量不同,生成物不同 |
| (1) |
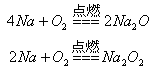 |
|
| (2) |
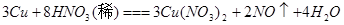 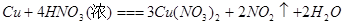 |
|
盐酸既是盐化工的重要产品,又是生产硅材料的重要原料。 如图归纳出了盐酸与其它物质间相互反应的关系(图中“——”表示相连的两种物质能发生反应)。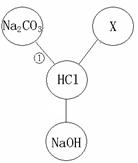
(1)若X是与其它三种不同类别的化合物,则X可以是(填化学 式) 。
(2)根据右图所示物质间关系,写出①反应的化学方程式: ;