粗盐中含泥沙、氯化钙、氯化镁等杂质,某同学自制的简易净水器中放置物质的顺序错误,使净水效果不理想。

(1)请按由上到下的顺序重新排列(填字母)。调整
后净化的盐水仍含可溶性杂质,他设计了下面的除杂流程:

(2)步骤①②都需要进行操作,步骤④需要进行操作。
(3)已知试剂X是碱溶液,则沉淀I为(写化学式),下列碱溶液不符合要求的是(填序号)。
| A. | 氢氧化钠溶液 | B. | 氢氧化钡溶液 | C. | 氢氧化钾溶液 | D. | 氢氧化钙溶液 |
(4)步骤②除去氯化钙的反应方程式是;步骤③中发生中和反应的化学方程式是。
废铁屑的主要成份是铁,同时还有少量铁锈(
),动物饲料硫酸亚铁的生产工艺之一如下图所示:

(1)在反应器中发生反应的化学方程式除
外还有:;
(2)滤液M中肯定含有的溶质的化学式是;
(3)在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和;
(4)滤液M经过操作B可得硫酸亚铁晶体(
)。已知硫酸亚铁的溶解度和析出晶体的组成如下表:
| 温度/℃ |
0 |
10 |
30 |
40 |
50 |
60 |
64 |
70 |
80 |
90 |
|
| 溶解度/g |
15.6 |
20.5 |
33.0 |
40.4 |
48.8 |
55.0 |
55.3 |
50.6 |
43.7 |
37.2 |
|
| 析出晶体 |
|
||||||||||
根据溶解度表,硫酸亚铁晶体(
)冷却结晶温度最高不超过℃;
(5)在化学反应中,若有元素化合价变化的反应定义为氧化还原反应。下列反应类型肯定是氧化还原反应的是(填字母编号);
A.化合反应 B.置换反应 C.分解反应 D.复分解反应
在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等。
将无水硫酸亚铁(
)隔绝空气加强热,生成产物有三氧化二铁和其它氧化物,试写出该反应的化学方程式。
人类的生产和生活都离不开金属
(1)如图所示的金属制品中,利用金属导热性的是 _________ (填字母序号).
(2)铝具有很好的抗腐蚀性能,用电解氧化铝的方法可以制取铝,氧化铝中铝元素和氧元素的质量比为 _________ .
(3)铁是应用最广泛的金属,工业上常以赤铁矿(主要成分Fe2O3)和一氧化碳为原料炼铁,该反应的化学方程式为 _________ .
(4)赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热可得铜,请将反应的化学方程式补充完整:2Cu2O+Cu2S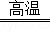 6Cu+ _________ .
6Cu+ _________ .
(5)某实验室废液中含有稀硫酸、硫酸亚铁和硫酸铜,若向其中加入一定量的锌,充分反应后过滤,向滤渣中加入盐酸,有气泡产生.则滤渣中一定含有的物质是 _________ ,滤液中一定含有的物质是 _________ .
下图所示A~G是初中化学常见的物质。图中“→”表示转化关系,“—”表示相互能反应。已知A是人体胃液中含有的酸,G是最轻的气体,B和C含有相同的元素。
(1)写出F的化学式 ,E物质的一种用途 。
(2)C和D之间的反应需要高温条件,写出它们发生反应的化学方程式: 。
(3)A和E发生反应的化学方程式是 ,反应的基本类型属于 。
实验室中的试剂一般要密封保存,否则可能会与空气接触而变质.某研究性学习小组发现一瓶未密闭的固
体,对其成分提出以下假设,并完成了实验探究.
假设1:只含
;假设2:含
和
;假设3:只含
(1)成分中可能含有
的原因是(用化学方程式回答).
(2)取少量样品于试管中,加入足量稀盐酸,观察到,说明假设2或假设3成立.
(3)进一步探究的过程如下:

①"操作1"的名称是_.
②"固体 "的化学式是.
③加入足量 溶液的作用是.
(4)变质试剂也有利用价值,从 和 的组成和性质看,这瓶变质试剂的用途是(写出一条).
氯化钾固体样品中混有少量碳酸钾和硫酸钾两种杂质,为了获得纯净的氯化钾,将样品溶解,按如图所示步骤进行提纯.已知试剂1为氯化钾溶液,B、C为固体难溶物,每步骤加稍过量的试剂.

(1)固体难溶物B含有碳酸钡和;
(2)检验步骤①已除去杂质的方法(操作、现象、结论)是;
(3)试剂Ⅱ中溶质的化学式:,试剂Ⅲ的名称是;
(4)由E获得氯化钾晶体的分离操作名称是.
某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50
5%的氯化钠溶液。
实验一:下图是同学们做粗盐提纯实验的操作示意图。


请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是。
(2)操作⑥中的错误是。
(3)粗盐提纯实验的操作顺序为(填操作序号)、称量精盐并计算产率。
(4)操作④中,当观察到时,停止加热。
实验二:用提纯得到的精盐配制了50
5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有(填序号)。
①氯化钠固体仍然不纯 ②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数 ④装瓶时,有少量溶液洒出
(1)用图
所示的方法收集
,为了检验是否集满,将放在集气瓶口。
(2)用图
所示方法蒸发食盐水,仪器
的名称是,仪器Y的名称是。

如图所示为各物质之间的转换关系,请回答下列问题:
(1)写出下列字母所代表物质的化学式:A: D: E: ;
(2)写出过程②的化学方程式 ,其基本反应类型是 。
科学家研究利用海水处理、回收废气中二氧化硫,其流程如下(序号表示化学反应): (1) 写出反应①的化学方程式 。
(1) 写出反应①的化学方程式 。
(2) SO2和CO2的化学性质相似。用氢氧化钠溶液吸收SO2时除生成NaHSO3外还可能生成
(写化学式)。
(3) 反应④中发生反应的离子是 。
(4)现有含二氧化硫的废气a g,经过氢氧化钠溶液充分吸收后得到亚硫酸氢钠,消耗氢氧化钠b g,通过计算求二氧化硫在废气中百分含量。
亚硝酸钠是一种工业用盐,它有毒、有咸味,外形与食盐相似。人若误食会引起中毒,危害人体健康,甚至致人死亡。亚硝酸钠的水溶液呈碱性,食盐的水溶液呈中性。如果让你来鉴别亚硝酸钠和食盐,你如何操作?并写出现象和结论。
实验 操作: 。
现象和结论: 。