运用学过的化学知识填空:
(1)检验一块布料是羊毛织品还是合成纤维织品,最简便可靠的方法是。
(2)测定溶液的酸碱度最简便的方法是使用。
(3)在工业上,广泛用于玻璃、造纸、纺织和洗涤剂生产的盐是。
(4)硬水煮沸后硬度降低是因为水中减少的缘故。
(5)加油站、面粉加工厂、纺织厂、煤矿的矿井内,都标有"严禁烟火"的字样或图标,因为这些地方的空气中常混有,它们遇到明火,有发生爆炸的危险。
目前,科学家提出一种最经济最理想的获得氢能源的循环体系(如图),下列说法错误的是()

| A. | 燃料电池能够使化学反应产生的能量转化为电能 |
| B. | 该氢能源的循环体系能够实现太阳能转化为电能 |
| C. | 在此循环中发生了反应: |
| D. | 燃料电池可以将 、 中的能量完全转化为电能 |
近年来,媒体常报道出煤气中毒的惨剧,煤气中毒是由于含碳燃料不充分燃烧生成 引起的.下列做法可以有效地避免煤气中毒发生的是( )
| A. | 严寒的冬天,在狭小密闭的房间内烧炭取暖,在炭盘旁边放一盘水 |
| B. | 在清洗偏远的水井时,边用柴油作为能源的抽水机放到井内抽水,边派人戴着口罩到井下洗井 |
| C. | 将液化石油气热水器安装在密闭的冲凉房内 |
| D. | 将液化石油气热水器安装在冲凉房外面,且要通风透气 |
下图是某燃煤发电厂处理废气的装置示意图。
1、使用此废气处理装置,可减少 的排放,从而减少酸雨对环境造成的危害;
2.写出该电厂处理废气的总的化学反应方程式
下列“课外实验”不能获得成功的是


| A.鲜花变色 | B.自制炭黑 | C.自制汽水 | D.硬水软化 |
化学就在我们身边,它能改善我们的生活。根据所学知识回答:
(1)若不小心被蚊虫叮咬(蚊虫能分泌出蚁酸),下列物质可用于涂抹以减轻疼痛的是 (填字母)。
A.食醋 B.食盐水 C.肥皂水
(2)常用燃料完全燃烧可以节约资源并减少对空气的污染。增大燃料与空气的接触面积和提供充足
的 都有利于燃料的完全燃烧。
(3)公共场所常用“84消毒液”(NaClO溶液)进行环境杀菌。NaClO中Cl元素的化合价是________。
(4)吸烟有害健康。在公共场所,非吸烟者会因少数吸烟者吸烟造成被动吸烟,这是因为________________________________________________________________________。
下列做法不利于减轻环境污染的是()
| A. | 燃料脱硫以减少酸雨的产生 | B. | 随意丢弃废旧电池 |
| C. | 农药化肥的合理施用 | D. | 开发利用清洁能源 |
使用下列能源会对环境造成污染的是
| A.风能 | B.石油 | C.氢能 | D.太阳能 |
(9分)化学就在我们身边,人类的衣、食、住、行都离不开化学。
(1)某服装标签如上图1,该服装面料含有的合成纤维是 (填“棉”或“涤纶”);新衣服拿在手里,有时能闻到特殊气味,能闻到气味的原因是 。
(2)人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”,在“五金”顺序中把金属 (填元素名称)的位置移到最后,正好符合由弱到强的金属活动性顺序。自行车车轮的钢圈会生锈主要是因为 。
(3)“西气东输”后,家庭用上了天然气,灶具开关通过电子打火引燃天然气,此过程满足燃烧的条件是 ;天然气燃烧反应的化学方程式为 。
(4)从海水中提取粗盐一般可采用 方法。上图2是特殊情况下使用的应急净水器。利用该净水器将2000g含氯化钠3%的海水暴晒4小时,收集到500g可饮用水,此时剩余海水中氯化钠的质量分数为 。
为减缓化学反应速率,下列做法合理的是
| A.面团发酵时放在温热处 | B.在食品密封包装时充入氮气 |
| C.煤燃烧时向煤炉中鼓入空气 | D.用食醋除水垢时使用浓度高的食醋 |
(3分)化学与生产、生活密切相关。请用下列物质的序号填空。
①甲醛;②天然气;③大理石;④木炭;⑤氯化钠。
(1)属于化石燃料的是__________。
(2)其水溶液可用于浸泡动物标本的是 。
(3)可用来制取氢氧化钠、氯气等的是 。
今年“两会”期间,北京连续出现严重的雾霾天气,给人们出行带来了严重的影响。国家环境保护部门对外公布《环境空气质量标准》,将PM2.5作为评价项目纳入标准。PM2.5是指大气中直径小于或等于2.5微米的颗粒物。
(1)防PM2.5专用口罩利用了活性炭的 作用;
(2)请你提出一条防治空气污染的合理建议: 。
(5 分)“绿色化学”是 21 世纪化学发展的主导方向。
⑴ “化学反应的绿色化”要求原料物质中所有的原子完全被利用且全部转入期望的产品中。 下列化学反应中, 符合“化学反应绿色化”要求的是 (填选项序号)。
① MgCl2通电 Mg+Cl2↑ ②CaO + H2O = Ca(OH)2
③Na2CO3+ Ca(OH)2 = CaCO3↓+ 2NaOH
(2)煤和石油中都含有硫元素,它们燃烧的废气中含有 SO2气体,SO2与水及氧气反应会导致硫酸型酸雨的形成,酸雨的 pH 7 (填“大于”、“小于”、“等于”之一)。
(3)当空气被 SO2严重污染时,可通过飞机喷洒物质 X 的粉末,使空气中的 SO2含量明显降低,发生反应的化学方程式为 2X + SO2 + O2 ="=" 2CaSO4 + 2 CO2, X 的化学式是 。
(4)当今社会,随着汽车用量的急剧增加,能源和环保问题日趋严峻,研制以太阳能、氢能等新型能源为动力的汽车迫在眉睫。氢燃料汽车使用过程中发生反应的化学方程式为 ;从环保的角度看,使用氢燃料汽车最突出的优点是 。
(10分)某市热电厂使用的燃料是含硫较多的煤.该厂附近一所中学的同学经常闻到空气有异味,且空气能见度差.学习化学后,同学们意识到这有可能是该厂排出的废气超标造成的,于是在老师的指导下做了探究实验,请你填写下列空白,
【提出问题】该厂附近所降雨水是否是酸雨?空气里SO2是否超标呢?
【查阅资料】I.我国关于SO2在风景区、居民区、工厂区的空气质量最高标准分别见下表: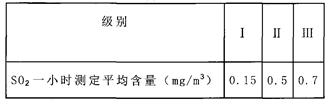
Ⅱ.硫酸钡既不溶于水,也不溶于酸(如不与稀盐酸、稀硝酸等反应).
【设计实验1】第一组同学取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示: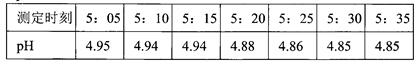
所降雨水 (填“是”或“不是”)酸雨。在测定时间内酸雨pH减小的原因可能是__
【设计实验2】第二小组同学设计以下步骤来测定空气中SO2的含量.
(1)用2L的空可乐瓶采集工厂附近的空气样品,采样的具体操作是:
(2)向取回的装有空气样品的可乐瓶中倒入NaOH溶液,盖紧瓶塞后充分振荡,仿照CO2与NaOH溶液的反应,写出SO2与NaOH溶液反应的化学方程式:
(3)加入一定量氧化剂H2O2,使其中Na2SO3完全转化为Na2SO4.向可乐瓶中加入过量的BaCl2溶液.Na2SO4和BaCl2反应的化学方程式为: ____
(4)经过过滤、洗涤、烘干,称量固体质量为1.165mg.
计算:1.165mg硫酸钡中硫元素的质量为 mg.由质量守恒定律可知,2L空气样品中SO2的质量为 mg.
由空气质量标准可得出结论:该厂排放的SO2严重超标.。
【发现新问题】考虑到空气中的各种气体成分,第一组认为第二组同学的SO2的含量偏大,其依据是 ;你提出的实验改进方案是
【反思与应用】为尽快改善该地区的空气质量,请你提出一条合理化建议:
某研究人员按下图所示流程进行“燃煤烟气的脱硫研究”。实验中,SO2和O2
的混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环。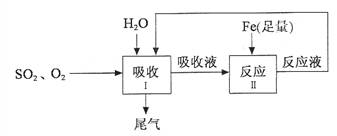
(1)Ⅰ中发生反应的化学方程式是2SO2+2H2O+O2 2X,则X的化学式是 。
(2)Ⅱ中发生反应的化学方程式是 。
(3)随着反应液流入Ⅰ中,吸收液中X的生成速率明显加快,其原因可能是 。
(4)经过多次循环后,反应液可以用来制备FeSO4·7H2O,它在医疗上常用于治疗
(选填字母)。
| A.甲状腺肿大 | B.佝偻病 | C.龋齿 | D.贫血症 |