如图所示A—G是初中化学常见的物质。图中“→”表示转化关系,“—”表示相互能反应。已知A是人体胃液中含有的酸,G是最轻的气体,B、C、D、E、F都是氧化物。请回答: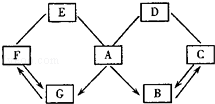
(1)G的化学式为__________。
(2)E与F发生化学反应的基本类型是__________,写出物质A的一种用途__________;
(3)A、D发生反应的化学方程式可能为_________。
用括号内物质不能一次性鉴别下列各组物质的是
| A.CaO、CaCO3、KCl三种固体(水) |
| B.CaCl2、K2CO3、K2SO4三种溶液【Ba(OH)2溶液】 |
| C.Cu、Fe、CuO三种固体(稀盐酸) |
| D.NaCI、Ca(OH)2、HCI三种溶液【K2 CO3溶液】 |
下列各组物质按单质、氧化物、酸顺序排列的一组是( )
| A. |
、 、 |
B. |
、 、 |
| C. |
、 、 |
D. |
、 、 |
FeCl3可用作催化剂和外伤止血剂.某实验兴趣小组利用FeCl3腐蚀电路铜板后的溶液(主要成分为FeCl2、CuCl2)进行了氯化铁回收实验。
该实验小组同学通过查阅资料,进行了尝试。
【阅读资料:】
不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离。右表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH
| |
Fe(OH)3 |
Cu(OH)2 |
| 开始沉淀的pH |
1.9 |
4.7 |
| 沉淀完全的pH |
3.2 |
6.7 |
(1)进行操作x时,应用到的仪器有:铁架台、玻璃棒、烧杯和 。
(2)实验中,步骤b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式 ;你认为步骤b调节溶液的pH到 (填数值范围)比较合适。
(3)实验中,步骤d加稀盐酸前,因缺少 (填操作名称)而使获得的氯化铁溶液不纯。
(4)FeCl3溶液容易生成Fe(OH)3发生变质,在保存FeCl3溶液时,常向FeCl3溶液中加入某种酸,以防止FeCl3溶液变质,你认为选用 (用字母表示)最合理。
A.稀硝酸 B.稀硫酸 C.稀盐酸 D.稀醋酸.
~
表示初中化学常见的物质.其中
是大理石的主要成分.各物质间相互转化关系如图所示(反应条件已略去)
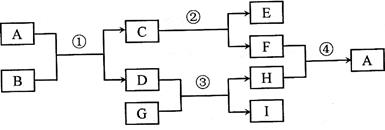
请回答下列问题:
(1)
的化学式为.
(2)
的一种用途是.
(3)上述转化中没有涉及的基本反应类型是.
(4)反应③的化学方程式为(只写一个).
在科学研究中,常常用到“对照”的科学方法,下列实验与这一科学方法不符合的是
| |
A. |
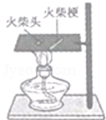 研究可燃物燃烧的条件 |
B. |
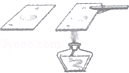 研究蒸发快慢影响的因素 |
| |
C. |
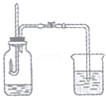 研究空气中氧气的含量 |
D. |
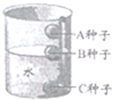 研究种子萌发的条件 |
在实验室,某同学将氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中,直至过量.加入氢氧化钠溶液的质量(横轴)与混合溶液中溶质质量(纵轴)的关系如图所示.
(1)实验中,观察到的现象为.
(2)实验中发生反应的化学方程式有.
(3)图中
线段对应溶质质量减小的本质原因是.
(4)向反应后的溶液中加入适量
溶液,恰好完全反应后溶液中的溶质有.

A-J是初中化学常见的物质,它们之间的转化如图1所示("-"表示相邻的两物质可以发生反应,"→"表示箭头前面的物质可以转化为箭头后面的物质;部分反应的反应物、生成物和反应条件没有标出)。图2所示的是部分物质的相关信息;I、J中含有相同的金属元素,H的相对分子质量比E的大。
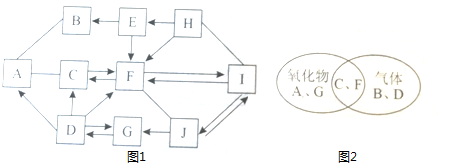
(1)F的化学式是。
(2)物质I俗称。
(3)写出上述物质转化过程中属于分解反应的一个化学方程式。
(4)写出H→E的化学方程式。
硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有
、
、
),设计了如图的试验流程(有些反应的部分反应物和生成物已省略).查阅资料发现常温下,单质硅(
)不能与盐酸反应,但能与氢氧化钠溶液反应(
).
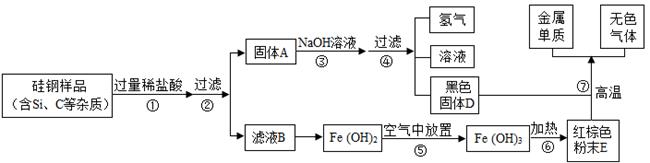
根据以上信息,回答下列问题:
(1)固体A的成分为,滤液B中的金属阳离子为;
(2)写出步骤⑦中发生反应的化学方程式;其基本反应类型为;
(3)在过滤操作时,若发现滤液浑浊,应;
(4)步骤⑤中发生的是化合反应,尝试写出其化学方程式.
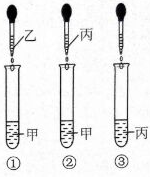
如图所示,其中甲、乙、丙、丁、戊分别是铁、盐酸、氢氧化钙、二氧化碳、碳酸钠中的一种.图中相连的两圆表示相应物质能发生反应,已知乙是铁.下列说法错误的是()
| A. | 五种物质中,只有铁是单质 | B. | 丙是盐酸 |
| C. | 戊是氢氧化钙 | D. | 甲与丁反应属于复分解反应 |
某白色固体可能由CaCO3、NaCl、BaCl2、NaOH、Na2SO4 中的一种或几种组成的,实验记录如下图:
下列分析正确的是
| A.原固体中不含BaCl2、Na2SO4 |
| B.原固体中一定含有CaCO3、BaCl2、NaOH |
| C.步骤②中得到的溶液中溶质只有CaCl2 |
| D.确定固体中是否有NaCl可以取无色溶液A直接滴入AgNO3溶液 |
除去下列物质中混有的少量杂质(括号内为杂质),操作方法正确的是
| 选项 |
物质 |
操作方法 |
| A |
NaCl(Na2CO3) |
加水溶解后加入稍过量盐酸、蒸发、结晶 |
| B |
KCl(MnO2) |
加水溶解、过滤、洗涤、干燥 |
| C |
CO2(HCl) |
通过盛有足量氢氧化钠溶液的洗气瓶 |
| D |
Cu(CuO) |
通入足量氧气并加热 |
甲、乙、丙、丁都是初中化学中最常见的物质,已知它们由
、
、
、
、
、
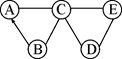
6种元素中的2种或3种组成,丙与甲、乙、丁都能发生反应。将这四种物质的溶液按下图所示相互滴加,现象为:①产生白色沉淀;②有气泡冒出;③无明显现象。
(1)甲、乙、丙、丁都属于(填"单质"或""化合物")。
(2)试管②中产生的气体是(填化学式)。
(3)试管①中反应的化学方程式是。
(4)向试管③滴加的溶液溶质可能是(填化学式,下同)或。
除去以下物质中的少量杂质,所用试剂及方法正确的是
| 选项 |
物质 |
杂质 |
所用试剂及方法 |
| A |
|
通入足量的
溶液 |
|
| B |
溶液 |
稀盐酸 |
加入过量的
,过滤 |
| C |
溶液 |
溶液 |
加入足量的
粉,过滤 |
| D |
溶液 |
溶液 |
加入适量的
溶液,过滤 |
已知A、B、C、D、E为初中化学中常见的五种不同类别的物质,其中A为年产量最高的金属单质,各种物质间的反应和转化关系如图所示(“——”表示相连的两种物质之间可以发生反应,“―→”表示一种物质可以转化为另一种物质;反应条件、部分反应物和生成物已略去)。请写出:
(1)B的化学式:_____________________;
(2)D与E反应的化学方程式:_ __。