甲、乙、丙、丁是初中化学中常见的四种物质,它们有如下关系:①甲+乙→ ,②乙+丁→ ,③丙+乙→ .则甲是,乙中一定含元素,丙物质是(填一种最简单的有机化合物).
工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3),生产的关键是在沉淀池中让 NaCl、NH3、CO2和H2O尽可能多地转化成NaHCO3(固体沉淀物)和NH4Cl(溶液)。主要生产流程如下: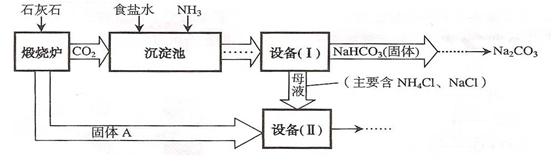
(已知2NH4Cl+Ca(OH)2==CaCl2+2NH3 ↑+2H2O)
(1)“煅烧炉”中发生反应的化学方程式是 。
(2)若在实验室里分离“设备(I)”中的混合物,用到的操作的名称是 。
(3)在“设备(Ⅱ)”中固体A与水反应的化学方程式是 。该反应属于 反应(填写基本反应类型)。
(4)对“设备(Ⅱ)”中的母液处理后,除水以外可在本流程中再利用的物质有 (填写化学式)。
(5)请写出一个该生产流程的优点: 。
请根据下列假设,分析物质间的转化关系,并进行物质的推断:
(1)假设
溶液与
溶液恰好完全反应,生成白色沉淀A与溶液B,过滤后,溶液B再与过量的
溶液反应,生成蓝色沉淀C和溶液D,则溶液D中溶质的组成为:(填化学式,多填、少填、错填均不给分,下同)
(2)假设
溶液与
溶液充分反应,生成白色沉淀A与溶液B,过滤后,溶液B再与适量
溶液反应,均恰好沉淀完全,生成蓝色沉淀C和溶液D。
②溶液D的几种组成中有两种组成所含溶质种类最多,所含溶质分别是、;
③溶液D的几种组成中都一定含有的溶质是。
请分析、比较以下几组化学反应,得出结论。
| 组别 |
化学方程式 |
结论 |
| I |
|
反应物相同,生成物不同, 原因。 |
| II |
|
反应物相同,生成物不同, 原因。 |
| III |
|
反应物相同,生成物不同, 原因。 |
| IV |
(反应缓慢) (反应迅速) |
反应物相同,反应速率不同, 原因。 |
| 实践与应用 |
科学探究正努力实现对化学反应的控制,很多化学家致力于研究二氧化碳的"组合转化"技术,把过多二氧化碳转化为有益于人类的物质。若让二氧化碳和氢气在一定条件下反应,可生成一种重要的化工原料,反应的化学方程式如下: ,推断X的化学式是。 |
(1)下列所示的粒子结构示意图中,属于同一种元素的是(填序号).

(2)金属材料在生产、生活中应用非常广泛.
①钢铁是重要的金属材料,它属于(填"纯净物"或"混合物").
②工业上用一氧化碳和赤铁矿(主要成分为氧化铁)冶炼铁,其反应的化学方程式是.
③某同学为了验证
三种金属的活动顺序,设计了如下一组实验:
| A. |
将锌片浸入稀硫酸溶液中 |
B. |
将铜浸入稀硫酸溶液中 |
C. |
将锌片浸入硫酸亚铁溶液中 |
该组实验还不能完全证明三种金属的活动性顺序,需要补充一个实验才能达到目的,你认为应该补充的实验是
.
(5分)右图是检验鸡蛋壳中是否含有碳酸根离
子的部分实验装置图.请回答问题:
(1)在下图中,写出标出仪器A的名称,液体药品B的名称,并将实验装置图补充完整;
(2)若鸡蛋壳中含有碳酸根离子,右侧装置内你能观察到的现象是 。
我国制碱工业先驱侯德榜发明了"侯氏制碱法"。其模拟流程如下:

(1)反应①的化学方程式为,反应②的基本反应类型为。
(2)工业上用分离液态空气的方法制取氮气,属于变化。(填"物理"或"化学")
(3)操作a的名称是,实验室进行此操作时所需的玻璃仪器有烧杯.玻璃棒. 。
(4)写出NH4Cl的一种用途。
科学兴趣小组在调查一化工厂时,发现有个车间排出的废水澄清透明,呈黄色.为测定该废水中所含的物质,他们进行如下实验(假设能发生的反应均恰好完全反应):
(1)用pH试纸测试,测得pH为2.
(2)取一定量废水溶液,加入Ba(NO3)2溶液,无现象.
(3)另取一定量废水溶液,加入AgNO3溶液后,过滤,得到白色沉淀A和滤液.
(4)向滤液中加入NaOH溶液,得到红褐色沉淀B.
由此可知:该废水溶液呈 性;所得的红褐色沉淀B为 ;废水溶液中肯定含有的盐是 .
轻质碳酸钙的成分是CaCO3,是无味的白色粉末。它应用于铜版纸、邮票纸等纸制品中,可以提高纸制品的稳定性、硬度和耐热性。它在国内的工业生产方法主要是碳化法,生产流程如下:

(1)步骤③中包含的操作名称是 。
(2)上述步骤中,发生化合反应的化学方程式为 。
(3)石灰石与轻质碳酸钙的差别是 (写出一条)。
请根据下图回答问题:

① 将图1和图6连接可以制取氧气,反应的化学方程式为 ,证明氧气已经集满的现象是 。若用图6收集一瓶含1/4空气的氧气,操作的方法是 。
② 图2中仪器A的名称为 ,它在装置中的主要作用是 。甲同学用图2和图 连接来制取二氧化碳,装置中加入盐酸的量至少要 。
③ 乙同学在图2基础上增加了一块带孔的隔板(如图3),则大理石应放在 处(填“a”或“b”),该装置中加入盐酸的量至少要 ;若加入盐酸过多,则有可能产生的后果是 ,要使反应停止,其操作是 。
④ 丙同学用过氧化氢溶液和二氧化锰制取氧气,反应的化学方程式为 。反应前他事先往试管中加入了少量的水,甲同学由此产生了疑问,提出了猜想:
猜想1:加水可以起到稀释的作用,使反应速度变缓。
猜想2:……
甲同学根据猜想进行了实验:每次取15mL 15%的过氧化氢溶液,稀释成不同溶质
质量分数,在其他条件相同的情况下进行实验。记录数据如下:
| 实 验 |
1 |
2 |
3 |
4 |
5 |
| 过氧化氢溶液溶质质量分数 |
1% |
3% |
5% |
10% |
15% |
| MnO2粉末用量/g |
0.5 |
0.5 |
0.5 |
0.5 |
0.5 |
| 收集到500mL气体时所用时间/s |
560 |
186 |
103 |
35 |
12 |
| 反应后液体温度/℃ |
26 |
38 |
43 |
59 |
71 |
根据表中数据可知:过氧化氢溶液的溶质质量分数对反应速度的影响是 。
甲同学的猜想2是:加水可以 。
除杂
⑴要除去CO气体中混有的少量CO2,反应的化学方程式____________________
⑵要除去CO2气体中混有的少量CO,反应的化学方程式____________________
如图是有关二氧化碳的几个性质实验:

A B C D E
(1)A中看到的现象有_________________,由此说明二氧化碳具有的性质是___________________。
(2)B中往装满二氧化碳的矿泉水瓶中倒入少适量水振荡后,矿泉水瓶变瘪的原因是:_______________。
(3)C中通入二氧化碳后石蕊试液变成_____色,将所得液体加热,发生的反应文字表达式为____________。
(4)E中的现象是___________________、_____________________。
(5)以上实验,只能体现二氧化碳的物理性质的是________(填序号)。
镁是一种用途广泛的国防金属材料,目前大部分镁都是利用从海水中提取镁盐制得的,工艺流程如下图所示:
请你根据上述材料,回答下列问题:
(1)操作①的名称是 (填“溶解”、“过滤”、“蒸发”之一)。
(2)试剂C中溶质的化学式是 。
(3)从海水中提取MgCl2时,经历了“MgCl2→Mg(OH)2→MgCl2”的转化过程,请分析这样做的目的是 。
(4)某校化学活动小组在实验室用蒸馏水和氯化镁配制了氯化镁溶液,模仿海水进行氯化镁含量的测定。学习小组的同学取该海水样品190 g,向其中加入氢氧化钠溶液,产生沉淀的质量与所加氢氧化钠溶液质量的关系曲线如图所示。请计算:上述海水样品中氯化镁的溶质质量分数是多少?(精确到0.1%)
某化学兴趣小组探究常温下碳酸钠饱和溶液的酸碱度。
[猜想与假设]溶液的pH可能是(填入你的猜想与假设):
①pH>7;②pH ;③pH 。
[设计与实验]小方、小钟、小陈三位同学进行了如下实验:
小方:取pH试纸于玻璃片上,用玻璃棒蘸取碳酸钠溶液沾在pH试纸上,测得pH>7。
小钟:取pH试纸于玻璃片上,先用蒸馏水润湿pH试纸,然后用玻璃棒蘸取碳酸钠溶液沾在pH试纸上,测得pH>7。
小陈:取pH试直接浸入碳酸钠溶液中,测得pH>7。
[评价]以上三位同学中操作规范的是 同学,
其余两位同学操作上的错误是 ; 。
[结论]从物质的类别看,碳酸钠是一种 (填“酸”或“碱”或“盐”),它的溶液显碱性,说明显碱性的溶液 (填“一定”或“不一定”)是碱的溶液。
[应用]根据碳酸钠溶液显碱性,说出它在日常生活中的一种用途: 。
化学是在分子、原子层面上认识和创造物质的一门科学。
(1)物质是由微粒构成的。在铁、二氧化碳、食盐三种物质中,由分子构成的是 。
(2)过氧化氢是一种常用的杀菌消毒剂,其原因是过氧化氢分子中含有“过氧基”(—O—O—)。据此推测,下列物质中,可用作杀菌消毒剂的是 (填序号)。
(3)气体A和气体B接触可发生反应,其微观过程如下所示。

①该反应过程中,属于氧化物的是 。
②将等体积的两只集气瓶分别盛满A、B,如图1所示进行实验。若相同条件下,气体的体积比等于分子个数比, 则图1实验中充分反应后,剩余的气体是 。