海洋是一个巨大的资源宝库,海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钠等.如图为综合利用海水制备金属镁的流程.
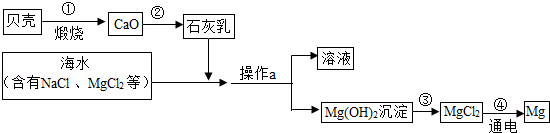
该流程中没有涉及的化学反应是( )
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
有一包固体粉末,可能是NaOH、Na2SO4、MgCl2、CuSO4中的一种或几种组成,为了分析固体粉末的成分,取少量该固体粉末进行实验,实验方案设计如下:
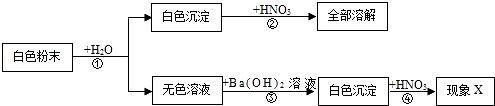
(1)固体粉末中一定有 .
(2)若现象X为“沉淀不溶解”或“沉淀部分溶解”,结论是固体粉末中 ;若现象X为“沉淀全部溶解”,结论是固体粉末中 .
(3)写出实验步骤②的化学方程式 .
(3)简单修改上述实验方案,可取消第④步实验,修改的方法是 .
科学兴趣小组在调查一化工厂时,发现有个车间排出的废水澄清透明,呈黄色.为测定该废水中所含的物质,他们进行如下实验(假设能发生的反应均恰好完全反应):
(1)用pH试纸测试,测得pH为2.
(2)取一定量废水溶液,加入Ba(NO3)2溶液,无现象.
(3)另取一定量废水溶液,加入AgNO3溶液后,过滤,得到白色沉淀A和滤液.
(4)向滤液中加入NaOH溶液,得到红褐色沉淀B.
由此可知:该废水溶液呈 性;所得的红褐色沉淀B为 ;废水溶液中肯定含有的盐是 .
用盐酸可以清除铁锈(主要成分为Fe203),盐酸中主要含有H20分子、H+、c1﹣.某探究小组为探究稀盐酸中的哪种微粒能使氧化铁溶解,设计了如下实验方案,得出了初步结论.
(1)请填写下表中的实验结论:
| 实验过程 |
实验现象 |
实验结论 |
| 向盛有少量Fe2O3的试管中加入NaCl溶液振荡 |
固体不溶解 |
|
(2)是否需要做“向Fe2O3,中加入水”的对比实验?为什么?
下列实验操作能达到目的是
| 选项 |
实验目的 |
实验操作 |
| A |
检验某未知溶液是否为碱溶液 |
测量溶液的pH |
| B |
鉴别稀H2SO4和稀HCl溶液 |
取样,加入适量的Ba(NO3)2溶液 |
| C |
除去CuSO4溶液中过量的H2SO4 |
加入适量的NaOH溶液 |
| D |
除去HCl中的水蒸气 |
通过盛装NaOH固体的U形管 |
A.A B.B C.C D.D
如图是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方,进行实验.请完成实验报告:

| 实验目的 |
实验现象 |
实验结论 |
| 测定空气中 的体积分数. |
白磷着火燃烧,活塞先右移,后左移,最后 停在刻度约为 (填整数)的位置上. |
空气的成分按体积计算, 约占  . . |
鸡蛋腐败会发出一种无色、有臭鸡蛋气味的气体(H2S).硫化氢气体是一种大气污染物,它在空气中点燃能完全燃烧生成二氧化硫和水,把硫化氢气体通入浓硫酸中,发生的反应为:H2S+H2SO4(浓)=SO2+S↓+2H2O
(1)从上述叙述中,归纳出硫化氢的物理性质:① 、② ;硫化氢的化学性质是:① 、② .
(2)若工厂排放的尾气中含有硫化氢,用浓硫酸来吸收是否可以? ,原因是 .
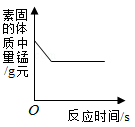
下列图像能正确反映对应变化关系的是
 |
 |
 |
 |
| A.一定质量的碳酸钠中不断加入盐酸 |
B.向一定质量的铜锌合金样品中不断加入稀硫酸 |
C.用酒精灯加热一定质量的高锰酸钾固体 |
D.向盛有少量二氧化锰的烧杯中不断加入过氧化氢溶液 |
轻质碳酸钙的成分是CaCO3,是无味的白色粉末。它应用于铜版纸、邮票纸等纸制品中,可以提高纸制品的稳定性、硬度和耐热性。它在国内的工业生产方法主要是碳化法,生产流程如下:

(1)步骤③中包含的操作名称是 。
(2)上述步骤中,发生化合反应的化学方程式为 。
(3)石灰石与轻质碳酸钙的差别是 (写出一条)。
甲、乙、丙、丁4种气体,由氢、碳、氧3种元素中的1~2种组成。
(1)甲是最清洁的燃料。甲是 。
(2)乙和丙均为氧化物,在一定条件下可以相互转化,它们相互转化的化学方程式是 、 。
(3)在一定条件下,丁与氧气反应生成乙和水,参加反应的丁、氧气和生成水的质量比为13︰40︰9。则丁中各元素的质量比是 。
同学们对实验“煅烧石灰石”展开了探究。资料:石灰石中的杂质高温不分解且不与稀盐酸反应

①为证明石灰石已分解,三位同学设计方案如下:
I.甲同学按图一所示进行实验(煤气灯能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式 (1) 。
II.乙同学按图二所示进行实验,观察到B中液体变 (2) 色,A实验的作用 (3) 。
III.丙同学取一定质量的石灰石煅烧,一段时间后发现固体质量减轻,证明石灰石已分解。
你认为哪位同学的方案不合理?并写出理由 (4) 。
②为证明石灰石是否完全分解?丁同学对丙同学煅烧后的固体又进行了如下探究
| 实验步骤 |
实验现象 |
结 论 |
| (5) |
有气泡产生 |
石灰石未完全分解 |
水是生命的源泉,下列变化与水相关。请回答:
①二氧化碳溶于水发生反应的化学方程式是 (1) 。
②自来水厂净水过程中常用到活性炭,其作用是 (2) 。
③铁丝在氧气中燃烧时,集气瓶内放少量水的目的是 (3) 。
④除去粗盐中泥沙等难溶性杂质的实验步骤:

I. 操作a的名称是 (4) ;
II. 三个步骤都用到的玻璃仪器是 (5) 。
⑤甲和乙两种固体物质(不含结晶水)的溶解度曲线如下图所示,回答下列问题:
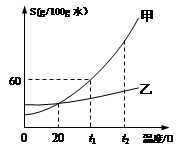
I.在 (6) ℃时,甲和乙两种物质的溶解度相等。
II.t1℃时,将50g固体甲加到50g水中,充分搅拌后所得溶液的质量为 (7) g。
III.甲的饱和溶液中含有少量的乙,由该液体得到固体甲采用的方法是 (8) 。
IV.若将甲物质的不饱和溶液变为饱和溶液,下列说法正确的是 (9) 。
A.溶剂的质量一定变小 B.溶质的质量可能不变
C.溶质的质量分数一定变大 D.溶液的质量变大
⑥下图是对20℃一定质量的丙溶液进行恒温蒸发结晶的实验过程,请回答:
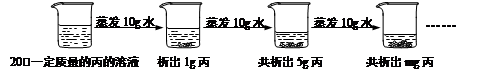
I.蒸发前原溶液是 (10) (填“饱和”或“不饱和”)溶液;m的数值是 (11) 。
II.依据上述实验,你认为丙的溶解度随温度变化的趋势是 (12) (填字母)。
A.随温度升高而增大 B.随温度升高而减小 C.无法判断
某固体A在一定条件下可发生如图所示的变化:
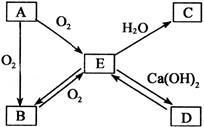
(1)它们各是什么物质?(写化学式)
A ,B ,
C ,D 。
(2)写出指定反应的化学方程式:
A→E 。
B→E 。
用碳、一氧化碳还原氧化铜的仪器、装置如下图。(连接装置的橡皮管省略)



请回答以下问题:
① 一氧化碳还原氧化铜的实验中,除A装置外,还需选用的仪器、装置组合是 (填字母),选用该仪器、装置的目的是 、 。
② 碳还原氧化铜的实验中(将A中的酒精灯换成酒精喷灯),反应的化学方程式是 。
③ 用碳和一氧化碳还原氧化铜的两个实验中,装置A中观察到的现象是 。
④ 现有一包混有少量碳粉的氧化铜粉末,为了测定其碳粉的质量分数,称取m g样品进行高温加热,实验过程中获取两组数据:
Ⅰ.反应前后仪器a中质量减少x g;
Ⅱ.吸收生成物的仪器中质量增加y g。
假设反应充分,称量准确,你认为应选择哪组数据进行计算会更为合理准确?你的理由是 ,请列出计算碳粉质量分数的式子 。(用m、x、y表示)。
某学习小组准备探究气体的测定和数据处理方法。
【提出问题】利用碳酸钙与稀盐酸反应来测定生成CO2的量。
【实验设计】通过下列两个实验分别测定CO2的质量和体积。

实验一 实验二
【分析处理】
实验一:
① 将小烧杯中的稀盐酸分几次加入到大烧杯中,并不断搅拌,判断反应后盐酸过量的依据是 。
② 若稀盐酸足量,计算理论上能产生二氧化碳的物质的量 。(根据化学方程式进行计算)
实验二:
③ 先连接好装置,再 (填操作),然后装好药品,最后将20mL稀盐酸快速推入锥形瓶中。若缓慢推入,则可能造成的后果是 。
④ 实验记录如下(表中数据在相同温度、相同压强条件下测定):
| 时间/min |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
| 注射器读数/mL |
60.0 |
85.0 |
88.0 |
89.0 |
89.5 |
89.8 |
89.9 |
90.0 |
90.0 |
90.0 |
根据以上实验过程和数据综合分析,最终生成CO2的体积是 mL。
【反思与评价】
⑤ 经过分析,下列说法错误的是 。
A.实验一的操作简单,便于读数
B.实验一最终得到的数据和通过计算得出的理论值完全相等
C.实验二在密闭体系内反应,更环保
D.实验二中若将碳酸钙粉末改成块状的大理石,更安全