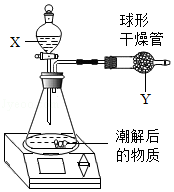
小余取8.0g干燥的氢氧化钠固体于敞口的锥形瓶中,观察到氢氧化钠固体发生潮解,一段时间后测得锥形瓶内物质质量为10.0g。为进一步探究上述现象的成因,小余立即用如图装置进行实验:将试剂X逐滴滴入锥形瓶中,直至不再产生气泡为止,测得装置前后质量减少了1.1g。(不考虑滴加液体体积、气体密度变化和结晶水的生成)
下列推断正确的是( )
①试剂X可以是稀硫酸
②固体Y可以是生石灰
③滴加试剂X前锥形瓶内水的质量为0.9g
④若没有球形干燥管,测得氢氧化钠固体从空气中吸收水的质量会偏小
A.①③B.①④C.②③D.②④
金属在生产和生活中有广泛的应用。
(1)铁在潮湿的空气中易生锈的原因是 。
(2)向硝酸银溶液中加入一定量的锌和铜的混合粉末,充分反应后过滤,滤液呈蓝色,则滤出的固体中一定含有 ;滤液中一定含有的金属离子是 (写离子符号)。
(3)某同学称取黄铜(铜锌合金)样品20g放入锥形瓶中,向其中加入100g稀硫酸恰好完全反应,测得反应后剩余物的质量为119.8g,则所用稀硫酸中溶质的质量分数为 。
如图所示的四个图象能正确反映对应变化关系的是( )
A.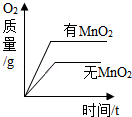 两份完全相同的双氧水在有无MnO2情况下产生O2
两份完全相同的双氧水在有无MnO2情况下产生O2
B.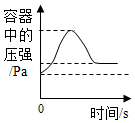 在密闭容器中用红磷测定空气中氧气的含量
在密闭容器中用红磷测定空气中氧气的含量
C.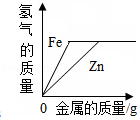 向等质量等质量分数的稀硫酸中,分别加入足量的铁粉和锌粉
向等质量等质量分数的稀硫酸中,分别加入足量的铁粉和锌粉
D.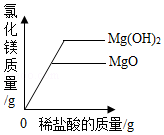 向等质量的氧化镁、氢氧化镁中,分别加入质量分数相同的稀盐酸至过量
向等质量的氧化镁、氢氧化镁中,分别加入质量分数相同的稀盐酸至过量
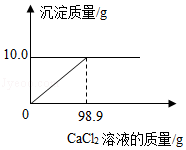
称取NaCl和Na2CO3的固体混合物11.1g,加入100.0g水配成溶液后,向其中逐渐加入一定浓度的CaCl2溶液。所加CaCl2溶液的质量与生成沉淀的质量关系如图所示。(提示:Na2CO3+CaCl2═CaCO3↓+2NaCl)
(1)恰好完全反应时生成CaCO3的质量是 g。
(2)当恰好完全反应时,计算所得溶液中溶质的质量分数。(写出计算过程)
(1)麦芽糖的化学式是C12H22O11,则每个麦芽糖分子中氢、氧原子的最简个数比为 ,麦芽糖中碳、氢、氧三种元素的质量比为 (填最简整数比)。
(2)鸡蛋壳中的主要成分是碳酸钙,小华为检测鸡蛋壳中碳酸钙的含量,进行的实验及实验数据如图所示。请回答下列问题:
(信息:鸡蛋壳中其他成分与稀盐酸接触不产生气体。)

①根据质量守恒定律可知,完全反应生成气体的质量为 g。
②计算鸡蛋壳中碳酸钙的质量分数。(写出计算过程,精确到0.1%)
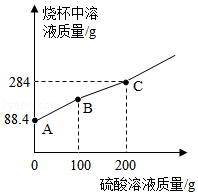
现有盛88.4g Na2CO3和NaOH混合溶液的大烧杯,向其中滴加质量分数为9.8%的H2SO4溶液,充分搅拌,烧杯中溶液的质量与滴加H2SO4溶液的质量关系如图所示,回答下列问题:
(1)写出AB段发生反应的化学方程式 。
(2)BC段可以观察到大烧杯的溶液中有气泡产生,则生成气体的质量为 g。
(3)B点时,大烧杯中的溶液pH 7(填“>”、“=”或“<”)。
(4)C点时,所得溶液为不饱和溶液。求溶液中溶质的质量分数。(写出计算过程)
现有一定质量的由两种金属组成的混合物。加入过量的稀盐酸,充分反应,测得生成H20.2g,将反应后的溶液蒸发,得到11.1g固体。则金属混合物的组成不可能是( )
A.Mg FeB.Fe ZnC.Zn MgD.Al Fe
将12.5g混有二氧化锰的氯酸钾固体加热至质量不再减少,冷却后称量固体的质量为7.7g。
(1)反应时生成氧气的质量为 g。
(2)计算反应前固体中二氧化锰的质量分数(要求写出计算过程)。
为了测定某纯碱样品中Na 2CO 3的质量分数。某化学兴趣小组的同学称取该纯碱样品11.0g,加入到足量的稀盐酸的烧杯中,充分反应后,称取烧杯内物质的总质量,发现比反应前物质的总质量减少了4.4g(纯碱样品中杂质不溶于水,不与酸反应)。求该纯碱样品中Na 2CO 3的质量分数(精确到0.1%)。
下列各图象不能正确反映其对应变化关系的是( )
A. 电解水
电解水
B.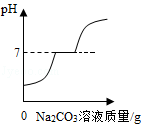 向氯化钙和盐酸的混合溶液中加入过量的碳酸钠溶液
向氯化钙和盐酸的混合溶液中加入过量的碳酸钠溶液
C. 向等质量的氧化锌和氢氧化锌中加入质量分数相同的稀盐酸至过量
向等质量的氧化锌和氢氧化锌中加入质量分数相同的稀盐酸至过量
D.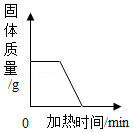 加热木炭和氧化铜的混合物
加热木炭和氧化铜的混合物
现有含氯化钠杂质的碳酸钠样品,取6.95g样品溶于水,配制成52.2g溶液。此溶液与50g某溶质质量分数的盐酸恰好完全反应,得到100g溶液。请分析计算:
(1)生成二氧化碳的质量是 。
(2)所得溶液中溶质的质量分数(写出计算过程)。
碳还原氧化铜的实验装置如图甲、乙所示。甲图中酒精灯上网罩的作用是 。
[提出问题]碳燃烧时可能生成CO 2也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
[作出猜想]猜想Ⅰ:CO;猜想Ⅱ:CO 2;猜想Ⅲ: 。
[设计方案]实验装置如图乙所示。打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通入一段时间氮气。
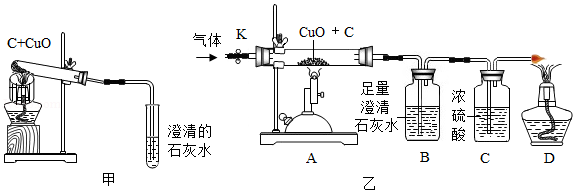
方案一:从定性观察角度判断
(1)实验时装置A处的现象是 。
(2)若B中无明显现象,D处的气体能点燃,则猜想 (填序号)成立。
方案二:从定量计算角度判断
取一定量碳粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:
| |
反应前的质量 |
反应后的质量 |
| A(玻璃管+固体) |
m 1 |
m 2 |
| B+C(广口瓶+混合液) |
m 3 |
m 4 |
(3)若猜想Ⅱ成立,则理论上(m 4﹣m 3) (m 1﹣m 2)(填">""<"或"=")。
(4)若猜想Ⅲ成立且CuO全部转化成Cu,则参加反应的碳粉的质量m的取值范围是 [交流反思]实验开始前缓缓通入氮气的目的是 。
硫酸镁和硫酸的混合溶液中,硫元素的质量分数占4.8%.向100g该混合溶液中加入氢氧化钠溶液,恰好完全反应,测得消耗氢氧化钠溶液的质量为100g。下列说法不正确的是( )
| A. |
氢氧化钠溶液中溶质质量分数为12.0% |
| B. |
所得溶液中溶质质量为21.3g |
| C. |
生成氢氧化镁沉淀的质量为8.7g |
| D. |
氢氧化钠溶液中钠元素质量为6.9g |
下列图象分别对应四个变化过程,能正确反映对应变化关系的是( )
| A. |
|
| B. |
|
| C. |
|
| D. |
|