某同学对若干块矿石样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应).请计算:
| 序号 |
加入稀盐酸质量(g) |
剩余固体质量(g) |
| 第1次 |
10 |
5.5 |
| 第2次 |
10 |
m |
| 第3次 |
10 |
1.2 |
| 第4次 |
10 |
1.2 |
(1)8g的石灰石样品中含有杂质 克?
(2)如表中m的数值应为 ?
(3)稀盐酸的质量分数是多少?
有一矿山上的石灰石样品,其中只含杂质二氧化硅(二氧化硅是一种既不溶于水也不与盐酸反应且耐高温的固体).小琳和他的同学想测定该样品中碳酸钙的质量分数,他们取一块石灰石样品,将其粉碎后,称出6g放入烧杯内(烧杯的质量为20g),然后加入50g足量稀盐酸,用玻璃棒搅拌至不再产生气泡为止.反应所需时间(t)和烧杯及其所盛物质的总质量(m)的关系如图所示.

试回答:
(1)实验结束后,共放出 g二氧化碳
(2)该石灰石样品中碳酸钙的质量分数是多少?
珍珠粉是由珍珠经加工制成的白色粉末,含有碳酸钙、蛋白质等成分,是重要的药品、化妆品原料.但市场上出现的假珍珠粉外观上与真珍珠粉差不多,肉眼往往无法辨别它们.
(1)为了寻找区分真假珍珠粉的方法,科学兴趣小组的同学进行了如图1实验:
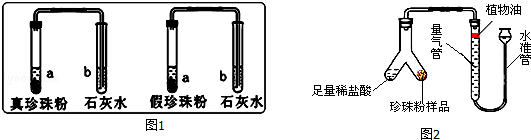
实验一:分别取真假珍珠粉适量置于两支试管中,加一定量的稀盐酸并将产生的气体通入澄清石灰水中,发现澄清石灰水均变浑浊,说明真假珍珠粉均含有 .
实验二:分别取真假珍珠粉稍许置于铁片上灼烧,发现真珍珠粉能闻到烧焦羽毛气味;假珍珠粉未闻到烧焦羽毛气味,由此可得出结论:假珍珠粉中不含 .
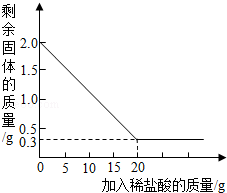
(2)为了比较真假珍珠粉中碳酸钙的含量,共进行了三次实验,每次各取5g真假珍珠粉,分别置于如图2实验装置中(稀盐酸足量且真假珍珠粉中只有碳酸钙与稀盐酸会反应生成气体),测定生成气体体积数据如下表:
| 样品气体体积mL次数 |
第一次 |
第二次 |
第三次 |
| 假珍珠粉 |
117.50 |
117.28 |
117.05 |
| 真珍珠粉 |
111.52 |
111.66 |
111.86 |
①量气管中水面上方加一层植物油的目的是 ,由实验数据可知:真珍珠粉中碳酸钙的含量 假珍珠粉(填“>”、“<”、“=”).
②根据三次测量结果,取平均值,算得5g真珍珠粉生成的气体质量为0.22g,求:真珍珠粉样品中CaCO3的质量分数.
在学习酸的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是因为里面含有氯化铁.为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),同学们做了如下实验:取10g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如图所示的关系.

(1)根据图中信息可知,与10g工业盐酸中的氯化铁反应的氢氧化钠溶液的质量为 g
(2)求该工业盐酸中氯化铁的溶质质量分数.(结果保留至 0.1%)
科学兴趣小组同学在综合实践活动中了解到,某石灰厂有一批石灰石原料,其中含有的杂质二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温时不发生分解反应).为了测定该石灰石的纯度,兴趣小组同学取用2克这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸20克分4次加入,充分反应后,经过滤、干燥等操作后称量,每次盐酸用量及剩余固体的质量见表,利用实验数据绘制的图象见图.
| 稀盐酸的用量 |
剩余固体的质量 |
| 第一次加入5克 |
1.5克 |
| 第二次加入5克 |
克 |
| 第三次加入5克 |
0.5克 |
| 第四次加入5克 |
0.3克 |
计算:
(1)分析上述图与表,第二次加入稀盐酸后,剩余固体的质量是 克;
(2)该石灰石样品中碳酸钙的质量分数;
(3)所用稀盐酸中溶质的质量分数是多少?
如图是稀盐酸和氢氧化钠溶液,其中一种物质逐滴加入另一种物质过程中溶液酸碱度的变化情况.

(1)该实验操作是将 滴加到另一种溶液中.
(2)图中 点时溶液中酸和碱恰好完全反应.
(3)若要将36.5克10%的盐酸全部反应完,需要NaOH多少克?(HCl+NaOH═NaCl+H2O)
精盐(NaCl)和纯碱(Na2CO3)是两种常见之物.
(1)用化学方法区别这两种固体,可以选择下列哪一种物质?
| A.白酒 | B.米醋 | C.纯净水 | D.酱油 |
(2)王军同学不慎在精盐中混入了少量纯碱,他想重新得到精盐,设计了以下两个实验方案:
方案一:固体混合物 溶液
溶液 固体
固体
方案二:固体混合物 溶液
溶液 固体
固体
你认为合理的实验方案是 .
说明另一方案不合理的理由: .
(3)假设(2)中固体混合物有53克,加入足量的稀酸充分反应后,生成4.4克,二氧化碳气体,求该固体混合物中氯化钠的质量分数.
火力发电厂用石灰石泥浆吸收废气中的二氧化硫以防止污染环境,其反应方程式为:
2CaCO3(粉末)+2SO2 + O2 ="==" 2CaSO4+2CO2.
(1)若100克废气中含6.4克二氧化硫,则处理100克这种废气需含碳酸钙(CaCO3)80%的石灰石 克;
(2)处理上述100克废气,可得到含CaSO4 85%的粗产品多少克?(请写出计算过程)
某化工厂利用海水资源进行联合生产,制备氢氧化钠和甲醇等物质。其化工流程如下:
已知:2H2+CO CH3OH
CH3OH
回答下列问题:
(1)电解食盐水的化学方程式为: ;在实验室进行电解水的实验中,为了增强导电性,往往向水中加入少量稀硫酸,而不能加入氯化钠,理由是 。
(2)若该工厂每天可生产80吨甲醇(CH3OH),需要提供 吨氢气。
(3)该工厂每生产80吨甲醇需要消耗多少吨26%的氯化钠溶液?(第3问写出计算过程)
实验室用锌和稀硫酸反应制取氢气的化学方程式为:Zn+H2SO4═ZnSO4+H2↑,要制取0.6克氢气,需要锌多少克?如果反应后所得到的ZnSO4溶液质量为200克,计算所得到的ZnSO4溶液的溶质质量分数是多少?(保留一位小数)
鸡蛋壳的主要成分是碳酸钙,为了测定蛋壳中碳酸钙的质量分数,小刚和小勇同学进行了如下实验。实验过程和测定的相关实验数据如下所示:请回答相关问题:

(1)逸航同学根据“蛋壳残渣质量为4.3g”,求得蛋壳中碳酸钙的质量分数为 ;
(2)鑫烁同学根据“反应过程中减少的质量”,也求得了蛋壳中碳酸钙的质量分数,请你写出鑫烁的计算过程和结果。
(3)逸航和鑫烁根据不同的数据求得蛋壳中碳酸钙的质量分数有明显差别,请你分析其中可能的原因 。
某氯碱工厂排放的尾气里含有毒的氯气(Cl2),为防止其污染空气,工厂用氢氧化钠溶液吸收氯气并得到消毒液[主要成分是次氯酸钠(NaClO)],此反应的化学方程式为:Cl2+2NaOH=NaClO+NaCl+H2O。若溶液中含有8kg的氢氧化钠。
计算:(1)理论上可吸收氯气的质量;
(2)可得到次氯酸钠的质量。
化学兴趣小组对某种粗锌(主要成分为锌,杂质不与酸反应)样品中锌的含量进行了测定。如图所示,称20 g该粗锌样品置于烧杯(质量为58.8 g)中,加入100 g足量稀硫酸,待粗锌完全反应后,称得烧杯及烧杯中剩余物总重量为178.4 g。

(1)硫酸(H2SO4)中氢、硫、氧三种元素的质量比为 。
(2)反应过程中产生氢气的质量为 g。
(3)计算该粗锌样品中锌的质量分数(写出计算过程及结果)。
秸秆是一种相对清洁的可再生能源,平均含硫量只有0.38%,而煤的平均含硫量为1%。某地燃烧秸秆的发电厂一年燃烧秸秆约2.0×105 t,相当于燃烧1.0×105 t煤。假设燃料中硫元素经燃烧后都转化为SO2,试计算该发电厂燃烧秸秆比燃烧煤每年少排放多少SO2?
载人宇宙飞船内常用含氢氧化锂(LiOH)的过滤网吸收宇航员呼出的CO2,以净化空气。若载人宇宙飞船内每名宇航员平均每天呼出的CO2为550 L,则吸收一位宇航员每天呼出的CO2需氢氧化锂的质量是多少?(写出计算过程;二氧化碳气体的密度为2.0 g∙L-1 ;化学方程式:2LiOH+CO2=Li2CO3+H2O)