近年来,我国高铁飞速发展,已成为世界上唯一高铁成网运行的国家。请回答下列问题。
(1)制造高铁列车使用了多种材料。下列高铁列车的部件中,其主要材料属于金属材料的是 (选填字母序号)。
| A. |
玻璃车窗 |
| B. |
镁铝合金车体 |
| C. |
塑料小桌板 |
| D. |
涤纶座套 |
(2)高铁电路多用铜质导线,这是利用了铜的延展性和 性。
(3)高铁刹车片由合金锻钢制作,时速300公里以上的列车紧急制动时,轮毂盘面和刹车片的温度瞬间达到700℃以上,合金锻钢应该具备耐磨和 等特性。
(4)建造高铁需要消耗大量的铝、铁等金属。工业炼铁的原理是氧化铁(Fe 2O 3)和一氧化碳在高温条件下反应,其化学方程式为 。
(5)车身表面烤漆不仅美观,还能起到防锈的作用。其防锈的原理是 。
(6)目前世界上已有50%以上的铁得到了回收利用。回收利用废旧金属的社会意义是 (写出一条即可)。
某工厂附近海水中含有较多Na2CO3等物质。该工厂采用海水脱硫技术吸收燃煤烟气中的SO2,其主要设备及流程如下:

(1)海水脱硫设备中,排出的海水呈碱性的是 (填字母序号)。
A.海水泵 B.吸收塔 C.曝气池①D.曝气池②
(2)向曝气池①内通入空气后,主要有两个化合反应发生,写出其中一个反应的化学方程式 。
(3)曝气池②排放的海水中不含H2SO4的原因是 (用化学方程式表示)。
如图是实验室中常见装置。回答下列问题。
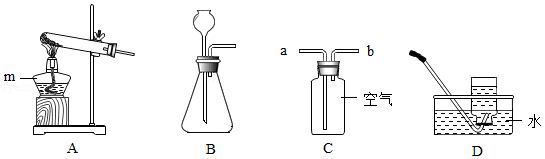
(1)装置A中仪器m的名称是 。
(2)用过氧化氢溶液制取氧气的化学方程式为 ,发生装置是 (填字母序号)。
(3)用装置C收集CO2气体时,气体应从 (填“a”或“b”)端通入。
(4)下列气体中,只能用装置D而不能用装置C收集的是 (填数字序号)。
①H2 ②N2 ③O2
天然溶洞中形态各异的石笋和钟乳石形成的过程中发生了一系列变化,其中一个化学反应是:CaCO 3+X+H 2O═Ca(HCO 3) 2。
(1)X的化学式是 。
(2)已知碳酸氢钙[Ca(HCO 3) 2]易溶于水。向一定量的澄清石灰水中通入二氧化碳,澄清石灰水变浑浊,发生反应的化学方程式是 ,继续通入二氧化碳,又会发现其变澄清,因为 (用文字描述)。
化学是美好生活的创建者。
(1)人类目前使用的燃料大多来自化石燃料,其中比较清洁的是 。
(2)如图所示,活性炭的作用有 (填序号)。
①消毒
②过滤
③吸附
④降低硬度
(3)我国先进的5G通信设备使用了多种材料。聚氯乙烯塑料(PVC)用作天线罩,它属于 材料;高纯硅(Si)用作基带芯片,其制取原理:四氯化硅(SiCl 4)和氢气在高温条件下生成硅和氯化氢,写出该反应的化学方程式: 。

补全实验报告。
装置及操作 |
现象 |
解释或结论 |
|
|
(1)向1中滴加 溶液 |
铁片上附着红色固体,溶液颜色变浅 |
Fe的金属活动性比Cu的强 |
(2)向2中滴加盐酸 |
固体减少,得到黄色溶液 |
化学方程式:
|
|
(3)向3中滴加足量盐酸 |
|
Ca(OH)2能与盐酸反应 |
|
(1)如图1为实验室制取并收集气体的装置图,请回答下列问题。
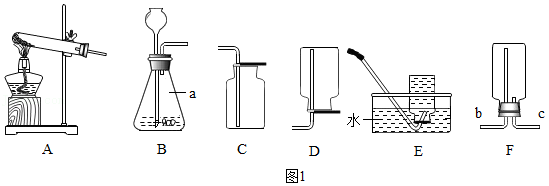
①仪器a的名称是 。
②若用A装置制取氧气,写出对应的化学方程式 。
③若需收集一瓶较纯净的氧气,应选用的装置是 (填装置序号)。
④若用C装置收集一瓶二氧化碳气体,其验满的方法是 。
⑤二氧化硫是一种有刺激性气味的有毒气体,比空气的密度大,易溶于水且与水反应。若用F装置收集二氧化硫气体,则气体应从 (填“b”或“c”)端导入。
(2)电解饱和食盐水可以制得氢氧化钠、氯气(Cl2)和氢气,并进而生产具有消毒、漂白作用的漂白液。
①粗盐中的难溶性杂质可通过溶解、 操作除去,以免破坏电解装置。
②写出电解饱和食盐水的化学方程式 。
③某同学想知道某一瓶放置一段时间的漂白液是否变质,设计了下列探究实验。
【查阅资料】
Ⅰ.制取漂白液(有效成分为NaClO)的原理:Cl2+2NaOH═NaCl+NaClO+H2O;
Ⅱ.在空气中NaClO易发生反应:2NaClO+H2O+CO2═Na2CO3+2HClO,HClO能使有色布条褪色,且HClO含量越高,漂白效果越好;HClO易分解,分解后丧失漂白作用;
Ⅲ.Ca(ClO)2易溶于水。
【提出问题】放置一段时间的漂白液是否变质?
【提出猜想】
猜想1:未变质,溶液中主要成分为NaCl、NaClO
猜想2:部分变质,溶液中主要成分为NaCl、NaClO、Na2CO3
猜想3:全部变质,溶液中主要成分为NaCl、Na2CO3
【实验探究】
实验操作 |
实验现象 |
实验结论 |
ⅰ取适量该溶液于烧杯中,放入有色布条 |
|
猜想3不成立 |
ⅱ另取适量该溶液于试管中,滴入适量氯化钙溶液 |
产生白色沉淀 |
猜想 成立 |
写出实验操作ii中产生白色沉淀的化学方程式 。
【拓展应用】由【查阅资料】和图2可知,需控制pH约为 时(填整数),漂白液具有最佳漂白能力。

金属材料与人类生活息息相关,请回答下列问题。
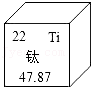
(1)钛元素在元素周期表中的信息如图所示,则钛的相对原子质量是 。
(2)家用台灯通常采用铜质插头,是利用金属铜的 性。
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是 。
(4)将一定质量的Zn片加入AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是 ;若滤液蓝色,则滤液中溶质一定有 。
我国“十四五”规划已经明确“2030年前实现碳达峰”的目标。碳达峰是指二氧化碳的排放达到峰值,不再增长。如图为自然界中CO2的循环图,图中箭头指向表示产生(排放)或消耗CO2的途径。回答下列问题:
(1)途径①需要消耗空气中的 。
(2)途径②中,枯枝败叶中的纤维素[化学式为(C6H10O5)n]在微生物作用下彻底转化为CO2和H2O,该转化中消耗O2与产生的CO2分子个数比为 。
(3)途径④通过光合作用吸收CO2的量白天 夜晚(填“大于”或“小于”)。

(4)途径⑤消耗的化石燃料是 (填“可”或“不可”)再生资源。
(5)降碳的一种途径是在合适的催化剂条件下,将二氧化碳与氢气反应使碳全部转化为乙烯(C2H4)、同时生成另一种化合物。请写出反应的化学方程式 。
(6)某年通过不同途径产生或消耗碳量的相对值如下表所示:
途径 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
相对值 |
0.6 |
60 |
60 |
121.8 |
5.5 |
92 |
90 |
据表可知,这一年大气中碳量增加了 (用表中相对值计算)。为达成“2030年前实现碳达峰”的目标,下列措施不可行的是 。
A.开发新能源
B.植树造林
C.禁止使用化石燃料
进一步分析上表回答:人口增多是否是大气中碳量增加的主要因素,并说明理由 。
2021年3月,四川“三星堆遗址”已出土黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物,其中青铜为合金。
(1)下列物质中属于金属材料的有 (填序号)。
A.象牙
B.黄金
C.丝织品
D.青铜
(2)青铜的硬度比纯铜 (填“大”或“小”)。
(3)铜制品长期暴露在空气中能与空气中的O2、H2O和 化合生成铜锈【主要成分是Cu(OH)2CO3】。
(4)黄铜是铜锌合金,区分黄铜和纯铜发生反应的化学方程式为 。
含有镁的合金广泛应用于航空航天领域,回答下列问题:
(1)取少量光亮的镁条于试管中,向其中加入稀盐酸,观察到 的现象可推断二者发生了化学反应。
(2)若验证镁与稀盐酸反应后的溶液中有盐酸剩余,下列实验设计可行的是 。
A.取生锈的铁钉于试管中,加入反应后的溶液
B.取少量反应后的溶液于试管中,滴加AgNO3溶液
C.取少量反应后的溶液于试管中,滴加稀氢氧化钠溶液
(3)向镁条中加入过量稀盐酸,完全反应后,再加入过量氢氧化钠溶液,生成5.8g氢氧化镁沉淀。
①写出加入氢氧化钠溶液时,生成氢氧化镁沉淀的化学方程式 ;
②计算镁条与稀盐酸完全反应后生成MgCl2的质量为 g。
新型冠状病毒肺炎疫情防控期间,要合理搭配饮食,以保证基本营养素的均衡摄取,增强身体免疫力;要合理使用消毒剂进行杀菌消毒。请回答下列问题:
(1)下列物质富含蛋白质的是 (填写字母标号)。
| A. |
水果、蔬菜 |
| B. |
花生油、奶油 |
| C. |
纯牛奶、蛋清 |
| D. |
米饭、馒头 |
(2)下列物质常用于制作消毒剂,其中属于氧化物的是 (填写字母标号)。
| A. |
过氧乙酸(CH 3COOOH) |
| B. |
二氧化氯(ClO 2) |
| C. |
苯酚(C 6H 6O) |
| D. |
次氯酸钙[Ca(ClO) 2] |
(3)体积分数为75%的酒精常用于手和皮肤消毒。因易燃,使用时要注意远离火源。乙醇燃烧的化学方程式是 。
(4)"84"消毒液的有效成分是次氯酸钠(NaClO),适用于物体表面以及室内环境等方面的消毒。NaClO中氯元素的化合价是 。
下列化学方程式及对应的基本反应类型都正确的是( )
A.CaHCO3═CaCO3↓+CO2↑+H2O 分解反应
B.Al(OH)3+3HCl═AlCl3+3H2O 复分解反应
C.P+O2 P2O5 化合反应
D.Fe2O3+3CO 3CO2+2Fe 置换反应
化学是一门以实验为基础的学科。请结合下列实验装置图回答问题:

(1)写出图中①、②两种仪器的名称:① ,② 。
(2)某同学用高锰酸钾加热制取氧气,反应的化学方程式为 ;应选择的发生装置为 (填字母) ,收集装置为 (填字母)。
(3)A装置与C装置比较,A装置的优点是可以控制反应的发生和停止。请写出一个利用A装置此优点的反应化学方程式 。
(4)实验室可用金属与浓硫酸反应制取SO2气体,金属锌和金属铜都能与浓硫酸反应制SO2气体。欲制取一瓶纯净的SO2气体,最好选择金属 (填“锌”或“铜”),选择理由是 。
壮丽七十年,奋斗新时代。我国科技发展日新月异,在空间科学研究领域取得重大成果。

①2019年1月3日,“嫦娥”四号成功实现人类探测器首次月球背面软着陆,开启了人类月球探测新篇章。“嫦娥”四号探测器由“长征”三号乙改进型运载火箭携带升空,该运载火箭的推进剂中有液氢和液氧。试写出氢气在氧气中燃烧的化学方程式: 。
②我国“墨子号”量子科学实验卫星团队在量子通信实验方面做出了卓越贡献,”墨子号”量子科学实验卫星上的光伏太阳能电池板的基板材料是玻璃纤维,光伏太阳能电池的作用是将 能转化为电能。在玻璃纤维中含有多种成分,其中有Na2SiO3、CaSiO3、SiO2,在上述三种物质中,硅元素表现的化合价均为 价。