金属在生产、生活和社会发展中的应用较为广泛。
(1)铜丝、铝丝常用作导线,是因为它们具有良好的 性。
(2)早在明代宋应星所著的《天工开物》里就对铁器的生产和使用有所记载,到了现代,炼铁技术得到进一步发展。炼铁的原理是利用一氧化碳与氧化铁的反应,请写出该反应的化学方程式 ,该反应 (填“属于”或“不属于”)置换反应。
(3)钢窗表面喷漆不仅美观,而且可有效防止铁与空气中的 接触而生锈。
(4)某同学对含X、Y、铜、银四种金属的混合物进行如图探究,根据实验流程回答下列问题:
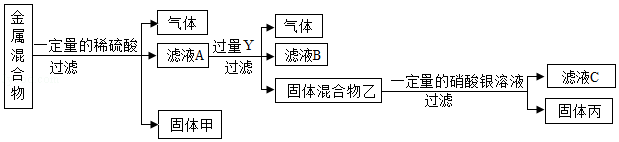
①四种金属的活动性由强到弱的顺序是 ;
②滤液C中所含溶质的成分可能有 种情况。
化学与生产和生活密切相关。请回答下列问题:
(1)俗语道“酒香不怕巷子深”,原因是 (用微粒的观点解释)。
(2)武德合金常用作保险丝,是因为合金的熔点比组成它的纯金属的熔点要 (填“高”或“低”)
(3)“灯影牛肉”是达州的一张美食名片,其牛肉中主要含有的营养物质是 (填字母序号)。
A.糖类 B.蛋白质 C.油脂 D.维生素
(4)华为公司研发了一种以甲醇为原料的新型手机电池,其容量为锂电池的10倍,可连续使用1个月才充一次电,其电池反应原理为:2CH3OH+3X+4NaOH═2Na2CO3+6H2O.其中X的化学式为 。
(5)人们在使用含碳燃料过程要注意通风,如果氧气不足会产生一氧化碳,使人中毒。某液化石油气中含有丙烯,其化学式为C3H6.小王同学取4.2g丙烯和12.8g氧气在一密闭容器中点燃,恰好完全反应,测得生成二氧化碳的质量8.8g,一氧化碳的质量2.8g,那么生成水的质量 g,写出该反应的化学方程式 。
根据要求回答下列问题:
(1)生活中区别硬水与软水常用 ;
(2)电解水的实验中,H2与O2的体积比约为 ;
(3)酒精(C2H5OH)在空气中完全燃烧的化学方程式为 ;
(4)现有Br2+2NaI═I2+2NaBr、Cl2+2NaBr═Br2+2NaCl两个反应,其反应规律和金属与盐溶液的置换反应类似,则Br2、Cl2、I2三种非金属活动性顺序由大到小为 。
我国自主设计的大型客机成功试飞,首艘国产航母正式下水,标志着我国的金属材料制造技术取得重大突破。根据所学知识回答下列问题:
| 金属 |
A |
B |
C |
D |
| 导电性(以100为标准) |
99 |
61 |
17 |
7.9 |
| 密度/(g•cm ﹣ 3) |
8.92 |
2.70 |
7.86 |
11.3 |
| 熔点/℃ |
1083 |
660 |
1535 |
327 |
| 硬度(以10为标准) |
3 |
2.7 |
5 |
1.5 |
(1)常温下一些金属的物理性质数据如表,据此可知高压输电线最好选用金属 (填字母);C的合金通常可以做菜刀、锤子等,其合金的硬度 5(填">"、"<"或"=")。
(2)铁矿石有多种,如赤铁矿(主要成分Fe 2O 3)和磁铁矿(主要成分Fe 3O 4)等,写出磁铁矿的主要成分与一氧化碳反应的化学方程式 。
(3)在Fe(NO 3) 2和AgNO 3的混合溶液中,加入一定量镁粉和锌粉的混合物,充分反应后过滤,得到滤渣和滤液。下列说法中正确的是 (填序号)。
a.若滤液为浅绿色,则滤渣中可能有锌
b.滤液中一定有Mg(NO 3) 2,滤渣中一定有银
c.若取少量滤液,加入KCl溶液,无明显现象,则滤渣中一定有铁
d.若取少量滤渣,加入稀盐酸,产生气泡,则滤渣的组成有三种情况
复学防疫,化学助力。
(1)起床后,测体温。测体温时水银体温计中汞柱会上升的微观原因是汞原子 。
(2)上学时,戴口罩。制作口罩用的无纺布面料主要是聚丙烯[(C3H6)n],聚丙烯中碳、氢元素的质量比为 。
(3)到校后,勤消毒。过氧乙酸用于教室消毒,其化学性质不稳定,分解的化学方程式为:2C2H4O3═2C2H4O2+X↑,则X的化学式为 。用于手部消毒的酒精溶液属于易燃物,使用时要注意安全,酒精燃烧的化学方程式为 。
(4)用餐时,讲营养。如午餐仅食用米饭、红烧肉、鸡蛋汤、牛奶,从均衡营养角度出发还应补充的一种食物是 。
从玫瑰花瓣中提取的花青素(紫色)可制成酸碱指示剂,滴入到不同溶液中颜色变化如下表,结合表中信息回答:
| 试剂 |
NaCl溶液 |
盐酸 |
NaHCO 3溶液 |
NH 4Cl溶液 |
NaOH溶液 |
| 颜色 |
紫 |
红 |
蓝 |
红 |
蓝 |
(1)NH 4Cl溶液呈 (填"酸性""碱性"或"中性"),用作化肥长期施用的结果是 。
(2)向某无色溶液中滴入花青素,溶液变蓝色,则此溶液中一定不存在  离子中的 (填离子符号)。
离子中的 (填离子符号)。
(3)胃溃疡患者不用碳酸氢钠片治疗胃酸过多的原因是 (用化学方程式表示)。
铝、铜、铁是生活中常见的金属。
(1)铝在空气中具有良好的抗腐蚀性的原因是 ;
(2)用铜制品电线主要是利用铜具有良好的 性;
(3)焊接铁制品时,通常先用稀盐酸除去铁表面的锈,反应的化学方程式为 。
(1)如图1为实验室制取并收集气体的装置图,请回答下列问题。
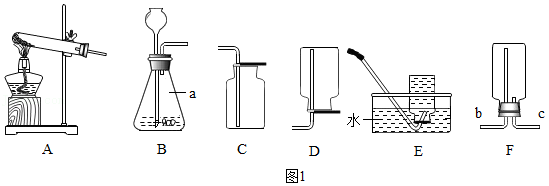
①仪器a的名称是 。
②若用A装置制取氧气,写出对应的化学方程式 。
③若需收集一瓶较纯净的氧气,应选用的装置是 (填装置序号)。
④若用C装置收集一瓶二氧化碳气体,其验满的方法是 。
⑤二氧化硫是一种有刺激性气味的有毒气体,比空气的密度大,易溶于水且与水反应。若用F装置收集二氧化硫气体,则气体应从 (填“b”或“c”)端导入。
(2)电解饱和食盐水可以制得氢氧化钠、氯气(Cl2)和氢气,并进而生产具有消毒、漂白作用的漂白液。
①粗盐中的难溶性杂质可通过溶解、 操作除去,以免破坏电解装置。
②写出电解饱和食盐水的化学方程式 。
③某同学想知道某一瓶放置一段时间的漂白液是否变质,设计了下列探究实验。
【查阅资料】
Ⅰ.制取漂白液(有效成分为NaClO)的原理:Cl2+2NaOH═NaCl+NaClO+H2O;
Ⅱ.在空气中NaClO易发生反应:2NaClO+H2O+CO2═Na2CO3+2HClO,HClO能使有色布条褪色,且HClO含量越高,漂白效果越好;HClO易分解,分解后丧失漂白作用;
Ⅲ.Ca(ClO)2易溶于水。
【提出问题】放置一段时间的漂白液是否变质?
【提出猜想】
猜想1:未变质,溶液中主要成分为NaCl、NaClO
猜想2:部分变质,溶液中主要成分为NaCl、NaClO、Na2CO3
猜想3:全部变质,溶液中主要成分为NaCl、Na2CO3
【实验探究】
实验操作 |
实验现象 |
实验结论 |
ⅰ取适量该溶液于烧杯中,放入有色布条 |
|
猜想3不成立 |
ⅱ另取适量该溶液于试管中,滴入适量氯化钙溶液 |
产生白色沉淀 |
猜想 成立 |
写出实验操作ii中产生白色沉淀的化学方程式 。
【拓展应用】由【查阅资料】和图2可知,需控制pH约为 时(填整数),漂白液具有最佳漂白能力。

金属材料与人类生活息息相关,请回答下列问题。
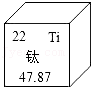
(1)钛元素在元素周期表中的信息如图所示,则钛的相对原子质量是 。
(2)家用台灯通常采用铜质插头,是利用金属铜的 性。
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是 。
(4)将一定质量的Zn片加入AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是 ;若滤液蓝色,则滤液中溶质一定有 。
我国“十四五”规划已经明确“2030年前实现碳达峰”的目标。碳达峰是指二氧化碳的排放达到峰值,不再增长。如图为自然界中CO2的循环图,图中箭头指向表示产生(排放)或消耗CO2的途径。回答下列问题:
(1)途径①需要消耗空气中的 。
(2)途径②中,枯枝败叶中的纤维素[化学式为(C6H10O5)n]在微生物作用下彻底转化为CO2和H2O,该转化中消耗O2与产生的CO2分子个数比为 。
(3)途径④通过光合作用吸收CO2的量白天 夜晚(填“大于”或“小于”)。

(4)途径⑤消耗的化石燃料是 (填“可”或“不可”)再生资源。
(5)降碳的一种途径是在合适的催化剂条件下,将二氧化碳与氢气反应使碳全部转化为乙烯(C2H4)、同时生成另一种化合物。请写出反应的化学方程式 。
(6)某年通过不同途径产生或消耗碳量的相对值如下表所示:
途径 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
相对值 |
0.6 |
60 |
60 |
121.8 |
5.5 |
92 |
90 |
据表可知,这一年大气中碳量增加了 (用表中相对值计算)。为达成“2030年前实现碳达峰”的目标,下列措施不可行的是 。
A.开发新能源
B.植树造林
C.禁止使用化石燃料
进一步分析上表回答:人口增多是否是大气中碳量增加的主要因素,并说明理由 。
2021年3月,四川“三星堆遗址”已出土黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物,其中青铜为合金。
(1)下列物质中属于金属材料的有 (填序号)。
A.象牙
B.黄金
C.丝织品
D.青铜
(2)青铜的硬度比纯铜 (填“大”或“小”)。
(3)铜制品长期暴露在空气中能与空气中的O2、H2O和 化合生成铜锈【主要成分是Cu(OH)2CO3】。
(4)黄铜是铜锌合金,区分黄铜和纯铜发生反应的化学方程式为 。
含有镁的合金广泛应用于航空航天领域,回答下列问题:
(1)取少量光亮的镁条于试管中,向其中加入稀盐酸,观察到 的现象可推断二者发生了化学反应。
(2)若验证镁与稀盐酸反应后的溶液中有盐酸剩余,下列实验设计可行的是 。
A.取生锈的铁钉于试管中,加入反应后的溶液
B.取少量反应后的溶液于试管中,滴加AgNO3溶液
C.取少量反应后的溶液于试管中,滴加稀氢氧化钠溶液
(3)向镁条中加入过量稀盐酸,完全反应后,再加入过量氢氧化钠溶液,生成5.8g氢氧化镁沉淀。
①写出加入氢氧化钠溶液时,生成氢氧化镁沉淀的化学方程式 ;
②计算镁条与稀盐酸完全反应后生成MgCl2的质量为 g。
新型冠状病毒肺炎疫情防控期间,要合理搭配饮食,以保证基本营养素的均衡摄取,增强身体免疫力;要合理使用消毒剂进行杀菌消毒。请回答下列问题:
(1)下列物质富含蛋白质的是 (填写字母标号)。
| A. |
水果、蔬菜 |
| B. |
花生油、奶油 |
| C. |
纯牛奶、蛋清 |
| D. |
米饭、馒头 |
(2)下列物质常用于制作消毒剂,其中属于氧化物的是 (填写字母标号)。
| A. |
过氧乙酸(CH 3COOOH) |
| B. |
二氧化氯(ClO 2) |
| C. |
苯酚(C 6H 6O) |
| D. |
次氯酸钙[Ca(ClO) 2] |
(3)体积分数为75%的酒精常用于手和皮肤消毒。因易燃,使用时要注意远离火源。乙醇燃烧的化学方程式是 。
(4)"84"消毒液的有效成分是次氯酸钠(NaClO),适用于物体表面以及室内环境等方面的消毒。NaClO中氯元素的化合价是 。
下列化学方程式及对应的基本反应类型都正确的是( )
A.CaHCO3═CaCO3↓+CO2↑+H2O 分解反应
B.Al(OH)3+3HCl═AlCl3+3H2O 复分解反应
C.P+O2 P2O5 化合反应
D.Fe2O3+3CO 3CO2+2Fe 置换反应
化学是一门以实验为基础的学科。请结合下列实验装置图回答问题:

(1)写出图中①、②两种仪器的名称:① ,② 。
(2)某同学用高锰酸钾加热制取氧气,反应的化学方程式为 ;应选择的发生装置为 (填字母) ,收集装置为 (填字母)。
(3)A装置与C装置比较,A装置的优点是可以控制反应的发生和停止。请写出一个利用A装置此优点的反应化学方程式 。
(4)实验室可用金属与浓硫酸反应制取SO2气体,金属锌和金属铜都能与浓硫酸反应制SO2气体。欲制取一瓶纯净的SO2气体,最好选择金属 (填“锌”或“铜”),选择理由是 。