实验室可利用Zn与稀硫酸的反应制取H2。
(1)用浓硫酸配制稀硫酸的操作为 (填字母),用玻璃棒引流,并不断搅拌。
A.将浓硫酸缓缓注入盛有水的烧杯中
B.将水缓缓注入盛有浓硫酸的烧杯中
(2)Zn与稀硫酸反应的化学方程式为 。
(3)图1所示的仪器B、D的名称为 、 ,组装制取H2的发生装置应选用的仪器为 (填字母)。
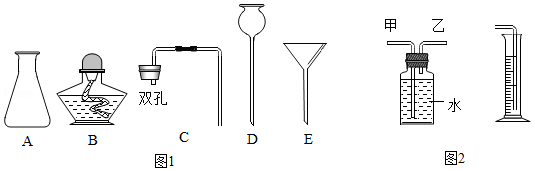
(4)为收集并准确测量H2的体积,在装入药品前,需检查装置的 。
(5)相同条件下H2密度比空气小,利用该性质可以通过 法收集H2,若用图2所示装置测量生成H2的体积,H2应从 (填“甲”或“乙”)管通入。
(6)为探究影响Zn与稀硫酸反应快慢的因素,进行以下三组实验,室温下,取颗粒大小相同的锌粒与足量的稀硫酸反应,测量产生10mL H2(通常状况)所需的时间,下表为实验数据:
实验编号 |
硫酸的质量分数/% |
硫酸的体积/mL |
锌粒的质量/g |
时间/s |
1 |
10 |
10 |
1 |
78 |
2 |
10 |
10 |
2 |
57 |
3 |
40 |
10 |
1 |
9 |
①比较实验1、2的数据,可以得出的结论是 。
②由实验数据可知,该实验中对Zn与稀硫酸反应快慢影响较大的因素是 。
③比较不同条件下锌粒与稀硫酸反应的快慢有不同的方法,除测量产生相同体积的H2所需的时间,还可采用的测量方法是 (写出一种)。
(1)如图1中A、B、C、D是四种粒子的结构示意图。
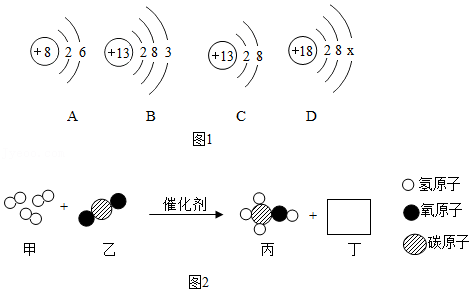
①C粒子的符号为 。
②图A、B、C、D共表示 种元素,由A、C两种元素组成的化合物的化学式为 。
③D中x= 。
(2)二氧化碳会引起温室效应。某纳米纤维化剂可将二氧化碳转化为液体燃料甲醇(CH3OH),其微观示意图如图2(图中的微粒恰好完全反应)。
①该反应中涉及到的单质的化学式为 。
②写出该化学反应方程式: 。
扬州既是世界美食之都,更是一座拥有两千多年历史的文化旅游名城。
(1)扬州早点是一张靓丽的城市名片。

①扬州包子面皮如雪。面皮的主要成分为淀粉,淀粉属于 (填字母)。
A.糖类
B.油脂
C.蛋白质
②大煮干丝富含蛋白质。蛋白质在人体内转化为能被吸收的小分子化合物,这类化合物称为 。
③翡翠烧卖色泽翠润,所用天然色素来自新鲜绿色蔬菜。获取天然色素时,将菜渣与菜汁分离开可采用 的方法。
(2)青砖黛瓦诉说着扬州的历史。

①《天工开物》中介绍了烧制青砖的方法,其中载有“灌水其上”“水火既济”。相关反应为水蒸气与灼热的碳生成CO和一种气体单质,其化学方程式为 。
②古代建筑工匠常用糯米灰浆粘合墙砖,糯米灰浆由糯米汁、熟石灰和砂土等混合制成。糯米灰浆属于 (填“复合材料”或“金属材料”)。熟石灰的化学式为 ,在空气中熟石灰最终转化为 (填化学式)。
③“帘外芭蕉惹骤雨,门环惹铜绿。”铜绿是铜发生一系列复杂反应的产物,空气中参与该反应过程的物质有 (填化学式)。
下列化学方程式书写正确的是( )
A.硫在氧气中燃烧:2S+3O2 2SO3
B.CO2使澄清石灰水变浑浊:CO2+CaOH═CaHCO3↓
C.Ba(OH)2溶液与Na2SO4溶液混合:Ba(OH)2+Na2SO4═BaSO4↓+NaOH
D.一氧化碳从氧化铁中还原出铁:Fe2O3+3CO 2Fe+3CO2
氢气被看作是理想的能源。氢气的制取和储存是氢能源利用领域的研究热点。
Ⅰ.氢气的制取
(1)科学家正致力于研究在催化剂和光照条件下分解水制氢气。写出该反应的化学方程式: ,该反应 (填“放出”或“吸收”)能量。
(2)水热分解可得氢气,高温下水分解体系中微粒含量与温度的关系如图所示。
图中曲线A、B对应的微粒依次是 (填符号)。
Ⅱ.氢气的储存
(3)一种镁铜合金可用于储氢。
①将镁、铜单质按比例在一定温度下熔炼得到上述合金。熔炼时须通入氩气,其目的是 。
②350℃时,该镁铜合金与氢气反应,生成了一种仅含Mg、H两种元素的化合物,其中氢元素的质量分数为7.7%.该化合物的化学式为 。
下列化学方程式与客观事实相符,且书写完全正确的是( )
A.用过氧化氢溶液制氧气:H2O2 H2↑+O2↑
H2↑+O2↑
B.铁丝在氧气中燃烧:4Fe+3O2 2Fe2O3
2Fe2O3
C.用稀硫酸除铁锈:Fe2O3+H2SO4═FeSO4+H2O
D.用澄清石灰水检验二氧化碳:CO2+Ca(OH)2═CaCO3↓+H2O
铝是大自然赐予人类的宝物,是现代文明不可缺少的物质基础。
(1)人类冶炼和使用金属铝的时间较晚,可能是因为 (填字母)。
a.地壳中铝元素含量少
b.冶炼铝的技术要求高
(2)用铝锂合金制造“神舟号”航天飞船的一些部件,主要是利用其强度高、耐腐蚀和 (写一条)等性质。高温下,铝与Li2O反应可置换出金属锂,写出该反应的化学方程式: 。
(3)用砂纸去除铝片表面的氧化膜。将其浸入硫酸铜溶液中,一段时间后,观察到铝片表面有红色物质析出,并有气泡产生,经检验气体为氢气。
①写出生成红色物质的化学方程式: 。
②硫酸铜溶液中的阳离子有 (填离子符号)。
(4)原子簇是若干个原子的聚集体,有望开发成新材料。某铝原子簇由13个铝原子构成,其最外层电子数的总和为40时相对稳定。写出该稳定铝原子簇的微粒符号: 。
[铝原子的结构示意图为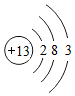 ]
]
化学与生产、生活密切相关。回答下列问题:
(1)宜宾芽菜因风味独特深受消费者喜爱。某品牌芽菜是由青菜、食用盐、食糖、食品添加剂等混合腌制而成,其营养成分如下表:
营养成分表
项目 |
每100克 |
能量 蛋白质 脂肪 碳水化合物 钠 |
925千焦 18克 0克 524克 1860毫克 |
①营养成分表中的“钠”是指 (选填“原子”、“分子”或“元素”),主要来源于 。
②从营养成分表可知,提供能量的主要物质是 。
③该品牌芽菜的外包装袋是由聚丙烯制成,聚丙烯属于 (填字母序号)。
A.天然高分子材料
B.有机合成材料
C.金属材料
(2)从源头上减少和消除污染是“绿色化学”的重要理念。工业燃煤会产生大气污染物SO2,为减少SO2的排放,煤燃烧时加入生石灰进行“固硫”。
①化石燃料包括煤、 和天然气。
②SO2造成的环境污染问题主要是 。
③煤燃烧时需不断鼓入空气,“固硫”最终生成CaSO4.“固硫”的化学方程式是 。

(1)如图1为实验室制取并收集气体的装置图,请回答下列问题。
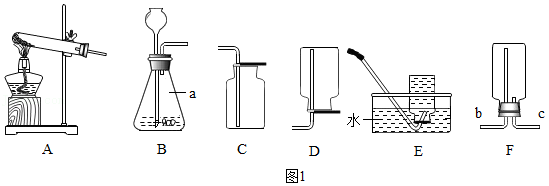
①仪器a的名称是 。
②若用A装置制取氧气,写出对应的化学方程式 。
③若需收集一瓶较纯净的氧气,应选用的装置是 (填装置序号)。
④若用C装置收集一瓶二氧化碳气体,其验满的方法是 。
⑤二氧化硫是一种有刺激性气味的有毒气体,比空气的密度大,易溶于水且与水反应。若用F装置收集二氧化硫气体,则气体应从 (填“b”或“c”)端导入。
(2)电解饱和食盐水可以制得氢氧化钠、氯气(Cl2)和氢气,并进而生产具有消毒、漂白作用的漂白液。
①粗盐中的难溶性杂质可通过溶解、 操作除去,以免破坏电解装置。
②写出电解饱和食盐水的化学方程式 。
③某同学想知道某一瓶放置一段时间的漂白液是否变质,设计了下列探究实验。
【查阅资料】
Ⅰ.制取漂白液(有效成分为NaClO)的原理:Cl2+2NaOH═NaCl+NaClO+H2O;
Ⅱ.在空气中NaClO易发生反应:2NaClO+H2O+CO2═Na2CO3+2HClO,HClO能使有色布条褪色,且HClO含量越高,漂白效果越好;HClO易分解,分解后丧失漂白作用;
Ⅲ.Ca(ClO)2易溶于水。
【提出问题】放置一段时间的漂白液是否变质?
【提出猜想】
猜想1:未变质,溶液中主要成分为NaCl、NaClO
猜想2:部分变质,溶液中主要成分为NaCl、NaClO、Na2CO3
猜想3:全部变质,溶液中主要成分为NaCl、Na2CO3
【实验探究】
实验操作 |
实验现象 |
实验结论 |
ⅰ取适量该溶液于烧杯中,放入有色布条 |
|
猜想3不成立 |
ⅱ另取适量该溶液于试管中,滴入适量氯化钙溶液 |
产生白色沉淀 |
猜想 成立 |
写出实验操作ii中产生白色沉淀的化学方程式 。
【拓展应用】由【查阅资料】和图2可知,需控制pH约为 时(填整数),漂白液具有最佳漂白能力。

金属材料与人类生活息息相关,请回答下列问题。
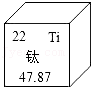
(1)钛元素在元素周期表中的信息如图所示,则钛的相对原子质量是 。
(2)家用台灯通常采用铜质插头,是利用金属铜的 性。
(3)我国是最早采用湿法炼铜的国家,铁与硫酸铜溶液反应的化学方程式是 。
(4)将一定质量的Zn片加入AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和滤液,则滤渣中一定含有的金属是 ;若滤液蓝色,则滤液中溶质一定有 。
我国“十四五”规划已经明确“2030年前实现碳达峰”的目标。碳达峰是指二氧化碳的排放达到峰值,不再增长。如图为自然界中CO2的循环图,图中箭头指向表示产生(排放)或消耗CO2的途径。回答下列问题:
(1)途径①需要消耗空气中的 。
(2)途径②中,枯枝败叶中的纤维素[化学式为(C6H10O5)n]在微生物作用下彻底转化为CO2和H2O,该转化中消耗O2与产生的CO2分子个数比为 。
(3)途径④通过光合作用吸收CO2的量白天 夜晚(填“大于”或“小于”)。

(4)途径⑤消耗的化石燃料是 (填“可”或“不可”)再生资源。
(5)降碳的一种途径是在合适的催化剂条件下,将二氧化碳与氢气反应使碳全部转化为乙烯(C2H4)、同时生成另一种化合物。请写出反应的化学方程式 。
(6)某年通过不同途径产生或消耗碳量的相对值如下表所示:
途径 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
相对值 |
0.6 |
60 |
60 |
121.8 |
5.5 |
92 |
90 |
据表可知,这一年大气中碳量增加了 (用表中相对值计算)。为达成“2030年前实现碳达峰”的目标,下列措施不可行的是 。
A.开发新能源
B.植树造林
C.禁止使用化石燃料
进一步分析上表回答:人口增多是否是大气中碳量增加的主要因素,并说明理由 。
2021年3月,四川“三星堆遗址”已出土黄金面具、青铜艺术品、象牙、残存的丝织品等重要文物,其中青铜为合金。
(1)下列物质中属于金属材料的有 (填序号)。
A.象牙
B.黄金
C.丝织品
D.青铜
(2)青铜的硬度比纯铜 (填“大”或“小”)。
(3)铜制品长期暴露在空气中能与空气中的O2、H2O和 化合生成铜锈【主要成分是Cu(OH)2CO3】。
(4)黄铜是铜锌合金,区分黄铜和纯铜发生反应的化学方程式为 。
含有镁的合金广泛应用于航空航天领域,回答下列问题:
(1)取少量光亮的镁条于试管中,向其中加入稀盐酸,观察到 的现象可推断二者发生了化学反应。
(2)若验证镁与稀盐酸反应后的溶液中有盐酸剩余,下列实验设计可行的是 。
A.取生锈的铁钉于试管中,加入反应后的溶液
B.取少量反应后的溶液于试管中,滴加AgNO3溶液
C.取少量反应后的溶液于试管中,滴加稀氢氧化钠溶液
(3)向镁条中加入过量稀盐酸,完全反应后,再加入过量氢氧化钠溶液,生成5.8g氢氧化镁沉淀。
①写出加入氢氧化钠溶液时,生成氢氧化镁沉淀的化学方程式 ;
②计算镁条与稀盐酸完全反应后生成MgCl2的质量为 g。
新型冠状病毒肺炎疫情防控期间,要合理搭配饮食,以保证基本营养素的均衡摄取,增强身体免疫力;要合理使用消毒剂进行杀菌消毒。请回答下列问题:
(1)下列物质富含蛋白质的是 (填写字母标号)。
| A. |
水果、蔬菜 |
| B. |
花生油、奶油 |
| C. |
纯牛奶、蛋清 |
| D. |
米饭、馒头 |
(2)下列物质常用于制作消毒剂,其中属于氧化物的是 (填写字母标号)。
| A. |
过氧乙酸(CH 3COOOH) |
| B. |
二氧化氯(ClO 2) |
| C. |
苯酚(C 6H 6O) |
| D. |
次氯酸钙[Ca(ClO) 2] |
(3)体积分数为75%的酒精常用于手和皮肤消毒。因易燃,使用时要注意远离火源。乙醇燃烧的化学方程式是 。
(4)"84"消毒液的有效成分是次氯酸钠(NaClO),适用于物体表面以及室内环境等方面的消毒。NaClO中氯元素的化合价是 。