、
、
、
是初中化学常见的物质,在一定条件下四种物质存在如下图所示的转化关系:
。
(1)若
是硫酸,
是氢氧化钠,该反应的基本类型是反应。
(2)若
、
均是含同种元素的非金属氧化物,且
有毒性,
能被磁铁吸引。
①
的化学式是,其固体俗称;
②
的合金可用于制作炊具,主要是利用它的性。
(3)若
、
是都是金属单质,
、
都是盐,请写出一个符合要求的化学方程式:,该反应说明金属活动性:
(填"<"或">")
。
利用下图装置进行实验。实验前
、
、
均已关闭。
| 内容 装置 |
【实验1】制备气体 |
【实验2】测定气体含量 |
 |
Ⅰ.打开
,用注射器向盛有锌粒的A中注入稀硫酸,直至液面浸没下端导管口 Ⅱ.在 上方导管口收集气体 |
Ⅰ.A(容积
)中为用排空气法收集的
,B中装满水。用注射器向A中注入15mL
溶液(足量),充分反应 Ⅱ.打开 和 |
(1)检查装置气密性:保持
关闭,打开
、
,向B中加水至液面浸没下端导管口,用手捂住A瓶外壁,说明装置在左侧气密性良好的现象是;用同样原理可以检查装置另一侧的气密性。
(2)实验1中,锌与稀硫酸反应的化学方程式为;气体收集完毕后,在不拆卸装置的情况下,使A中未反应的稀硫酸大部分转移到B中的操作是。
(3)实验2中,当B中液面不再变化时,测得B中减少了160mL水,则A中
的体积分数约为 %。
某学校组织学生到郊外野炊。
(1)有些同学带了如下的食品,其中主要为人体提供蛋白质的是;主要为人体提供糖类的是(填字母)。
A、鸡蛋 B、水 C、花生油 D、面包
(2)在野炊活动中用到的水来自一个大型水库,你认为水库的水属于(填"纯净物"或"混合物"),小明同学认为该水库的水是硬水,你认为可以用来鉴别。若要测定该水库的水的酸碱度,可以选择.
A、紫色石蕊试液 B、无色酚酞试液 C、pH试纸
(3)在野炊活动过程中,小花不小心被黄蜂蛰了(黄蜂毒液呈碱性),下列物品可以用于涂抹以减轻疼痛的是(填字母)
A、食醋 B、食盐水 C、肥皂水 D、洗洁精
未经处理的工业废水会严重污染水和土壤,某种新型催化剂可有效降解工业废水中的有机污染物。为探究该催化剂降解有机污染物的速度受哪些因素影响,学习小组进行了如下实验。
取四份等质量的某有机物,控制条件如左下图,然后加入等量的新型催化剂,测得该有机物被降解的百分比随时间变化的关系如下表:

| 时间(分) 有机物被降解百分比(%) 组别 |
0 |
5 |
10 |
15 |
|
|
0 |
10 |
40 |
60 |
|
|
0 |
40 |
80 |
100 |
|
|
0 |
30 |
60 |
90 |
|
|
0 |
0 |
0 |
0 |
(1)实验中设置
和
组的目的是探究对降解反应速度的影响。
(2)实验
三组结果表明,当
相等时,温度升高,降解反应速度。(选填"先增大后减小"或"先减小后增大")
(3)部分同学认为
时,40
是该催化剂最合适的温度,但有同学并不认同。为寻找该催化剂最合适的温度,他应该采取的做法是。
(4)实验中若要测定某一时刻有机物被降解的百分比,需要迅速把试管中液体的
调到10,这样做的目的是。
硫酸厂的废水中因含硫酸而显酸性,需要处理呈中性后才能排放。某兴趣小组的同学取少量废水按下列步骤进行实验。
第一步:验证废水酸性。往废水中滴加石蕊试液,石蕊变,说明废水呈酸性。
第二步:处理废水。该小组同学设计了以下两个方案。
方案一:用熟石灰处理废水,其反应的化学方程式为。
方案二:用
处理废水,观察到废水中出现。
经过分析,同学们认为方案二没有达到处理废水的目的,因为处理后的废水中含有较多的。
如图为酸碱的化学性质知识网络,
、
、
、
是四种常见的不同类别的无机化合物,图中短线表示两种物质在一定条件下可以发生化学反应。请你据图回答。

(1)
、
、
三种物质中,能用来鉴别稀硫酸与氢氧化钙溶液的物质是。
(2)能同时实现反应①和②的物质可以是,反应①的实验现象为。
有 、 、 三种气体,能让燃着的木条燃烧更旺的是。小柯将二氧化碳气体通入滴有紫色石蕊试液的水中,他可能要探究的问题是,所得溶液的 7(选填"<"、"="或">")
把铜丝放在酒精灯上加热使其表面变黑,这黑色物质是______,将其插入盛有稀硫酸的试管里,溶液变成 __________色,化学方程式为__ ;
用质量分数为5%的稀盐酸和10%的氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如下图所示:
(1)该实验是将________________(选填“稀盐酸”或“氢氧化钠溶液”)滴加到另一种溶液中。
(2)当加入溶液的质量为bg时,溶液中的溶质是________________________。
(3)当加入溶液的质量a为40 g时,求所得溶液中溶质的质量。
金属元素与人类关系密切.
(1)高钙豆奶粉中的“钙”指的是__________(填“元素”“原子”或“分子”)
(2)地壳中含量最高的金属元素是________(填符号,下同),海水中含量最高的金属离子是_____.
(3)铝可制成蒸锅,主要利用铝的延展性和________性.
(4)药品“氢氧化铝[Al(OH)3]”片剂能与胃酸(主要成分为盐酸)发生中和反应,治疗胃酸过多症,该反应的化学方程式为____________________________________________.
(5)人类向大自然提取量最大的金属是铁。写出高温下一氧化碳把铁从赤铁矿石中还原出来的化学方程式:________________________________________
稀硫酸与氢氧化钠溶液混合没有明显现象,为证明硫酸与氢氧化钠发生了化学反应,小颖同学进行了如下探究:
(1)小颖同学通过图一所示的实验,证明硫酸与氢氧化钠发生了化学反应,她依据的实验现象是 。
(2)氢氧化钠是实验室常用药品,下列有关说法中,正确的是 (填序号)。
| A.称量:可将NaOH固体直接放在天平左边托盘的纸上进行称量 |
| B.溶解:NaOH固体溶于水时放出大量热,溶解时需用玻璃棒不断搅拌 |
| C.应急:先用大量水冲洗皮肤上的NaOH溶液,再涂上3%~5%稀盐酸溶液 |
| D.保存:NaOH固体易吸收空气中的水蒸气和C02,应密封保存 |
(3)溶液的pH变化与所加入稀硫酸的质量关系如图二所示,图中A点对应溶液中的溶质有________(写化学式)。
(4)根据匿示信息,当溶液恰好为中性时,求所得不饱和溶液中溶质的质量。 (不计滴加的酚酞试液质量,计算精确到0.0lg)
(7分)为探究CO2和NaOH确实发生了化学反应,某实验小组的同学设计出了下列2种实验装置,请回答下列问题:
(1)A、B两个实验装置,可能看到实验现象分别是 、 ,产生该实验现象发生反应的化学方程式为 。产生该实验现象的原因是 。
(2)某同学质疑上述实验设计,该同学质疑的依据是 。
(3)在原实验的基础上,你能证明CO2和NaOH肯定发生了化学反应的实验是 。
将氧气通过灼热的铜网,红色固体会变成黑色,该反应的化学方程式为 。欲将黑色固体变回红色,可以通过某个置换反应实现,请写出化学方程式 。将上述黑色固体放入稀硫酸中溶液会变成蓝色,该反应的化学方程式为 ,该反应的基本类型是 。
2015年苏州市初中化学实验操作考查内容为"溶液酸碱性的检验"。请根据实验回答下列问题。
(1)测得碳酸饮料的pH7(填"〈"或"="或"〉")。
(2)下列使用pH试纸的方法中,正确的是(填序号)。
| A. | 将pH试纸剪成几段使用 |
| B. | 将pH试纸直接插入待测液中 |
| C. | 将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上 |
| D. | 将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上 |
E.读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照
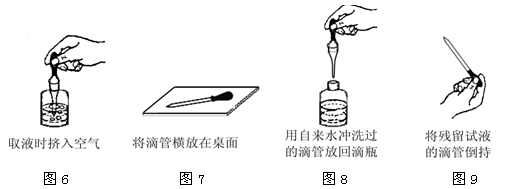
(3)本次实验中滴管使用出现了如图6~图9所示的四种常见错误操作。请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法。
(4)使用白色点滴板完成实验有显色明显、便于对比、(填一项)等优点。
(7分)中和反应是中学化学中重要的学习内容,其在日常生活和工农业生产中有广泛的应用。
(1)下图表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH的变化曲线。请从曲线图中获取信息,回答下列问题:
①图1图象表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化。进行该反应的实验操作是按照图2中的 (填甲或乙)图所示进行。
②曲线上M点表示 。
③向烧杯中倾倒20g质量分数为4.00%的氢氧化钠溶液,滴入3滴酚酞试液,振荡,再逐滴滴入质量分数为3.65%的稀盐酸,边滴边振荡,直至溶液刚好变为色为止,共用去稀盐酸20g,则反应后溶液中溶质质量分数为 (结果精确到0.1%)。
(2)为证明中和反应是放热反应,某小组进行了如图所示的实验操作:
根据上图实验,甲同学认为:NaOH与稀盐酸发生的中和反应是放热反应。乙同学认为:甲同学得出这个结论的依据不科学,理由是 。
(3)为探究影响中和反应放出热量多少的因素,他们又进行了如下实验:在编号为A、B、C、
D、E的五只烧杯中各装入36.5g溶质质量分数为5%、10%、15%、20%、25%的盐酸,再向上述五只烧杯中分别加入40g 20%的氢氧化钠溶液,最后测量其温度,数据记录如下:
实验结论:影响中和反应放出热量多少的因素 。
交流反思:反应后,烧杯内溶液pH最小的是 (填烧杯编号)。