下列物质能在pH=12的无色溶液中大量共存的是
| A.KNO3﹑FeCl3、NaCl | B.HCl、AgNO3、K2SO4 |
| C.BaCl2﹑NH4Cl﹑ZnCl2 | D.NaNO3、Ba(OH)2、NaOH |
镧( )是一种活动性比锌更强的元素,它的氧化物的化学式为 , 是不溶于水的碱,而 、 都可溶于水。由此判断下列几组物质,不能直接反应制取 的是
| A. | 和 | B. | 和 |
| C. | 和 | D. | 和 |
下列叙述与对应的示意图表示正确的是()
| A水的电解 |
B. 向稀硫酸中滴加过量的氢氧化钠溶液 |
 |
B. |
| C.加热一定质量的氯酸钾制取气体 |
D.等质量的锌、铁与足量等浓度的稀硫酸反应 |
 |
 |
某实验小组对实验室制取氢气的反应原理进行探究。
【知识回顾】能产生氢气的化学反应有: ①水电解 ②活泼金属与酸反应
【讨论交流】反应①的化学方程式;同学们讨论后认为该反应不适用于实验室制取氢气。
【实验探究】为了探究哪种物质更适合用于实验室制取氢气,大家设计了如下实验:
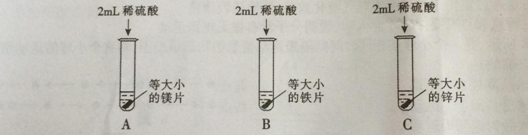
【分析与结论】填写实验报告。
| 实验 |
实验现象 |
实验结论 |
| A |
剧烈反应,迅速产生大量气泡,试管外壁 | 反应速率过快,气体不便收集,不能用于实验室制取氢气 |
| B |
缓慢产生少量气泡 |
反应速率过慢,不能用于实验室制取氢气 |
| C |
较快产生大量气泡,试管外壁发热 |
通过实验得出,适合实验室制取氢气的化学反应方程式为;
【知识拓展】(1)确定实验室制取气体的反应原理时,要考虑诸多因素,如反应的快慢、收集的难易、等。
(2)用稀盐酸制取氢气时,制得的气体中可能会增加的杂质为。
下列整理归纳得出的规律合理的是
| A. | 溶液中的溶剂一定是水 | B. | 同种物质分子间的间隔,气体一定比液体大 |
| C. | 酸、碱中一定含有氧元素 | D. | 不能使酚酞试液变红的溶液一定是酸溶液 |
下列图像与对应的表述不吻合的是( )
| A. |
向氢氧化钠溶液中不断加水

|
| B. |
氯酸钾和二氧化锰混合加热制取氧气

|
| C. |
向硫酸和硫酸铜的混合溶液中滴加氢氧化钠溶液

|
| D. |
某温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体

|
化学变化中,同种元素可在不同物质中"旅行"。(注:"--→"表示某种物质通过一步反应可转化为另一种物质)回答下列问题:
(1)按甲、乙物质所含元素种类递增的规律,完成图所示的"旅行"。
①若图为碳元素的"旅行"路线,其中甲为二氧化碳,乙为碳酸钙,
写出路线Ⅱ反应的化学方程式:(写一个),该反应属于(填基本反应类型)。

②若上图为氢元素的"旅行"路线,写出其中一个反应的化学方程式:。
(2)从单质、碱、盐中分别选择一种物质,完成下图所示的"旅行"。写出一组甲、乙、丙物质的化学式。

甲,乙,丙。
下列说法正确的是()
| A. | 用活性炭可以降低水的硬度 |
| B. | 可用 试纸测定溶液的酸碱度 |
| C. | 赤铁矿的主要成分氧化铁的化学式是 |
| D. | 用 制取 时,加入 可以增加生成 的质量 |
物质x可发生下列所示的两个反应,则X可能是()
①X+碱→盐+水 ②X+金属氧化物→盐+水.
| A. | B. | C. | D. |
下列实验设计不能达到实验目的的是()
| A. | 用燃着的木条区分氧气和二氧化碳 |
| B. | 用盐酸验证敞口放置的 溶液已变质 |
| C. | 用盐酸除去石灰水中的少量 |
| D. | 用盐酸除去铁钉表面的少量铁锈 |
某化学兴趣小组探究常温下碳酸钠(Na2CO3)饱和溶液的酸碱度。
【猜想与假设】溶液的pH可能是(填入你的猜想与假设)
① pH>7 ② pH 7; ③ pH 7。(填“>”“=”“<”)
【设计与实验】小方、小钟、小陈三位同学进行了如下实验:
小方:取pH试纸于玻璃片上,用玻璃棒蘸取Na2CO3溶液沾在pH试纸上,测得pH>7。
小钟:取pH试纸于玻璃片上,先用蒸馏水润湿pH试纸,然后用玻璃棒蘸取Na2CO3溶液沾在pH试纸上,测得pH>7。
小陈:取pH试纸直接浸入Na2CO3溶液中,测得pH>7。
【评价】以上三位同学中操作正确的是 同学,其余两位同学操作上都有错误,其中 同学所测得的pH值会比实际值偏小。
【结论】从物质的类别看,碳酸钠是一种 (填“酸”或“碱”或“盐”),它的水溶液显碱性,所以它的水溶液能使紫色石蕊溶液变 色。
【应用】工业上常使用碳酸钠与熟石灰来制取氢氧化钠,请写出该反应的化学方程式
。该反应所属基本化学反应类型是 。
实验室有两瓶失去标签的溶液,一瓶是稀盐酸,另一瓶是氢氧化钠溶液。下列试剂不能将它们鉴别出来的是( )
| A.酚酞溶液 | B.镁条 | C.硫酸铜溶液 | D.氯化钾溶液 |
下列四个图像中,能正确反映对应变化关系的是( )
 |
 |
 |
 |
| A.向一定量的稀盐酸中加入过量的镁粉 |
B.向一定量的稀盐 酸中加入足量的水稀释 |
C.向两份完全相同的稀盐酸中分别加入锌粉、镁粉 |
D.向一定量氢氧化钠溶液中滴加稀盐酸 |
下表用甲试剂鉴别乙中的两种化肥,难以实现的是 ( )
| |
甲 |
乙 |
| A |
Ca(OH)2 |
CO(NH2)2、NH4HCO3 |
| B |
Ba(NO3)2 |
KCl、(NH4)2SO4 |
| C |
AgNO3 |
NH4Cl、NH4NO3 |
| D |
NaCl |
K2SO4、KNO3 |
(4分)某化学课堂围绕“酸碱中和反应”,在老师引导下开展探究活动,请你和同学们一起进行实验探究。
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中。
【知识梳理】该反应的化学方程式为(1) ;
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想与假设】
甲组:只有Na2SO4 乙组:有Na2SO4和H2SO4 丙组:有Na2SO4和NaOH
【收集证据】丙组同学取烧杯中的溶液少量于试管中,滴加几滴酚酞试液溶液,无明显变化,溶液中一定没有(2) 。
【表达与交流】为了验证其余猜想,甲组同学的实验方案是取少量试液于试管中,滴加氯化钡溶液,观察是否有白色沉淀产生。你认为他们的实验方案(3) (填“正确”或“不正确”),你的理由是(4) 。
乙组同学取少量试液于试管中,加入(5)______ 溶液,振荡,观察到(6)___________________________,证明自己的猜想是正确的。
【反思与评价】为回收硫酸钠,应取剩余试液于烧杯中,加入(7)______ 溶液,充分搅拌,蒸发即可得到纯净的硫酸钠。