将一定量的锌粉加入到硫酸镁和硫酸铜的混合溶液中,反应一段时间后过滤,得无色滤液和滤 渣。滤渣的成分可能是()
| A. | 锌 | B. | 镁、铜 | C. | 锌、铜 | D. | 镁、锌、铜 |
下列事实不能用金属活动性顺序解释的是()
| A. | 银的导电性强于铜 |
| B. | 镁和铝与稀盐酸反应的剧烈程度不同 |
| C. | 金属铜与稀硫酸不反应 |
| D. | 铜能将银从硝酸银溶液中置换出来 |
回答下列与金属有关的问题
(1)在黄铜(铜锌合金)片和纯铜片中,硬度较大的是,将它们分别放入稀盐酸中能产生气泡的是;
(2)铁生锈是铁与空气中的发生化学反应的过程;
(3)向
和
的混合溶液中加入一定量Al粉,充分反应后过滤;取少量滤液滴加稀盐酸,产生白色沉淀.滤液中一定含有的溶质是。
下列反应发生后,固体质量增加的是( )
| A. | 铁丝在纯氧中剧烈燃烧 |
| B. | 将锌片插入稀硫酸中 |
| C. | 加热高锰酸钾制氧气 |
| D. | 氢气在加热条件下还原氧化铜 |
下列认识或做法正确的是( )
| A. | 在煤炉上放一壶水就能防止一氧化碳中毒 |
| B. | 对于人体必需的元素摄入量越多越好 |
| C. | 用铁制容器放波尔多液(含硫酸铜) |
| D. | 用白醋除热水瓶胆内的水垢 |
探究 、 、 三种金属的活动性顺序,下列试剂的选择方案不可行的是()
| A. | 、 、 溶液 | B. | 、 、 、稀硫酸 |
| C. | 、 、 溶液 | D. | 、 溶液、 溶液 |
(2分)如图所示,弹簧测力计下挂一重物A,烧杯中盛有溶液B。试根据要求回答下列问题(忽略A、B体积变化):
(1)若B为饱和氯化钠溶液,A与B不反应,向B中加入少量硝酸钾晶体,弹簧测力计示数
将 (填“变大”、“变小”或“不变”,下同);
(2)若A为铁块,B为硫酸铜溶液,将A放入 B中,过一会儿,弹簧测力计的示数将 。
在质量相等、质量分数相同的稀硫酸中,分别加入等质量的镁粉和铁粉,生成氢气的质量 随反应时间 的变化如图所示,下列叙述错误的是()

| A. | 反应结束后稀硫酸都没有剩余 |
| B. | 表示镁和稀硫酸发生反应 |
| C. | 反应结束后消耗的两种金属质量相等 |
| D. | 反应结束后消耗的镁与铁的质量比为3∶7 |
在已平衡的天平两边分别放一个等质量的烧杯,烧杯中装有等质量等质量分数的足量稀盐酸,在左边烧杯中加入13g锌片,要使天平再次保持平衡,需要在右边烧杯中加入铜片的质量为
| A. | 13g | B. | 12.6g |
| C. | 10g | D. | 11.6g |
某化工厂的废液中含有硝酸银、硝酸亚铁和硝酸锌.某同学取适量的上述废液样品,将一定质量的镁粉加入样品中,充分反应后过滤,得到滤液和滤渣.请填空:
(1)若得到的滤液为浅绿色,则滤液中的溶质一定含有(填写化学式,下同),可能含有。
(2)若得到的滤液为无色,则滤渣中至少含有种金属。
(3)反应后得到滤渣的质量(选填"小于"、"大于"或"等于")反应前加入镁粉的质量。
将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(
)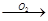 钠的氧化物
钠的氧化物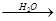 氢氧化钠溶液
氢氧化钠溶液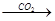 白色固体
白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(
)外还有过氧化钠(
),氧化钠与过氧化钠都能与水发生反应,方程式如下:
;
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:
,
猜想2:
,
猜想3:
【实验探究一】:
| 实验操作 |
实验现象 |
实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 |
猜想1正确 |
【继续探究】:钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:
猜想二:
和
【实验探究二】:
| 实验操作 |
实验现象 |
实验结论 |
| 1.取少量白色固体加入足量 |
产生白色沉淀 |
白色固体成分 和 |
| 2.过滤、取少量滤液加入 |
【实验反思】
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式 。
(2)过氧化钠也能与盐酸反应,方程式为:
,X的化学式为 。
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断
碱性氧化物(填"是"或"不是")。
金属是重要的资源,在日常生活中已得到越来越广泛的应用.

(1)铜常用于制作导线,因为其具有良好的。
(2)将纯铝和铝合金相互刻画,纯铝上留下明显划痕,说明。
(3)对汽车部分钢铁部件进行喷漆可以防止其生锈,原因是。
(4)如图,向一定量
溶液中加入铜和锌的混合粉末,充分反应后过滤,的溶液甲和固体乙。
①若乙中含有锌、铜、银三种固体,则溶液甲中所含的金属离子符号为,此时向固体乙中加入稀盐酸,发生反应的化学方程式为,该反应类型为反应。
②若溶液甲显蓝色,是因为(用化学反应方程式表示),此时固体乙中一定含有的物质是。
化学学习中常用到"质量守恒"、"反应先后"等思想来分析、解决问题.下列推断正确的是( )
| A. |
酒精中加入 水,根据溶质守恒推出酒精溶液的溶质质量分数为 |
| B. |
酒精燃烧生成 和 的分子个数比为 ,根据原子守恒推出酒精分子中 、 原子个数比为 |
| C. |
少量铁粉放入硝酸银和硝酸铜的混合溶液中,根据反应的先后推出析出固体铜 |
| D. |
向硫酸铜与硫酸的混合溶液中滴加氢氧化钠溶液,根据反应的先后推出先生成蓝色沉淀 |
某实验小组在探究金属的化学性质的时,得到金属与酸反应制取氢气的质量关系(见下图)。请根据图像信息判断,下列说法正确的是()
| A. | 四种金属与酸反应的速率: |
| B. | 四种金属的活动性顺序: |
| C. | 同质量的四种金属与足量酸反应得到氢气的质量: |
| D. |
、 、 、 四种金属与酸反应得到氢气的质量比: |
下列事实的结论或解释中不正确的是( )
| A. | 水烧开后易把壶盖冲起﹣﹣说明温度升高分子会变大 |
| B. | 公园的桂花开放时满园飘香﹣﹣说明分子在不断运动 |
| C. | 酸碱中和反应都能生成水﹣﹣实质是 与 结合生成了 |
| D. | 铝制品有抗腐蚀性能﹣﹣实质是表面生成了致密氧化膜起保护作用 |