氧化亚铜(Cu2O)可用于船底防污漆,防止海生物对船舶设备的污损。某氧化亚铜样品中含有10%的金属铜,现取4.0g该样品放入烧杯中,加入一定溶质质量分数的稀硫酸恰好完全反应,得到27.0g不饱和溶液。发生反应的化学方程式为Cu2O+H2SO4=CuSO4+Cu+H2O
请计算:(1)所取样品中氧化亚铜的质量为________g。
(2)所用稀硫酸溶质的质量分数。
造纸厂会产生含氢氧化钠的废水,需经处理呈中性后排放。为测定某造纸厂废水中氢氧化钠的质量分数,小明取40g废水样品加入到锥形瓶中,逐滴加入10%的稀硫酸,至恰好完全反应时,消耗稀硫酸49g。计算废水中氢氧化钠的质量分数。
为了测定某种大理石废料中碳酸钙的含量,某研究小组的同学取50g该大理石样品,分5次加入200g稀盐酸(假设杂质不与盐酸反应,也不溶于水)进行充分反应。实验过程中的数据记录如下:
| 稀盐酸的质量 |
第一次 40g |
第二次 40g |
第三次 40g |
第四次 40g |
第五次 40g |
| 剩余固体质量 |
40.0g |
30.0g |
20.0g |
10.0g |
5.0g |
(1)写出实验中发生反应的化学方程式___________________________________________;
(2)根据已知条件列出求解50g大理石样品生成二氧化碳质量(x)的比例式__________;
(3)小组同学用质量分数为36.5%的浓盐酸配制200g上述稀盐酸,需要浓盐酸和水的质量比为________;
(4)向第一次反应后所得溶液中加入54.4g水,则所得溶液的溶质质量分数为__________;
(5)某工厂要想制得280t含杂质19%的生石灰,理论上需要这种大理石废料的质量为__________;
国庆前夕,为了给气球充气,王老师与小明到实验室制取氢气,王老师将一定量的锌放入一定量的稀硫酸中,恰好反应,充完气球后,在锥形瓶中得到338g溶液,小明将338g溶液平均分成两等份,做如下实验:一份蒸发8g水,另一份加入2gZnSO4粉末,所得的两份溶液质量分数相等,试问:
(1)上述制取氢气的化学反应方程式为______________________________;
(2)小明配得两份溶液质量分数相等,其质量分数为___________;
(3)设稀硫酸中溶质的质量为X,根据反应后每份338g溶液中溶质的质量,列出求解(X)的比例式_______________________________________;
(4)原稀硫酸的质量分数为____________(结果保留小数点后一位)。
人类的生活和生产都离不开金属材料。
(1)下列物质不属于合金的是 。
| A.青铜 | B.铝 | C.钢 | D.生铁 |
(2)每年因腐蚀而报废掉的金属材料数量惊人,铁生锈的条件是铁与 和 同时接触。
(3)工业炼铁可以把赤铁矿(主要成分为Fe2O3)在高炉里和CO反应,生成单质铁,
该反应的化学方程式是 ;
①氧化铁(Fe2O3)的相对分子质量是 ;
②2000t含氧化铁80%的赤铁矿中理论上可炼得含铁90%的生铁 t(保留一位小数)。
某实验小组为研究碳酸钠和碳酸氢钠混合物的组成做了以下实验:充分加热10.0 g样品至恒重,剩余固体质量为6.9 g。
查阅资料已知:碳酸氢钠受热易分解生成碳酸钠、水和二氧化碳;碳酸钠受热不易分解。
计算:(1)生成二氧化碳的质量。
(2)混合物中碳酸钠的质量分数。
请根据下图所示的实验过程和提供的数据计算: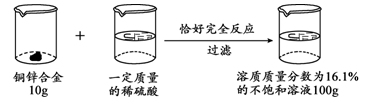
(1)生成氢气的质量。
(2)合金中铜的质量分数。
(3)所加稀硫酸的质量。
食品加工厂在制作馒头等面食时,经常会用到食用小苏打。与工业制取碳酸氢钠不同,食用小苏打是由纯碱溶液和二氧化碳反应制得:
CO2 + H2O + Na2CO3 === 2NaHCO3。
某温度下,向121.2g碳酸钠溶液中通入一定量的CO2至碳酸钠恰好完全反应,反应后的溶液中有碳酸氢钠析出,过滤,分别得到23.96g固体和106.04 g溶液。
请计算:
(1)参与反应的CO2质量。
(2)过滤后的溶液中,碳酸氢钠与水的质量比。
某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,实验测得相关数据如下图所示: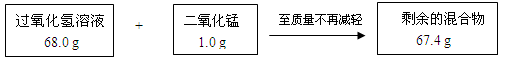
(1)剩余的混合物中二氧化锰的质量为 g,二氧化锰在反应中的作用是 ,反应生成氧气的质量为 g。
(2)计算该过氧化氢溶液中溶质的质量。
(3)计算该过氧化氢溶液中溶质的质量分数。
有一种石灰石样品,其中含有的杂质是二氧化硅(它是一种不溶于水,也不与盐酸反应,耐高温的固体物质),某同学想测定该样品的纯度,他取用2 g这种石灰石样品,把20 g稀盐酸分四次加入,充分反应后剩余固体的质量如下表所示:
| 稀盐酸的质量 |
剩余固体的质量 |
| 第一次加入5 g |
1.315 g |
| 第二次加入5 g |
0.63 g |
| 第三次加入5 g |
0.3 g |
| 第四次加入5 g |
0.3 g |
(1)2 g石灰石样品中的杂质质量是 g;
(2)石灰石样品的纯度为 ;
(3)100 kg这种纯度的石灰石充分煅烧后,可得到固体多少千克?
为了测定某黄铜(合金)中铜锌的有关数据,进行了如下实验:
(1)配制溶液:将40g质量分数为98%的浓硫酸稀释成9.8%的稀硫酸,加水稀释后溶液质量是Xg.依题意列出计算X的方程或算式(不要求计算) ______________________
(2)取26g上述合金粉末,向其中滴入上述配好的稀硫酸,至不再产生气泡为止(反应涉及的化学方程式是Zn+H2SO4=ZnSO4+H2↑),过滤,得滤渣和滤液,将滤渣洗涤、晾干称量得19.5g,求
① 26g黄铜样品中锌的质量是___________g.
② 求生成氢气的质量是多少?
为了测定某品牌小苏打样品中碳酸氢钠的质量分数,兴趣小组进行了如下图所示的实验(假设该样品中只含有氯化钠一种杂质)。请计算:
(1)生成CO2气体的质量;
(2)样品中碳酸氢钠的质量分数。
实验室有一瓶失去标签的过氧化氢溶液,为了测定其溶质质量分数,某同学取50.0g该过氧化氢溶液放入烧杯中,然后加入2.0g二氧化锰,等不再产生气泡。称得烧杯中剩余物质的总质量为50.4g.请计算此过氧化氢溶液的溶质质量分数。
现有含杂质的氯化镁样品10g(杂质不溶于水,也不参加反应),向其中加入一定量的氢氧化钠溶液恰好完全反应,过滤,得到117g质量分数为10%的溶液。
求:
(1)样品中氯化镁的质量分数。
(2)所加入氢氧化钠溶液的溶质质量分数。(计算结果精确到0.1%)。
(9分)学习酸碱中和反应时,很多同学对其产生探究兴趣.
(1)甲同学将固体氢氧化钠放入装有稀硫酸的试管中并振荡,试管壁发烫,于是他得出酸碱中和反应是放热反应的结论.乙同学认为甲同学推理不合理,理由是 .
(2)配制40g10%的氢氧化钠溶液.
步骤为:计算、称取、量取、 、转移.量取水时如俯视读数,则配得的溶液溶质质量分数将 (选填“大于”“小于”“等于”)10%,最后将氢氧化钠溶液转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是 (填字母)
A.40g B.10% C.NaOH溶液
(3)乙同学为了验证甲同学的结论,将实验加以改进:将稀硫酸慢慢滴入装有40g10%氢氧化钠溶液的烧杯中,用温度计测出反应后溶液温度随加入稀硫酸质量的变化如图所示:
①B到C的过程中,烧杯内溶液中含有的阳离子有 (填离子符号);
②恰好完全反应时所得溶液中溶质质量分数.