2012年3月22日是“世界水日”。水与人类的生活和生产密切相关。请回答以下问题:
(1)生理盐水中的溶质是 (填化学式)。
(2)下列洗涤方法中,利用乳化原理的是 ( )
A.用食醋除水垢 B.用稀盐酸除铜粉中的铁粉
C.用汽油清洗油渍 D.用洗洁精清洗油污
(3)课外活动中,同学们玩起了以水为主题的“化学反应接龙”游戏。游戏的规则为:用前一个反应的一种生成物作为下一个反应的反应物,并按序号和要求的基本反应类型循环,如上图a所示。仿照示例完成下列反应的化学方程式。
示例:①分解反应:电解水2H2O 2H2↑+O2↑
2H2↑+O2↑
②置换反应
③化合反应
(4)右图b是A、B、C三种物质(均不含结晶水)在水中的溶解度曲线。
①t1℃时,A、B、C三种物质中溶解度最大的是 ;
②t2℃时,将C物质的饱和溶液转化为不饱和溶液的方法有 (填一种)。
下列关于“一定”的说法存在科学性错误,请举一实例说明:
(1)均一、稳定、无色透明的液体一定是溶液(写名称,下同)
(2)含有氢、氧元素的化合物一定是碱
(3)由同种元素组成的物质一定是单质
(4)化学反应前后分子的数目一定不变(用化学方程式表示)
化学与生活息息相关,请运用化学知识回答下列问题:
(1)测土壤溶液的酸碱度常用 ;
(2)检验软水和硬水常用 ;
(3)在水的净化中常用的除臭剂是 ;
(4)用分子的知识解释“缉毒犬”能够辨别气味,发现毒品的原因是 .
大量实验表明,少量固体物质溶于水所形成的溶液具有与水不同的性质,常被人们应用于日常生活.如:冬天常在汽车的水箱内加入少量的乙二醇,其目的是
▲ ;在高原煮鸡蛋,在水中加食盐的目的是 ▲ ;做溶液导电性实验时,向水中滴几滴稀硫酸,能增强溶液的 ▲ 性.
请根据溶液的有关知识回答下列问题:
(1)将
饱和溶液变成不饱和溶液可采取的措施有.
(2)"海水晒盐"的原理是.
(3)配制0.9%的生理盐水的主要实验操作步骤有.
20℃时氯化钠的溶解度为36克。该温度下,某氯化钠溶液的组成模型如图,请你回答: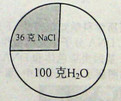
(1)该溶液的溶质是
(2)保持温度不变蒸发10克水后,氯化钠溶液的溶质质量分数 。(填“变大”、“变小”、“不变”)
日常生活中许多现象与化学有着密切联系,请选择适当的物质填空:医用酒精的溶剂是 ;冬天用煤火取暖,若通风不畅会发生中毒,是由 引起的。
(5分)溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。
(1)衣服上沾有的油污,可用汽油洗去,是因为汽油能 (填“溶解”或“乳化”)油污。
(2)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体的溶解度与 有关。
(3)某固体物质的溶解度曲线如下图所示:
20℃时,要使接近饱和的该物质的溶液变为饱和溶液,通常可采用三种方法,它们
分别是 、 、 。
水和溶液在生产生活中起重要作用。
(1)下列图甲、图乙代表水的两种变化,按要求回答下列问题。(图“ ”表示氢原子,图“
”表示氢原子,图“ ”表示氧原子)
”表示氧原子)
①请从微观角度解释图甲变化的原因: 。
②图乙中:反应后方框内应再填入 个“ ”微粒。
”微粒。
③图甲和图乙两种变化的微观本质区别是 。
④请结合生活实例,说明微观粒子的其它性质: 。
(2)①将厨房中常用的四种物品分别放入水中,能形成溶液的是 (填序号)。
a.蔗糖 b.花生油 c.味精 d.面粉
②现欲将300 g 25%的NaCl溶液稀释为15%的NaCl溶液用于农业选种,需要加水的质量为
g。
元旦联欢会上,雯雯拿出一幅画(如图所示),表演了一个化学魔术。
(1)她向画中的衣服上喷了一种无色溶液,衣服由紫色变成红色,若衣服上预先涂过石蕊溶液,则喷的无色溶液可能是 。
(2)她向画中的灯笼上喷了另一种无色溶液,灯笼由白色变成红色,则该无色溶液及灯笼上预先涂过的试剂分别是 。

归纳与整理是化学学习的一种重要方法。
(1)某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你来解决下列问题:
A.小红同学从某一欠收农田里取回一份土壤样品,如果检测结果呈酸性,从经济和可行方面考虑,那么要改良此土壤的酸性,应向农田里施加 (填化学式)。
B.小红同学用下图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)。
I.为了验证反应①,小红将无色酚酞试液滴入NaOH溶液中,溶液由无色变成 。
II.依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为: 。
III.为了验证反应③能够发生,你选择的物质是 。
a.Na2CO3 b.HCl c.FeCl3 d.Ba(NO3)2
C.请你设计一个实验除去FeCl2溶液中少量的CuCl2,请写出主要操作步骤和化学方程式。实验主要操作步骤: 、 ,
化学方程式: 。
(2)甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
①25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为 g。
②要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是 。
③现有操作步骤: a.溶解 b.过滤 c.降温结晶 d.加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤是 (填字母序号)。
④将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数 (填“变大”、“变小”或“不变”)。
⑤向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出。你认为“全部溶解”的原因可能是 。
已知某物质在不同温度下的溶解度数据如下表所示:
| 温度(℃) |
0 |
20 |
40 |
60 |
80 |
| 溶解度(克) |
12.6 |
15.3 |
20.0 |
25.0 |
38.2 |
如果要配制该物质溶质质量分数为20%的饱和溶液200克,需要水克,此时溶液的温度应为℃。
某化学兴趣小组进行溶液的配置和粗盐的初步提纯实验.
(1)配置150g质量分数为10%的氢氧化钠溶液.
①计算:需要氢氧化钠固体的质量为 g;水的体积为 mL(水的密度近似看作1g/cm3)
②称量:调节托盘天平平衡后,将 放在托盘天平的左盘,称量其质量.然后再右盘添加 .最后添加氢氧化钠固体,直至天平平衡.
③溶解:用量筒量取所需的水,倒入装有氢氧化钠固体的烧杯里,用玻璃棒 ,使其溶解,并冷却至室温.
④存储:把配好的溶液装入试剂瓶,塞好橡皮塞并 ,放到指定的地方.
(2)粗盐的初步提纯实验
①称取5.0g粗盐,用药匙逐步加入10mL水中,知道粗盐不再溶解为止.还需要进行的实验步骤的顺序为:称量剩余粗盐、 (填编号)
| A.过滤 | B.计算产率 | C.蒸发 | D.称量精盐 |
②过滤操作如图所示,指出其中的错误之处: ; ; ;
.