在化学小组为探究铝、铜、银三种金属的活动性顺序,设计了如图所示实验方案。下列说法不正确的是( )

A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.由实验甲、乙、丙可知金属活动性:Al>Cu>Ag
D.实验甲中的CuSO4改为CuCl2不能完成本实验探究
自2011年我省实施找矿战略行动以来,在铜、铅、锌、金、铁、铌、钽等金属方面取得找矿新成果.下列关于铁、锌、铜三种金属及其合金的说法不正确的是( )
| A. |
铁在潮湿的空气中易生锈 |
| B. |
可以用铁桶盛放硫酸铜溶液 |
| C. |
可以用稀硫酸鉴别锌与铜的金属活动性强弱 |
| D. |
黄铜(铜与锌的合金)的硬度大于纯铜 |
将一定量的锌粉加入到Mg(NO 3) 2、Cu(NO 3) 2、AgNO 3三种物质的混合溶液中充分反应后过滤,将滤渣放入稀盐酸溶液里,有气泡产生。则下列情况不可能存在的是( )
| A. |
滤渣是Ag、Cu、Zn |
| B. |
滤渣是Ag、Cu、Mg |
| C. |
滤液中含有Zn 2+、Mg 2+、NO 3 ﹣ |
| D. |
金属活动性顺序是Ag<Cu<Zn<Mg |
据图示判断X、Y、Z三种金属与氢的活动性由强到弱的顺序是( )

| A. |
X>H>Y>Z |
B. |
Y>Z>X>H |
C. |
Z>Y>X>H |
D. |
X>H>Z>Y |
如图"→"表示一种金属能把另一种金属从其盐溶液中置换出来,则甲、乙、丙三种金属的活泼性由强到弱的顺序是( )

| A. |
甲、乙、丙 |
B. |
乙、丙、甲 |
C. |
丙、甲、乙 |
D. |
甲、丙、乙 |
将金属M放入稀硫酸中M溶解并产生气泡:将M放入硫酸锌溶液中,无明显现象,根据以上实验事实推测M可能是( )
| A. |
Cu |
B. |
Ag |
C. |
Mg |
D. |
Fe |
将a、b、c三种金属分别投入稀盐酸中,只有b溶解并产生气泡;把a和c分别放入硝酸银溶液中,在a表面有银析出,c没有变化。则a、b、c三种金属可能是( )
| A. |
Fe、Cu、Ag |
B. |
Cu、Ag、Fe |
C. |
Cu、Zn、Ag |
D. |
Ag、Zn、Cu |
以下实验能比较出铜和银的金属活动性强弱的是( )
| A. |
测定两种金属的密度 |
| B. |
铜片放入硝酸银溶液中 |
| C. |
将两种金属片相互刻划 |
| D. |
铜片、银片分别放入稀硫酸中 |
下列实验现象记录正确的是( )
| A. |
把铜丝放入硫酸铝溶液中,紫红色固体表面产生银白色固体,溶液变成蓝色 |
| B. |
向氢氧化钾溶液中滴入氯化铁溶液,有浅绿色沉淀生成 |
| C. |
将一氧化碳通入灼热的氧化铁,红棕色粉末逐渐变为黑色粉末 |
| D. |
将燃着的木炭伸入氧气中,产生白色火焰,放出热量 |
根据金属活动性顺序判断,下列容器与所盛放溶液不会发生化学反应的是( )
| A. |
用铁制容器盛盐酸 |
B. |
用铜制容器盛盐酸 |
| C. |
用铁制容器盛硝酸银溶液 |
D. |
用铜制容器盛硝酸银溶液 |
小柯为比较Mg、Fe、Cu三种金属的活动性顺序,进行了如图甲所示的实验。实验后把两试管中的物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,充分反应后过滤。滤液中含有的金属离子可能的组成有( )
①Mg 2+
②Mg 2+和Fe 2+
③Fe 2+和Cu 2+
④Mg 2+、Fe 2+和Cu 2+

| A. |
①② |
B. |
①③ |
C. |
②④ |
D. |
③④ |
在柠檬中插入两种不同活动性的金属可以制得水果电池。相同条件下,水果电池的电压与两种金属的活动性差异大小有关。下列柠檬电池的两种金属,活动性差异最大的是( )
| A. |
|
B. |
|
| C. |
|
D. |
|
往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是( )

| A. |
c点对应溶液中含有的金属离子为Zn 2+和Cu 2+ |
| B. |
bc段(不含两端点)析出的金属是Fe |
| C. |
ab段(不含两端点)对应溶液中含有的金属离子为Zn 2+、Ag +、Cu 2+和Fe 2+ |
| D. |
若bc段和cd段中析出固体质量相等,参加反应的锌粉质量分别为m 1和m 2,则m 1>m 2 |
某废液中只含有Fe(NO3)2、Cu(NO3)2、Ba(NO3)2三种溶质,为了回收金属、保护环境,小科设计了如图方案(所加试剂均过量),下列判断正确的是( )
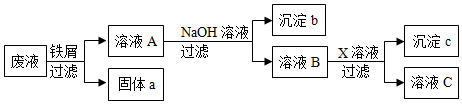
A.固体a是铜
B.X一定是Na2SO4
C.溶液B中含有的盐有Ba(NO3)2、NaNO3
D.若回收到6.4g固体a,则加入的铁屑质量为5.6g