根据图中A,B.C三种固体的溶解度曲线回答:
(1)t1℃时,A的不饱和溶液变成饱和溶液可采用的一种方法是 ;
(2)t2℃时,A,B,C三种物质的溶解度大小关系是 ;
(3)将t2℃的A,B,C三种物质的饱和溶液降温到t1℃,不会析出晶体的是 。

南海是我国的固有领海,蕴藏着丰富的海洋资源。2017年5月18日,我国南海神狐海域的可燃冰试采取得圆满成功,实现历史性突破。
(1)可燃冰的主要成分是甲烷。请你写出甲烧在空气中燃烧的化学方程式: 。
(2)可燃冰被科学家誉为“未来能源”“21世纪能源”,原因是 。
(3)1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图2所示,试回答下列问题:

①t1℃时,NaCl的溶解度 Na2CO3的溶解度(填写“大于”“等于”“小于”之一)。
②t1℃时,50g水中加入10g Na2CO3,经充分溶解,所得溶液中溶质与溶液的质量之比为 (填最简整数比)。
③t1℃时,将不同质量的碳酸钠饱和溶液和氯化钠饱和溶液均升温至t2℃,此时所得碳酸钠溶液溶质质量分数 氯化钠溶液溶质质量分数(填写“大于”“等于”“小于”“无法判断”之一)。
下列说法中,不正确的是( )
A.溶液中有晶体析出时,溶质质量减小,则溶质质量分数一定减小
B.将钢铁制成合金是有效减缓钢铁制品锈蚀的方法之一
C.碱溶液中都含有氢氧根离子,因此碱具有相似的化学性质
D.自然界中二氧化碳的循环平衡,对地球生命具有重要意义
根据下表回答问题:
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
溶解度 /g |
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
NH4Cl |
33.5 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
|
(1)海水中含有大量的氯化钠,海水晒盐的原理是 ,氨碱法制纯碱先向饱和食盐水中通入氨气,通入氨气的作用是 ,可向滤出晶体后的NaHCO3溶液中加入 以回收氨,使之循环使用。
(2)氯化钠和氯化铵具有相同溶解度的温度范围在 ℃之间。
(3)图中,A是60℃时含有120g水的NH4Cl溶液,经过如下操作后,得到固体。

I.C中溶液的质量是 g.A溶液为NH4Cl的 (选填“饱和”或“不饱和”)溶液,该溶液中溶质的质量分数为 (结果精确到0.1%)。
II.对以上过程的分析,正确的是 (选填编号)。
①A到B的过程中,溶质质量没有改变
②B中溶质与溶剂的质量比为55.2:100
③由B到C开始析出NH4Cl固体的温度在40℃至50℃之间。
根据下表回答问题:
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
溶解度 /g |
NaCl |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
NH4Cl |
33.5 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
|
(1)海水中含有大量的氯化钠,海水晒盐的原理是 ,氨碱法制纯碱先向饱和食盐水中通入氨气,通入氨气的作用是 ,可向滤出晶体后的NaHCO3溶液中加入 以回收氨,使之循环使用。
(2)氯化钠和氯化铵具有相同溶解度的温度范围在 ℃之间。
(3)图中,A是60℃时含有120g水的NH4Cl溶液,经过如下操作后,得到固体。

I.C中溶液的质量是 g.A溶液为NH4Cl的 (选填“饱和”或“不饱和”)溶液,该溶液中溶质的质量分数为 (结果精确到0.1%)。
II.对以上过程的分析,正确的是 (选填编号)。
①A到B的过程中,溶质质量没有改变
②B中溶质与溶剂的质量比为55.2:100
③由B到C开始析出NH4Cl固体的温度在40℃至50℃之间。
右图为甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )

A.20℃时,甲物质的溶解度比乙物质的溶解度小
B.甲物质中混有少量乙物质,采用蒸发结晶的方法提纯甲物质
C.40℃时,甲、乙两种物质的饱和溶液中溶质质量分数相等
D.60℃时,将80g甲物质放入100g 水中,所得溶液中溶质质量与溶剂质量之比是 4:5
酸、碱、盐是重要的化合物,研究它们的性质有重要意义.
(1)NaCl、KNO3、NH4Cl三种固体在水中的溶解度曲线如图所示,请仔细观察曲线,回答下列问题:
①三种固体物质的溶解度受温度影响最小的是 .
②30℃时三种固体物质饱和水溶液中溶质的质量分数由大到小的顺序是 .
③图中A、B点的坐标为:A(10,21)、B(40,64).若将100g40℃的硝酸钾饱和水溶液降温到10℃,析出KNO3固体的质量为 g(保留一位小数).
(2)实验桌上有NaOH、Ba(OH)2、Na2CO3、稀硫酸四种溶液,它们只有编号却没有标签.某同学按下列步骤鉴别四种溶液.

①写出反应Ⅲ的化学方程式 .
②如图是水和NaOH水溶液中微粒的存在情况示意图,由此分析C溶液能使酚酞溶液变红的原因是 (填序号).

a.C溶液中Na+数目大于CO32﹣数目
b.C溶液中H2O数目大于OH﹣数目
c.C溶液中H2O数目大于H+数目
d.C溶液中OH﹣数目大于H+数目.

如图是甲、乙两种物质的溶解度曲线,以下说法正确的是( )

A.15℃时,甲物质溶液中溶质的质量分数一定等于乙物质溶液中溶质的质量分数
B.15℃时,甲物质饱和溶液和乙物质饱和溶液中溶质与溶剂的质量比为1:5
C.30℃时,甲物质的饱和溶液和乙物质的饱和溶液降温至15℃时均是饱和溶液
D.30℃时,甲物质溶液中溶质的质量分数一定小于乙物质溶液中溶质的质量分数
如图是3种物质的溶解度曲线,下列叙述正确的是( )

A.0℃时,NaCl的溶解度小于NH4Cl的溶解度
B.40℃时,饱和Na2CO3溶液的溶质度量分数为49%
C.将饱和Na2CO3溶液由80℃冷却至40℃时,有固体析出
D.80℃时,分别将等质量的NH4Cl和NaCl固体溶于适量的水,恰好均配成饱和溶液,所得溶液的质量前者小于后者
KNO3、NaNO3、NaC1的溶解度曲线如图所示,下列说法正确的是( )

A.20℃时,KNO3的溶解度最大
B.0℃时,100 g NaNO3饱和溶液中含73 g NaNO3
C.从NaCl溶液中获取NaCl晶体时,必须采用冷却热饱和溶液的方法
D.分别将20℃的KNO3、NaNO3饱和溶液加热至80℃时,KNO3溶液溶质的质量分数小于NaNO3溶液
下列说法正确的是( )
| A. |
原子通过得失电子形成离子,离子一定不能形成原子 |
| B. |
不饱和溶液转化为饱和溶液,溶质的质量分数一定增大 |
| C. |
中和反应生成盐和水,有盐和水生成的反应一定是中和反应 |
| D. |
某溶液中滴入无色酚酞试液后变红,该溶液一定是碱性溶液 |
KNO3与KCl的溶解度曲线如图所示。下列说法正确的是( )
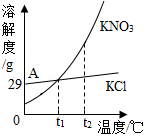
A.KNO3的溶解度比KCl的溶解度大
B.t1温度下的KCl的饱和溶液升温至t2,有晶体析出
C.A点所表示的KCl饱和溶液溶质的质量分数为29%
D.冷却热的KNO3饱和溶液可获得KNO3晶体
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )

A.t1℃时,甲、乙的溶液中所含溶质质量相等
B.t2℃时,将50g甲加入50g水中,可得到100g溶液
C.甲中含有少量乙时,可用降温结晶法提纯甲
D.t1℃时,分别将甲、乙的饱和溶液升温至t2℃,所得溶液的溶质质量分数甲>乙
甲、乙、丙三种固体物质的溶解度曲线如图所示,从中获取的信息正确的是( )

A.蒸发溶剂可使丙的饱和溶液变为不饱和溶液
B.t2℃时,100g甲的饱和溶液降温至t1℃,析出甲的质量为15g
C.t1℃时,甲、乙、丙三种溶液所含溶质的质量可能相同
D.t2℃时,甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数大小顺序为乙>甲=丙