水和溶液在生产生活中起着重要的作用。
(1)生活中可用 检测饮用水是否为硬水;
(2)下列物质分别放入足量水中,充分搅拌后可得到溶液的是 (填序号);
| A.细沙 | B.食用油 | C.面粉 | D.白糖 |
(3)某同学欲配制50g 8%的氯化钠溶液。在量取水时俯视读数,若其他环节均正确,则所配溶液的溶质质量分数 8%(填“大于”或“小于”或“等于”);
(4)铁在氧气中燃烧的实验里,集气瓶底放少量水的作用是 。
今年3月22-28日是第28届“中国水周”,其主题为“节约水资源,保障水安全。”人类的日常生活和工农业生产离不开水。
(1)城镇自来水厂生产流程可用下图表示:

除去水中固态杂质的设备是:_ ___;投药(多为ClO2)的作用是_ ___。活性炭的作用是 。自来水厂的净水过程 (填“能”或“不能”)将硬水软化成软水,生活中将硬水软化的方法是 。
(2)海水淡化可缓解淡水资源匮乏的问题。右图为太阳能海水淡化装置示意图。

①水变成水蒸气的过程中,不发生变化的是 (填字母序号)。
A.分子质量 B.分子种类 C.分子间隔
②利用该装置将一定量的海水暴晒一段时间后,剩余海水中氯化钠的质量分数会 (填“变大”、“变小”或“不变”)
化学就在我们身边,它与我们生产生活息息相关。请从①稀有气体、②氧气、③食盐、④明矾中选择符合题意的物质,并用其符号填空。
(1)可供给人类呼吸的气体是 ;
(2)烹饪时可作调味品的是 ;
(3)作为焊接金属的保护气的是 。
(4)可以吸附水中的悬浮杂质而沉降的是 。
河水净化的主要步骤如下图所示,请回答下列问题

(1)步骤Ⅰ中加入的絮凝剂一般是 ;
(2)步骤Ⅱ的操作是 ,如果实验室进行此操作所需的玻璃仪器是玻璃棒、烧杯和 ;
(3)步骤Ⅳ加入液氯消毒,液氯(Cl2)与水反应生成氯化氢(HCl)和次氯酸(HClO),是利用次氯酸的强氧化性来杀菌,写出该反应的文字或符号表达式 ;
(4)可以向净化的水中加入 ,来检验是硬水还是软水。
水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解一些有关水的知识。请你回答:
(1)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是 .
(2)硬水给生活和生产带来很多麻烦,生活中可用 来区分硬水和软水,常用 的方法来降低水的硬度.
(3)请写出水在通电条件下反应的化学方程式 .
(4)请写出两个产物为MgCl2和水的化学方程式: 、 .
某同学将浑浊的湖水样品倒入烧杯中,先加入絮凝剂,静置一会后,用下列左图所示装置进行过滤,请问:

(1)常用的絮凝剂是 ,其作用 。
(2)左图中还缺少的一种仪器,该仪器是 。其作用是 。
(3)过滤后发现,滤液仍浑浊,可能的原因是 。(一种即可)
(4)改进后过滤,得到了澄清透明的水,他兴奋地宣布:我终于制得了纯水!对此你的看法为
(填“是”或“不是”)纯水,理由是 。
(5)他按右图将该水电解:甲试管中产生的气体是 ,乙试管中产生的气体是 。甲乙两试管中产生的气体体积比约是 ,实验时常在水中加入硫酸钠等物质其目的是 ,此实验得到的结论:水是由 组成的。
水是生命之源,万物之基,是人类宝贵的自然资源,我们每个人都要关心水、爱护水、节约水。
(1)我国规定生活饮用水的水质必须达到下述四项指标:
a.不得呈现异色;
b.不得有异味;
c.应澄清透明;
d.不得含有细菌和病毒.
其中“c指标”可以通过 操作达到;
(2)“水的质量决定生命的质量”这句广告词充分说明了饮用水的质量关系到我们的健康。
生活中常采用 的方法降低饮用水的硬度。除去饮用水的异味可采用的物质是 ,测定饮用水的酸碱度,可使用 。高铁酸钾(K2FeO4)是一种“绿色”环保高效净水剂,可由如下反应制得:Fe2O3 + 3X + 4KOH=2K2FeO4 + 3KNO2 + 2H2O,则X的化学式为 ,K2FeO4中Fe的化合价为 。
某校研究性学习小组对县城某段溪水水质的状况进行相关的调查研究。
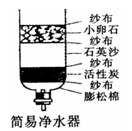
(1)如图所示的自制净水器中的 物质,可除去水中的异味和色素。
(2)硬水会给生活和生产带来许多麻烦,长期饮用硬水可能会引起体内结石;如用硬水洗涤衣物,既浪费肥皂又洗不干净,时间长了还会使衣物变硬。通过化学学习,我们知道可用 来区分该内河的水属于硬水还是软水;生活中要降低水的硬度,可采用的方法是 。
(3)你认为下列行为不会造成溪水水质下降的是 。(填标号)
A.在河边种植花草树木
B.居民将生活污水直接排入内河
C.将垃圾倒入内河中
(4)有些科学家预言:“世界上最后一滴水就是人类的眼泪”.这句话警示我们应树立保护水资源的意识:一是节约用水,二是防止水体污染.请你举一例节约用水的做法: (合理答案均可)
(5)在实验室我们也可以借助漏斗等仪器来过滤少量的浑水,使之较为干净。如下图所示,玻璃棒的作用是

(6)某同学用如如图的装置进行过滤操作,实验后发现滤液仍浑浊,请你写出可能的任意一点原因:
将浑浊的河水净化的实验过程如下图所示:

(1)操作①必须使用的玻璃仪器有:漏斗、 和烧杯,若经操作①,
所得液体a仍浑浊,其原因可能是 (填写序号)。
①漏斗内的滤纸有破损 ②漏斗下端未靠在烧杯内壁 ③漏斗内液面高于滤纸的边缘
(2)若液体a有异色异味、液体b无异味异味,则加入物质B是 (填“明矾”或“活性炭”)。
(3)若液体b为硬水,则操作③可以是 。
a. 过滤 b. 蒸馏 c. 加明矾、搅拌、静置
人类的生活和工农业生产都离不开水.如图是自来水厂净水过程示意图.
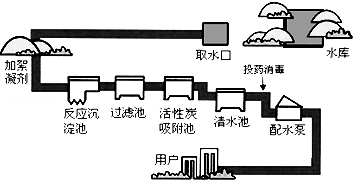
请根据图示回答下列问题:
(1)自来水厂生产自来水时,使用下列的净水方法有 ;
A 沉淀 B 过滤 C 煮沸 D 蒸馏 E 吸附
(2)实验室进行过滤操作时,玻璃仪器除了烧杯、漏斗外还需要 ,其作用是 .
(3)进入用户的水 (填“是”或“不是”)纯水,生活中采用 的方法将硬水软化.
(4)实验室常用电解水的实验来探究水的组成,其化学反应方程式为 .
水是一种重要的资源,人类的日常生活和工农业生产离不开水。请回答:
(1)图1是实验室电解水的示意图。实验中生成氧气的试管是 (填“1”或“2”),该反应的化学方程式为: 。

图1 图2
(2)图2表示自来水生产的一般过程。下列说法正确的是
| A.加入絮凝剂使水中悬浮物凝聚 | B.通过沙滤池除去水中可溶性杂质 |
| C.通过活性炭吸附有色物质和有臭味物质 | D.通入氯气杀菌消毒 |
(3)我国南海海岛众多,但淡水资源匮乏。为了解决这一问题,人们设计了太阳能海水淡化装置,原理如图3所示。
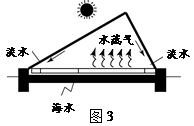
① 在相同时间内,海岛上晴好天气比阴雨天气制得淡水更多,其微观解释是 。
② 若某海水中氯化钠的质量分数为2.5%,利用该装置将1000kg的海水暴晒一段时间后,测定发现,剩余海水中氯化钠的质量分数是原来海水的十倍,则可得到的淡水为 kg;已知该温度下氯化钠的溶解度为36g,则剩余海水是 (填写“饱和溶液”、“不饱和溶液”或“不确定”)。
如图所示是初中化学的一些重要实验,请回答:

(1)实验A:通电后,乙中产生的是 ,区别硬水和软水的试剂是 ,现象是 。写出该实验反应的化学方程式 。
(2)实验B:测得空气中氧气体积分数小于五分之一的原因可能是 (只答一条)
(3)实验C:图中a的名称是 ,在操作中,它的作用是 ,浑浊的河水经过该装置过滤后得到的水是 (“纯净物”或“混合物”).
(4)实验D:集气瓶内放少量水的目的是 ,观察到_____ 现象,写出铁丝与氧气反应的化学方程式 。
(5)实验E:倾倒CO2时观察到的现象是___ _.
水是人类生活中不可缺少的物质.
下列净水方法中,通常用于除去水中难溶性杂质的是 ,净水程度最高的是
| A.过滤 | B.煮沸 | C.蒸馏 | D.吸附 |
自来水厂常用二氧化氯消毒,其中氯元素的化合价为 ;
自来水中含有少量Ca2等可溶性化合物,烧水时Ca2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一.请写出Ca2受热分解的化学方程式: .
化学与生活息息相关,请你用所学化学知识解释以下生活中的问题。
(1)小明看到妈妈向洗衣服的水中加入 ,搅拌后泡沫 (填“多”或“少”),他认为这时的水为硬水。
(2)小明向一杯水中加入了一大块冰糖,水差点就洒出来了,过一会儿,他发现冰糖消失,液面下降了,这是说明分子具有 、 性质。
水是宝贵的自然资源,生命的孕育和维系需要水;人类的日常生活和工、农业生产离不开水。人类必须爱惜水—节约用水、保护水—防治水污染。
(1)下列做法不正确的是_________(填序号)
①用洗菜水冲厕所
②生活污水可任意排放
③农业和园林浇灌改大水浸灌为喷灌、滴灌
(2)自来水厂生产自来水的过程中,常加入__________,用来吸附水中的一些溶解性杂质,除去臭味。在吸附、沉淀、过滤、蒸馏四种净水方法中,_________的净化程度最高。
(3)某化工厂产生的废水中含有一定量的盐酸,不能直接排放到河流中,可向废水中撒入一定量的石灰石粉末对废水进行处理,发生反应的化学方程式为___________________________。