如图为实验室常用装置.

(1)写出仪器①的名称 .
(2)实验室用a装置制氧气,反应的化学方程式为 .
(3)a装置还可用于实验室制二氧化碳,反应的化学方程式为 ;将产生的气体通入澄清石灰水,若澄清石灰水 ,该气体为二氧化碳.
(4)若在实验室收集氢气,应选择的收集装置为 (填序号).
小科开展了二氧化碳的制取和部分性质实验:

(1)收集二氧化碳应选择图中 装置。
(2)小科采用图E方法检验二氧化碳的性质,观察到蜡烛熄灭。该现象除了能说明二氧化碳不能燃烧外,还能说明二氧化碳具有 的性质。
如图是初中化学实验室制取气体的一些装置图。根据要求回答问题。
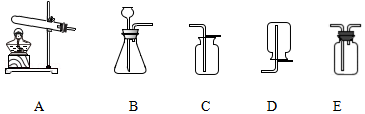
(1)实验室制取气体若选用A装置,除因为反应条件需要加热外,还因为 。写一个用A装置制取某气体的化学方程式 ,该气体可用C装置收集,检验是否收集满的方法是 ,证明该气体已收集满。
(2)气体X的密度比空气小,且不与酸反应,可由一种固体物质与水反应生成。要得到一瓶干燥的该气体,所选装置的连接顺序是 (填字母),可选用 做干燥剂。气体X在空气中燃烧的化学方程式为:2X+5O 2 4CO 2+2H 2O,则X的化学式是 。
某兴趣小组制取氧气,并尝试回收部分药品。可能用到的部分装置如图1。

(1)如图1中仪器a的名称是 。
(2)用双氧水和MnO2制氧气。发生反应的化学方程式为 ,收集氧气的装置可选用 (填字母)。
(3)加热KClO3固体制氧气(1.5g MnO2作催化剂),并对KClO3完全分解后的残留固体进行分离。(已知反应原理为:2KClO3 2KCl+3O2↑)
①发生装置应选用 (填字母)。
②KCl的溶解度曲线如图2所示。将残留固体冷却至室温(20℃),称得其质量为4.8g。欲将KCl全部溶解。至少应加入该温度下蒸馏水的体积约 (填字母)。

a.5mL
b.10mL
c.20mL
d.30mL
③对溶解所得混合物进行过滤,滤渣经处理得MnO2,从滤液中获得KCl晶体的最佳方法是 。
实验室用大理石和稀盐酸制取CO2,并用向上排空气法收集,可供选择的仪器如图。

(1)仪器E的名称是 ;
(2)组装整套装置时,可选用图中的A、B、H、I、J、L、P和 ;
(3)利用组装完毕后的装置制取CO2气体时,验满的操作是 ;
(4)若要制取8.8gCO2,理论上至少需要100g质量分数为 的稀盐酸;
(5)选择气体的制取装置时,需要考虑反应物的状态、 和气体的性质。
配制100g质量分数为15%的KNO3溶液,需要水 毫升(水的密度为1g/cm3)。在配制过程中量取水的体积时仰视读数,则所配制溶液的溶质质量分数 (选填“偏大”、“不变”、“偏小)。
配制50g质量分数6%的氯化钠溶液,结合实验回答下列问题。
(1)用托盘天平称量 g 氯化钠固体;
(2)溶解时需要用到的仪器是 和玻璃棒;
(3)下列操作中,会引起溶质的质量分数偏差的是 。
A. 称量读数时天平指针偏左 B. 量取水时仰视读数 C. 装瓶时洒出少量溶液。
台州甘蔗制糖有着悠久的历史。甘蔗制糖的部分环节为:清洗甘蔗→压榨甘蔗→分离渣汁→蒸发浓缩→……

(1)甘蔗在压榨过程中发生的变化属于 。
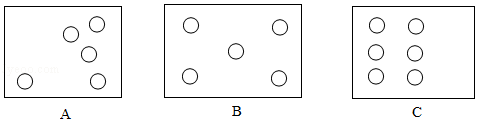
(2)渣汁的分离与图中的 (选填“A”、“B”或“C”)实验原理相同。
(3)糖汁在蒸发浓缩过程中,溶液的溶质质量分数将怎么变化? 。
化学实验要严格按操作要求进行,在横线上填写以下错误操作造成的后果:
(1)实验室用剩的药品放回原瓶:____________________。
(2)用量筒量取20mL水仰视读数,量取水的体积会________(填"偏大"或"偏小")。
(3)加热固体药品时,试管口向上倾斜:___________________________。
(4)将锌粒直接投入瓶口朝上且直立的试管中:____________________。
(5)滴管取用试剂后平放或倒置:_______________。
(6)倾倒细口瓶里的药液时,标签没向着手心:________________。
(7)用试管刷刷洗试管时,用力过猛:________________。
(8)给试管里的液体加热时,试管口对着人:________________________________。
根据下列装置,回答问题:

(1)写出图中标号①仪器的名称: 。
(2)实验室里常用H 2O 2和MnO 2来制取O 2,应选用的发生装置为图中的 。(填字母)
(3)实验室若用装置D收集H 2,则气体应从导管 (填"a"或"b")端进入。
(4)工业常需分离H 2、CO 2的混合气体。某同学采用装置E也能达到分离该混合气体的目的。操作步如下:
步骤1:关闭活塞B,打开活塞A,通入混合气体,可收集到 。
步骤2;然后, (填操作),又可收集到另一种气体。
2020年年初新冠状病毒在我国传播扩散,给我们的生命健康和生产带来严重影响。预防新冠状病毒的主要措施有戴口罩、勤洗手、养成良好饮食习惯、减少聚集等。在抗击新冠状病毒的过程中,我们也学到了不少防疫新冠状病毒的知识。
(1)医用口罩。
医用口罩是由三层无纺布做成的。中间一层用来隔离病毒的喷熔无纺布的材料是聚丙烯。聚丙烯和聚乙烯一样都属于 高分子材料(选填“合金”“复合”“合成”“天然”)。口罩隔离病毒相当于化学实验操作中的 (填写实验操作名称)。
(2)良好的饮食习惯。
营养要全面、均衡。要多吃富含蛋白质、维生素以及矿物质的食物,比如肉、蛋、奶类、新鲜的水果和蔬菜以及坚果等。
樱桃是人们喜爱的一种水果,富含糖类、蛋白质、维生素(A、B、C等)、矿物质(钙、磷、铁等),具有很高的营养价值。樱桃所含的营养成分中,能够提供能量的是 、蛋白质。樱桃中含有的钙、磷、铁等,是指 (填“分子”“原子”“元素”)。
(3)正确使用消毒液。
某品牌消毒液的有效成分主要是乙醇(体积分数72%﹣82%)、过氧化氢(0.10%﹣0.14%( ))。乙醇俗名 ,乙醇消毒液在使用过程中要特别注意远离火源,其原因是乙醇具有挥发性、 性,请写出乙醇燃烧的化学方程式 。
洁厕灵(含HCl)、84消毒液(含NaClO)是生活中两种常见的清洁、消毒用品;两者混合使用时会发生化学反应(2HCl+NaClO═NaCl+H2O+Cl2↑),生成有毒物质,因此禁止将两者混合使用!下列说法正确的是 。
A.Cl2是有毒气体
B.洁厕灵可以用铁质容器盛放
C.洁厕灵可用于清洁大理石台面
D.室内喷洒84消毒液后,会嗅到刺激性气味,是因为微粒在不断运动
E.口服84消毒液可以预防新冠状病毒
某同学要在一块空地上种植作物,于是对这块空地的土壤酸碱度进行测定。
(1)在空地上确定5~6个位置进行取样测定土壤酸碱度。以下三种取样位置设定合理的是 。
(2)将采集到的土样进行处理后,用玻璃棒蘸取土壤浸出液,滴在 上,将其呈现的颜色与标准比色卡比色,确定了空地土壤的pH约为7.查阅资料,常见作物最适宜生长的土壤pH范围如下表,则这块空地上适合种植的作物有 。
作物 |
大蒜 |
丝瓜 |
茄子 |
沙枣 |
最适pH范围 |
5.6~6.0 |
6.0~6.5 |
6.8~7.3 |
8.0~8.7 |
碳酸钠俗称纯碱或苏打,在生活、生产和实验研究中均有广泛应用。
[配制溶液]配制溶质质量分数分别为1%、2%和4%的Na2CO3溶液
(1)若配制50g溶质质量分数为4%的Na2CO3溶液,下列操作正确的是 (填字母)。
a.用托盘天平称取2g Na2CO3固体
b.选用50mL量筒量取所需体积的水
c.选用带玻璃塞的广口试剂瓶,将配好的溶液装瓶并贴标签
(2)分别测定25℃时,上述3种溶液的pH,记录数据如下:
实验编号 |
Ⅰ |
Ⅱ |
III |
溶质质量分数 |
1% |
2% |
4% |
溶液pH |
11.62 |
11.76 |
11.90 |
分析Ⅰ、Ⅱ、Ⅲ三组数据可得出的结论是 。
[制备物质]用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3
[已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀]
(3)在烧杯中制备FeCO3沉淀时,应选用的加料方式是 (填字母)。
a.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
b.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
c.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
(4)潮湿的FeCO3固体置于空气中易变质,反应如下:4FeCO3+6H2O+O2═4X+4CO2.则X的化学式为 。
[标定浓度]标定待测盐酸的溶质质量分数
(5)将Na2CO3固体在270℃干燥至恒重,准确称取0.212g无水Na2CO3于锥形瓶中,加入50mL蒸馏水溶解,滴入待测盐酸,当两者恰好完全反应时,消耗盐酸的体积为20.00mL(该盐酸的密度近似等于lg•mL﹣1,反应中Na2CO3所含的碳元素全部转化为CO2)。
①列式计算待测盐酸的溶质质量分数(结果用百分数表示,保留两位小数)。
②若上述测定过程中Na2CO3固体未经充分干燥,则测出盐酸的溶质质量分数将 (填“偏大”、“偏小”或“无影响”)。
某同学以高锰酸钾为原料制取氧气。
(1)用如图方法检查装置的气密性,使劲捂住试管却仍观察不到导管口有气泡冒出。若此装置气密性良好,为顺利完成该装置的气密性检查,提一条合理建议 。
(2)清洗试管时,试管中的固体物质溅落在衣服上,留下了黑点,用彩漂液(主要成分是过氧化氢)清洗,黑点处迅速产生气泡,请用化学反应方程式表示气泡产生的原因 。

水是一切生物生存所必需的,我们应该了解有关水的一些知识。
(1)为了防止水的污染,下列做法有利于保护水资源的是 (填编号);
①抑制水中所有动、植物的生长 ②不任意排放工业废水
③大量使用化肥农药 ④生活污水净化处理后再排放
(2)有一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气(Cl2),该反应的化学方程式为 ;从能量变化角度看,该反应将电能转化为 能;
(3)在化学实验和科学研究中,水也是一种常用的试剂。极少部分水分子在特定条件下容易解离而得到H+和OH﹣,H+易与水分子形成水合氢离子(H3O+),与水分子相比,下列对水合氢离子描述不合理的是 (填字母序号);
A.氧元素的化合价发生了改变 B.微粒的构成发生了改变
C.微粒的化学性质发生了改变 D.微粒的电子数发生了改变
(4)溶液在生产和生活中有广泛的应用。某同学配制溶液时,在用量筒量取所需水的过程中,他俯视读数,这样配制得到的溶液溶质质量分数会 (填“偏大”、“偏小”或“无影响”)。