(14分)归纳与演绎是重要的科学方法,也常用于化学的学习.请根据下列实验装置,回答问题:
(1) 我们已经学过实验室制取氧气、二氧化碳两种气体的反应原理、制取与收集方法,请你归纳出实验室制取这两种气体反应的共同点 (填序号).
| A.需要加热 | B.需用催化剂 | C.没有气体参加反应 | D.生成的气体只有一种 |
(2) 用高锰酸钾制取氧气可选用发生装置是__ _(填序号),反应的方程式__ ;
(3) 装置B中反应的方程式为__ _;要随时使反应停止或发生可选择的发生装置有______ ____(填序号,从A-E中选择);若用E和G组装一套气密性好的装置来测定二氧化碳的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏小得多,原因是二氧化碳_____ _____.
(4) 若用双氧水和二氧化锰制取氧气且能获得平稳的气流,可选择的发生装置有__ (填序号),方程式是_______ __;若用C和G组装一套气密好的装置来测定氧气的体积,反应结束后,发现量筒内收集到的水的体积总是比理论值偏大(水的体积测量准确),其主要原因是 .
(5) 化学上可通过多种反应得到氨气(极易溶于水,密度比空气小),例如:
① 氯化铵(固) + 氢氧化钙(固) 氯化钙 + 氨气+ 水
氯化钙 + 氨气+ 水
② 碳酸氢铵(固) 氨气+二氧化碳+水
氨气+二氧化碳+水
结合以上实验装置完成下列填空(以下均填序号): 你选择上述反应 作为实验室制取氨气的反应原理,选用上图中A~H的 作为反应的发生装置,采用的收集装置是F和H,其中氨气应从_ 管导入(填a或b)F中,H中用倒置漏斗比直接用导管通入水中吸收氨气的优点是 .实验室中漏斗的其它用途 (写一种)
已知铜可以和浓硝酸发生如下反应:Cu + 4HNO3(浓) = Cu(NO3)2 + 2H2O + 2NO2↑,实验室可以通过该反应制取二氧化氮气体。NO2是一种红棕色气体,密度比空气大,能和水反应。NO和NO2都是空气的污染物。现给出下列装置: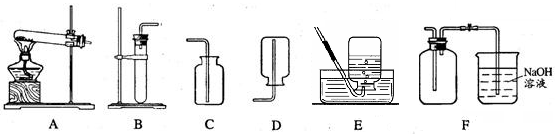
(1)某同学做该实验时,有失去标签的浓硝酸和浓盐酸,如何区分出浓硝酸?
(2)制取NO2的发生和收集装置应分别选用 和 。请写出利用你选择的发生装置制取另一种气体的反应方程式。
(3)随着反应的进行能产生NO气体,请解释可能的原因?
(4)已知NO密度比空气略大,难溶于水,NO能与氧气反应生成NO2,应选用装置 收集NO,并写出NO和氧气反应的化学方程式。
(5)某同学做完实验后,为回收废液中的金属铜,向废液中加入28g铁屑,恰好完全反应。请计算回收到的铜的质量。
实验室选用下图所示装置制取和收集气体,根据要求回答下列问题。
(1)指出标号①的仪器名称 。
(2)实验室用B装置制取氧气时,有关的化学反应方程式: 。
(3)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择 (填序号)。
(4)写出一个用装置A 、C装置连接制取气体的化学方程式 。
根据下列实验装置图,回答有关问题。
(1)指出编号仪器名称:① ,② 。
(2)实验室利用A装置可制取氧气,反应的化学方程式为 。
(3)实验室制取并收集氢气应选择的装置是 (从A~E中选择),反应的化学方程式为 ,使用该套装置制取气体的优点是 ,若用F装置收集氢气,则气体应从 端进入。
某学习小组围绕"气体的实验室制取"进行研讨,请你参与完成下面的问题。
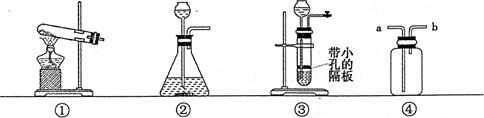
(1)图①装置制取气体的适用条件是。
(2)图③装置相比图②装置的主要优点是。
(3)实验室不宜用镁来代替锌与稀
反应制取
,主要原因是。
(4)实验室若用图④装置收集
时,气体应从端通入。(填字母)
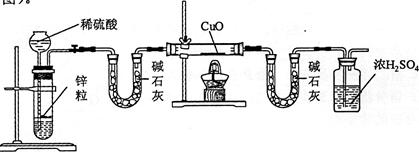
(5)为了测定铜元素的相对原子质量
,某同学以氢气还原氧化铜的反应设计了:上图中第一个装有碱石灰的
形管的作用是。
若测得反应前氧化铜的质量为
,实验完成后第二个装有碱石灰的
形管增加的质量为
,则
=。(用
表示)。
(6)请利用单孔橡胶塞、玻璃导管、胶皮管、试管、集气瓶和玻璃片,设计一套制取
的实验装置,并将该实验装置的简图画在答题卡的方框内。

如下图所示为实验室中常见气体制备、净化、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。某学校
两个化学实验探究活动小组的同学欲用它昂们完成各自的探究实验。
(1)第一组的同学以石灰石和稀盐酸为原料,在实验室制备、收集干燥纯净的二氧化碳气体,按照要求设计实验装置、连接仪器,并检验装置的气密性。(提示:挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收)
①所选仪器的连接顺序为________→_______→________→________(填写仪器序号字母)。
②写出实验室制取二氧化碳的反应方程式_____________________________________。
③检验集气瓶中气体是否为二氧化碳的具体方法________________________________
_________________________________________________________________________。
(2)第二组的同学以过氧化氢溶液为原料(MnO2为催化剂)制备氧气,并对某种尼龙材料的组成元素进行分析探究。资料显示该尼龙材料一定含C、H、N三种元素。
所选仪器按“A→B1→E→B2→D→碱石灰干燥管”的顺序连接,(B1、B2为浓硫酸洗气瓶),实验前检验装置气密性。使该塑料试样碎屑在纯氧气中充分燃烧,观察现象,收集有关实验数据(假设发生的化学反应都充分反应)。试回答下列问题
仪器A中所发生反应的化学方程式________________________________________。
仪器D中的明显现象是__________________________________________________。
③仪器E中玻璃管中放入的尼龙试样碎屑质量为3.5g,塑料试样充分燃烧后,测得仪器B2的质量增加3.6g,则该塑料试样中H元素的质量分数为________。(结果保留一位小数)
④若装置中没有连接仪器B1,这样测算出的该塑料试样中H元素的质量分数与实际值比较将_______(填“偏小”“偏大”“基本一致”之一)。
化学兴趣小组在实验室进行关于气体的实验,所用的部分装置如下图所示。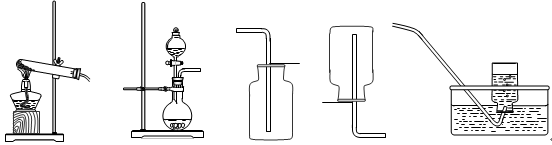
A B C D E
(1) 甲同学用双氧水制取氧气,发生反应的化学方程式是 ,选择的收集装置是C或 ,用 置于集气瓶口检验C收集满氧气。
(2) 乙同学用氯酸钾和二氧化锰为原料制取氧气,二氧化锰的作用是 ,应选择的发生装置是 。该同学发现产生的气体能使带火星的木条复燃并有刺激性气味,下列分析不合理的是 。
a.反应中氧气的物理性质发生了变化 b.此时得到的气体一定是混合物
c.只加热氯酸钾,若生成的气体无气味,说明刺激性气味一定与二氧化锰有关
d.可能是生成的氧气与残留在发生装置中的空气在加热的条件下反应生成了新物质
(3) 丙同学研究了木条复燃与氧气体积分数的关系,发现不纯的氧气也能使带火星的木条复燃。下图F是他其中一次实验的装置,集气瓶中有约占总体积40%水,氧气从 (填“a”或“b”)导管口进入,排尽集气瓶中的水,收集氧气后集气瓶中氧气的体积分数是 。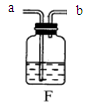
(4) 下图G装置也可制取二氧化碳气体。G装置的优点是可随时控制反应的发生和停止。若打开弹簧夹,固体与液体接触,反应便能发生,请简述使G装置中反应停止的操作 。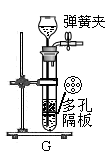
下图A、B、C是实验室制备某些常见气体的发生装置示意图。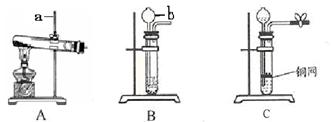
(1)写出图中标号仪器的名称:
a , b 。
(2)A可用作实验室制取氧气的化学方程式是 。
(3)B可用作实验室制取二氧化碳的化学方程式是 。
(4)下列装置可用来进行“排空气法”收集H2的是 (填序号)。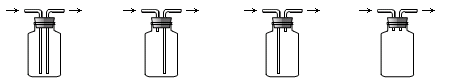
A. B. C. D.
(5)某同学在装置B的基础上,增加了隔离铜网和止水夹等改成装置C来制取二氧化碳,装置C与B相比,突出优点是 。
(6)取石灰石与稀盐酸充分反应后的溶液A, 向其逐滴加入碳酸钠溶液,并用pH数字探测仪连续监测,得曲线如下(pH为纵坐标,时间为横坐标)。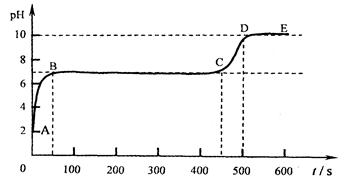
①写出BC段相关的化学方程式是 。
②CD段上升的原因是 。
③小红取溶液A50 g,逐滴加入某质量分数的碳酸钠溶液。他根据实验测得的数据绘出下图,其中纵坐标m是实验得到的沉淀的质量,横坐标表示的是碳酸钠溶液质量。由图像回答下列问题: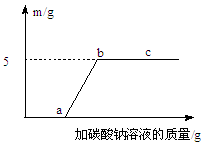
(Ⅰ)原废液中含氯化钙的质量为 g。
(Ⅱ)C点时的溶液中溶质含 。(填化学式)
(11分)下图列出了实验室里一些实验装置,请回答有关问题: 

(1)装置C由导管、集气瓶和 (填仪器的名称)组成。
(2)实验室用H2O2和MnO2制取O2的化学方程式为 ,选用的发生装置是 (填序号,下同);若用KClO3和MnO2制取O2,则选用的发生装置是 ,收集装置可用 。
(3)实验室制取二氧化碳的化学方程式为 ,二氧化碳气体通入E中,看到的现象是: 。用石灰石和稀盐酸制取二氧化碳时,选用的发生装置是 ,当不再有气泡逸出后,测得反应残留液的pH如图中a点所示,再向残留液中逐渐滴入碳酸钠溶液,并连续精确测定溶液的pH,溶液pH随时间的变化如图曲线所示(纵坐标:pH,横坐标:时间)。
请写出bc段发生反应的化学方程式: , cd 段上升的原因是: 。
(4)实验室制取H2时,若选用装置D收集H2,则应从 口进气(填x或y)。
化学实验是科学探究的重要途径。请根据下列实验图示回答相关问题:
(1)A实验中,烧杯③的作用是 。
(2)B实验中,硬质玻璃管中的现象是 ;装置末端酒精灯的作用是 。
(3)C实验中,若要除去粗盐中难溶性的杂质,其正确操作步骤为 (填序号);若按照②③①的步骤配制50 gl6%的氯化钠溶液,所配制溶液的溶质质量分数
(填“偏小”或“偏大”)。
登山运动员常利用氢化钙固体作为能源提供剂,在需要时与水反应生成其他物质和氢气,提供燃料。某兴趣小组用纯净干燥的氢气和金属钙制取氢化钙,所选装置图如下:
A B C D E
查阅资料:(1)钙易与水反应生成碱和气体。
(2)无水氯化钙能作干燥剂。
(1)请写出E图中仪器①的名称 。
(2) 请按气流方向连接顺序i接(),()接(),()接(),k接 a
(填仪器接口的字母编号)。写出C中可能发生的化学方程式 。
(3)实验结束后,某同学取少量生成物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色。该同学据此判断,上述实验的确有CaH2生成。另一位同学认为该同学的判断不准确,原因是 。
(4)氢化钙作为能源提供剂,与直接用氢气相比,其优点是
某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如下图所示,请回答有关问题:


实验进行一段时间之后,A玻璃管内观察到的现象是
B装置中氢氧化钠溶液的作用是。
为避免将
排放到空气中,并回收利用
,方框中连接的是C和D装置,导管接口的连接顺序应为a→除
外,还有氢气等物质可以还原
,某同学设计了用金属锌粒与稀硫酸反应制取氢气的实验装置,如右图所示:
①制取氢气的反应方程式为②用E和F装置制取二氧化碳,F装置与E装置比较,优点是
某化学研究性学习小组进行了氨(
)的制取和有关性质的探究实验。
资料卡片:氨气通常情况下是有刺激性气味的无色气体,密度比空气小,能使湿润的红色石蕊试纸变蓝色,极易溶于水,浓氨水具有挥发性。加热熟石灰和氯化铵固体混合物可以生成氨气,若要快速产生氨气,可以将浓氨水滴加到生石灰中得到。

请根据有关信息回答下列问题:
(1)仪器a的名称是。
(2)利用A装置制取氨气的化学方程式是。
(3)将浓氨水滴加到生石灰中快速产生氨气,发生装置最好是(选填装置编号)。
(4)研究性学习小组用D装置收集氨气,判断氨气已经收集满的方法是。
(5)研究性学习小组用下图所示的装置探究氨的性质,观察到脱脂棉团由白色变为红色。该现象涉及到的性质是(填字母编号)。

| A. |
氨分子是不断运动的 |
B. |
浓氨水具有挥发性 |
C. |
氨气有刺激性气味 |
D. |
氨气的水溶液显碱性 |
(6)若将制取氨气的熟石灰溶于水形成的饱和溶液置于小烧杯并放入一只大烧杯中(如下图),在大烧杯中加入下列物质,观察到小烧杯中饱和溶液变浑浊,则加入的物质是(填字母编号)。

| A. |
水和浓硫酸 |
B. |
水和氯化钠固体 |
C. |
水和硝酸铵固体 |
D. |
水和氢氧化钠固体 |
如果配制6%的氯化钠溶液的溶质质量分数偏小,其原因是
| A. | 称取的氯化钠固体质量偏大 |
| B. | 转移称量好的氯化钠同体时,有少量洒落在桌面上 |
| C. | 量取水的体积偏小 |
| D. | 转移配制好的溶液时,有少量液体溅出 |