[广东]2014年初中毕业升学考试(广东省佛山卷)化学
2013年佛山启动了"生活垃圾分类"试点活动,对提升城市文明和生活质量具有积极的意义。下列各图为城市生活垃圾分类标志,则废旧电池属于()
| A. |
可回收垃圾 |
B. |
餐厨垃圾 |
| C. |
有害垃圾 |
D. |
其他垃圾 |
佛山西樵山是岭南名山,有"天然氧吧"之美誉.山林里空气中的自由电子附着在氧分子上形成负氧离子( ),被称为"空气维生素". 的相对分子质量是()
| A. | A.16 | B. | B.32 | C. | C.32g | D. | D.33 |
生活中常用的不粘锅,其内衬用的一种材料叫聚四氟乙烯。该材料属于( )
| A. | 金属材料 | B. | 纳米材料 | C. | 复合材料 | D. | 有机合成材料 |
磁悬浮列车给城镇交通带来了极大的方便,其所用超导材料需在低温环境下才能发挥作用。下列用于磁悬浮列车的气体是()
| A. | B. | C. | D. |
认识物质及其变化对把握自然规律至关重要。下列与其它物质变化类型不同的一项是()
| A. |
|
B. |
|
| C. |
|
D. |
|
化学物质给生活带来了极大的便利,也使我们的生活变得丰富多彩。下列物质有关应用错误的是()
| A. | 金刚石:用于裁玻璃 | B. | 明矾:用于净水 |
| C. | 烧碱:用于食用碱 | D. | 氯化钠:用于配制生理盐水 |
视黄醇对治疗夜盲症有重要的作用,化学式可表示为 ,相对分子质量为286。下列有关视黄醇的说法中正确的是()
| A. | 视黄醇属于无机化合物 |
| B. | 视黄醇的化学式中X=2 |
| C. | 视黄醇中碳元素与氢元素的质量比为2:3 |
| D. | 视黄醇中氢元素的质量分数约为10.5% |
柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出来H+,从而呈现酸性,主要用于香料或作为饮料的酸化剂。下列物质不能与柠檬酸反应的是( )
| A.Mg | B.Fe2O3 | C.C02 | D.NaOH |
在实验事实的基础上归纳结论,是化学学习的重要思想和方法。下列有关金属活动性实验探究的归纳和总结中不科学的是( )
| A. | 镁与氧气在常温下就能反应,而铁与氧气在高温时才能反应,故镁比铁活泼 |
| B. | 锌粒与盐酸反应比铁片与盐酸反应要剧烈,故锌比铁活泼 |
| C. | 铝能与盐酸反应放出氢气,而铜不能与盐酸反应,故铝比铜活泼 |
| D. | 铜与硝酸银溶液反应得到银,故铜比银活泼 |
化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的。下列实验操作或设计中正确的是()
| A. |
|
B. |
|
C. |
|
D. |
|
下列有关概念的辨析中正确的是( )
①分子是保持所有物质化学性质的最小微粒; ②催化剂一定能加快化学反应的速率;
③元素的种类是由原子的中子数决定的; ④由一种元素组成的物质可能是混合物;
⑤合金在化学性质上不再具备金属的特性; ⑥水溶液呈碱性的物质不一定是碱。
| A. | ①④ | B. | ②③ | C. | ④⑥ | D. | ⑤⑥ |
某同学在探究"酸与碱能否发生反应"时,用稀NaOH溶液、稀盐酸和酸碱指示剂进行实验的过程见下图。下图所加试剂①②③分别是( )

除去下列物质中的少量杂质。所选用的试剂及操作方法均正确的是
| 选项 |
物质(括号内为杂质) |
试剂 |
操作方法 |
| A |
铁粉(焦炭) |
稀硫酸 |
过滤 |
| B |
气体(水蒸气) |
生石灰 |
干燥 |
| C |
固体(
) |
足量的水 |
溶解、过滤、蒸干 |
| D |
固体(
) |
过量稀盐酸 |
蒸干 |
在一定质量表面被氧化的镁条中,慢慢加入一定浓度的盐酸,反应中有关量的变化情况描述正确的是()
| A. |
|
B. |
|
| C. |
|
D. |
|
下图为
的溶解度曲线图,现有M状态下的
溶液65
,若要将该溶液经过处理后,刚好得到该温度下的饱和溶液,下列处理方法正确的是( )

| A. | 在 时,将65 溶液倒出去32.5 |
| B. | 将65 溶液蒸发掉32.5 的水,再冷却到 |
| C. | 在 时,向65 溶液中加入15 固体并充分溶解 |
| D. | 将65 溶液的温度从 降低到 |
在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示。
下列有关说法正确的是( )
| 物质 |
a |
b |
c |
d |
| 反应前的质量/ | 30 |
20 |
10 |
15 |
| 反应后的质量/ | x |
y |
O |
10 |
| A. |
参加反应的c与d的质量比为 |
| B. |
|
| C. |
当 时,该反应一定是化合反应 |
| D. |
x的取值范围: |
(6分)在“宏观—微观—符号”之间建立联系,是学习化学的一种重要思维方式。下图是元素周期表中部分元素的原子结构示意图,根据所学知识回答下列问题。
(1)上图四种元素中,属于非金属元素的是 (填元素符号)。
(2)2个镁离子的符号为 ,铝原子的核电荷数X为 ,硅的氧化物的化学式为 。
(3)相对原子质量与原子真实质量之间存在紧密的关系(见下表),根据下表判断6.02×1023个钠原子的质量y为 。请归纳下表中的规律:
。
| |
碳 |
氧 |
钠 |
| 相对原子质量 |
12 |
16 |
23 |
| 6.02×1023个原子的质量 |
12g |
16g |
y |
氨水(
)也是常见的碱,是由
溶于水形成的溶液。氨水很不稳定,容易放出有刺激性气味的
。根据所学知识回答:
(1)
在水溶液中解离出来的离子有。
(2)打开装有氨水的试剂瓶后闻到刺激性气味,说明分子。
(3)写出
与稀
反应的化学方程式。
(4)将一片有酚酞的干燥纸条和一片有酚酞的湿润纸条分别放入两瓶干燥的
中,现象是:
。
 (5)
在一定的条件下能跟
反应,反应过程可用下列示意图表示(注: 表示氮原子,●表示氧原子,
表示氢原子;各物质未配平)。请分析在该反应中参加反应的
与
的分子个数之比为。
(5)
在一定的条件下能跟
反应,反应过程可用下列示意图表示(注: 表示氮原子,●表示氧原子,
表示氢原子;各物质未配平)。请分析在该反应中参加反应的
与
的分子个数之比为。

酱油是中国的传统调味品,佛山海天酱油享誉国内外。下表是某酱油膏的部分营养成分列表,根据所学知识回答。
酱油膏的部分营养成分列表(每100克中含)
| 成分名称 |
含量 |
成分名称 |
含量 |
成分名称 |
含量 |
| 水分(克) |
54.7 |
蛋白质(克) |
13 |
脂肪(克) |
0.7 |
| 糖类(克) |
10.2 |
钠(毫克) |
7700 |
钙(毫克) |
46 |
| 铁(毫克) |
8.6 |
硒(微克) |
2.96 |
(1)上表中不含六大基本营养素中的。
(2)上表中"钠"、"钙"等是指(填"单质"、"分子"、"原子"或"元素")。
(3)老年人每天都要摄入足量的钙,有利于防止。
(4)糖类主要是给人体提供能量。写出葡萄糖(
)在酶作用下缓慢氧化的化学方程式。
(5)人体缺硒可能引起表皮角质化和癌症,但摄入量过高又会使人中毒。这里告诉人们的道理是。
(7分)过氧化钙(CaO2)难溶于水,常温下稳定,在潮湿空气及水中缓慢放出氧气,广泛应用于渔业等领域。下图是以大理石(含Al2O3及其他不溶于水也不溶于酸的杂质)等为原料制取CaO2的流程图:

(1)操作a、b、c的名称都是 。
(2)操作a的目的是 。
(3)从滤液C中可回收的副产品的化学式为 。
(4)写出反应①的化学方程式 。
(5)反应②的基本反应类型是 。
(6)在该生产过程中,用110kg大理石制得了72Kg的过氧化钙。如果不考虑过程中的损耗,可计算出大理石中CaCO3的质量分数为 。(结果保留一位小数)
是初中化学常见物质。其中,
的浓溶液能挥发出刺激性气味的气体,从
的反应过程中有蓝色沉淀生成,
为白色沉淀。下图是这些物质的转化关系,部分反应物、生成物及反应条件已省略。

(1)请写出化学式:
(2)写出
的化学方程式:
(3)在
的反应过程中,
与
溶液恰好完全反应,反应后所得溶液的
(4)
溶液与铁粉反应后,取剩余固体加入盐酸,没有气体放出。请分析:
与铁粉反应后的溶液组成中除了
外,一定存在的物质有
氧气的化学性质比较活泼,能支持燃烧。下图是木炭在氧气中燃烧实验示意图,

对该实验进行分析并回答。
(1)图①中仪器
的名称是。
(2)从燃烧条件的角度分析,图②加热木炭的目的是。
(3)图②中熄灭酒精灯的操作是。
(4)图③中木炭在氧气里燃烧比在空气里燃烧要剧烈,说明了。
(5)图④在整个实验设计中的意图是。
某学习小组围绕"气体的实验室制取"进行研讨,请你参与完成下面的问题。
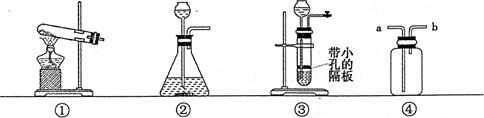
(1)图①装置制取气体的适用条件是
(2)图③装置相比图②装置的主要优点是
(3)实验室不宜用镁来代替锌与稀
反应制取
,主要原因是
(4)实验室若用图④装置收集
时,气体应从
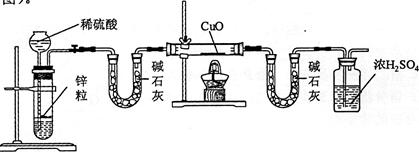
(5)为了测定铜元素的相对原子质量
,某同学以氢气还原氧化铜的反应设计了:上图中第一个装有碱石灰的
形管的作用是
若测得反应前氧化铜的质量为
,实验完成后第二个装有碱石灰的
形管增加的质量为
,则
=
(6)请利用单孔橡胶塞、玻璃导管、胶皮管、试管、集气瓶和玻璃片,设计一套制取
的实验装置,并将该实验装置的简图画在答题卡的方框内。

地球上的金属资源广泛地存在于地壳和海洋中,工业上主要是从含有金属元素并有开采价值的矿石中提炼金属。
(1)赤铁矿在自然界中储藏丰富,其主要成分的化学式是。
(2)磁铁矿的主要成分是
。在
中存在两种不同价态的铁离子,其中1/3是
,2/3是
。请写出
与盐酸反应的化学方程式。
(3)工业上主要采用高炉炼铁,常用到的原料有铁矿石、焦碳、石灰石和空气。其中,焦碳的作用是。(仅答一点)
(4)由于铁的氧化物中
和
均为黑色,实验室用
还原
得到的铁中是否会含有
和
,某同学设计了下列探究实验。
资料:
溶液与铁发生的反应是2
,但
溶液不与
、
反应;含有
的盐溶液遇到
溶液时变成红色,利用该反应可检验
的存在。
【提出问题】
还原
得到黑色产物的成分是什么?
【猜 想】
猜想l:
猜想2:
和
;
猜想3:
和
; 猜想4:。
【实验探究】限选试剂:
、盐酸、澄清石灰水、
溶液、
溶液。
| 实验操作 |
实验现象 |
实验结论 |
| Ⅰ取少量黑色产物加入到装有足量
溶液的烧杯中,充分反应后过滤,对过滤所得固体用蒸馏水洗涤。 |
黑色固体部分溶解。 |
猜想2和4都 不成立。 |
| Ⅱ ,,. | 黑色固体全部溶解,溶液 不变红色。 |
|
| Ⅲ另取少量黑色产物装入玻璃管中,通入
,一段时间后加热,并将反应后的气体通入装有一定量的的烧杯中。 |
。 |
猜想l不成立, 猜想3成立。 |
硝酸铵(
)是常用的一种氮肥,对促进植物茎、叶生长茂盛,叶色浓绿,提高植物蛋白质含量等有作用。请回答下列问题:
(1)
中含有
,则
中氮元素的化合价为。
(2)与80g硝酸铵具有相同肥效的尿素【
】的质量为。
(3)硝酸铵不能与碱性肥料一起施用,因为铵盐能与碱发生反应而失效。在化学方程式
_____中,_____的化学式为。
(7分)菱镁矿的主要成分是
,为了分析某菱镁矿中镁元素的含量,某学习小组进行了实验研究。取10g菱镁矿,逐渐加入未知浓度的
溶液,生成的气体全部用
溶液吸收,
溶液增加的质量记录如下表:
| 加入
溶液的质量/g |
50 |
100 |
150 |
200 |
|
溶液增加的质量/g |
2.2 |
4.4 |
4.4 |
4.4 |
说明:菱镁矿中的杂质不溶于水,不与酸发生反应。.
(1)10g菱镁矿与
溶液完全反应,生成
的质量为
(2)计算该菱镁矿中镁元素的质量分数。(写出计算过程)

(3)该实验研究中所用
溶液的溶质的质量分数是
(4)为避免溶液排放对环境的影响,某同学对上述反应后溶液进行了过滤,并在滤液中加入了l.71%的
溶液。请你画出加入
溶液的质量与产生沉淀的质量的关系图。(在答题卡的坐标中作图,并标出曲线折点的坐标)




 对着干燥的玻璃片哈气
对着干燥的玻璃片哈气 浓硫酸腐蚀纸张
浓硫酸腐蚀纸张 用合金在纯金属上刻画
用合金在纯金属上刻画 胆矾的研碎
胆矾的研碎








 粤公网安备 44130202000953号
粤公网安备 44130202000953号