如图所示A—G是初中化学常见的物质。图中“→”表示转化关系,“—”表示相互能反应。已知A是人体胃液中含有的酸,G是最轻的气体,B、C、D、E、F都是氧化物。请回答: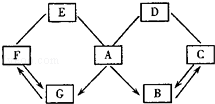
(1)G的化学式为__________。
(2)E与F发生化学反应的基本类型是__________,写出物质A的一种用途__________;
(3)A、D发生反应的化学方程式可能为_________。
7.0g含杂质的铁粉样品与足量稀硫酸反应,产生氢气的物质的量与时间关系如图所示(杂质不与酸发生反应)。计算样品中所含铁的质量分数(根据化学方程式列式计算)。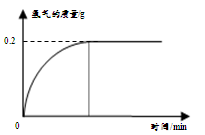
实验室里有一瓶长期暴露在空气中的氢氧化钠固体,某化学兴趣小组对其进行了如下探究。
(1)确定固体的成分。
【提出猜想】猜想Ⅰ:固体中只含碳酸钠;
猜想Ⅱ:固体中只含氢氧化钠;
猜想Ⅲ:固体中含有 。
【进行实验】
| 实验步骤 |
实验现象 |
实验结论 |
| ①取少量固体溶于水,加入 ; |
产生白色沉淀 |
猜想Ⅲ成立 |
| ②将上述反应后的混合液过滤,取少量滤液,加入 。 |
|
(2)测定固体中碳酸钠的质量分数。
【查阅资料】二氧化碳几乎不溶于饱和碳酸氢钠溶液中。
【进行实验】取2g固体,在25℃、101kPa下用如图所示装置进行实验,步骤如下: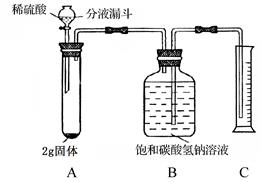
①连接好装置并检查气密性;
②装入药品,通过分液漏斗滴加足量稀硫酸后,关闭分液漏斗活塞;
③充分反应后,恢复至25℃、101kPa,量筒中液体的体积为220mL。
【实验分析】
①装置B中的饱和碳酸氢钠溶液不能用水代替,原因是 。
②充分反应后,装置A中残留的的二氧化碳对实验结果是否有明显影响? (选填“有”或“没有”)。
③已知在25℃、101kPa下二氧化碳的密度为1.8g/L,则固体中碳酸钠的质量分数为 (结果保留至0.1%)。
(3)除去固体中的碳酸钠。
【进行实验】实验流程如下图: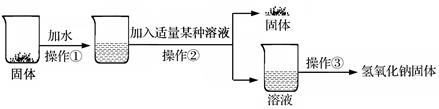
【实验分析】该流程中发生反应的化学方程式为 。
操作①、②、③均需用到的一种仪器是 。
Na2CO3中往往会含有少量的NaCl,现在一烧杯中盛有20.4g的固体混合物,向其中逐渐滴加溶质质分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题: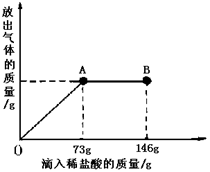
①当滴加稀盐酸至图中B点时,烧杯中溶液的pH 7(填>、=、<)。
②当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数。(计算结果保留一位小数)
某碳酸钠样品含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配制成
溶液,将其全部加入到
一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质量是
,将溶液蒸干,得到
硫酸钠。
计算:
(1)加入的硫酸溶液的溶质质量分数;
(2)原碳酸钠样品中碳酸钠的质量分数(计算结果精确到0.1%)。
某兴趣小组的同学为探究实验室久置的氢氧化钠固体的成分,进行了有关实验,请你与他们完成以下探究:
【提出猜想】猜想I:全部是氢氧化钠;猜想II:全部是碳酸钠;猜想III:_________________。
【实验验证】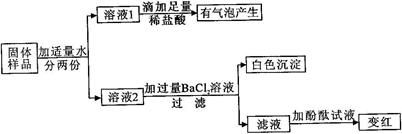
(1)请完成猜想III;
(2)溶液1中加足量稀盐酸,产生无色、无味的气体,说明原固体中含有_________;
(3)溶液2中滴加过量BaCl2溶液的目的是____________________________,反应的化学方程式为 。
(4)由以上实验现象可知猜想_______正确;
(5)久置的NaOH固体变质的原因是(用化学方程式表示)____________________。
用括号内物质不能一次性鉴别下列各组物质的是
| A.CaO、CaCO3、KCl三种固体(水) |
| B.CaCl2、K2CO3、K2SO4三种溶液【Ba(OH)2溶液】 |
| C.Cu、Fe、CuO三种固体(稀盐酸) |
| D.NaCI、Ca(OH)2、HCI三种溶液【K2 CO3溶液】 |
下列图像与所对应操作相符的是.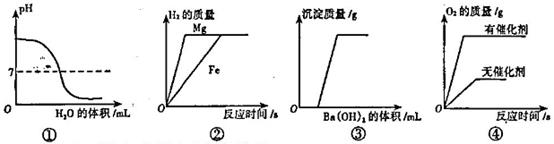
| A.①是对氢氧化钠溶液加水稀释 |
| B.②是将镁片和铁片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合 |
| C.③是向HCI与Na2 SO4泥合溶液中加入Ba (OH)2溶液 |
| D.④是用等质量、等浓度的双氧水分别制取氧气 |
某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如下图所示。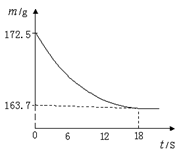
求:(1)计算碳酸钠中各元素的质量比:Na:C:O= 。
(2)碳酸钠的相对分子质量为: 。
(3)生成CO2的质量。
(4)该纯碱样品中Na2CO3的质量分数。
请你参与某学习小组研究性学习的过程,并协助完成相关任务。
【研究课题】探究X物质的成分。
【查阅资料】(1)X物质可能由Ca(HCO3)2、Mg(HCO3)2、Ca(OH)2、Mg(OH)2、CaCO3、BaCO3中的一种或几种组成。
(2)X物质是通过过滤水溶液得到的沉淀。
(3)相关物质的溶解性如下表:
| 物 质 |
Ca(HCO3)2 |
Mg(HCO3)2 |
Ca(OH)2 |
Mg(OH)2 |
CaCO3 |
BaCO3 |
| 溶解性 |
可溶 |
可溶 |
微溶 |
不溶 |
不溶 |
不溶 |
【设计并实施方案】
(1)由查阅资料可知X物质肯定不含可溶性的Ca(HCO3)2、Mg(HCO3)2。
(2)甲同学在烧杯中放入少量研碎的X物质,加入足量蒸馏水充分搅拌,静置。取上层清液滴入Na2CO3溶液,没有白色沉淀,说明X物质中无 (填化学式)。
(3)乙同学设计了下列实验装置,想进一步确定X物质的成分。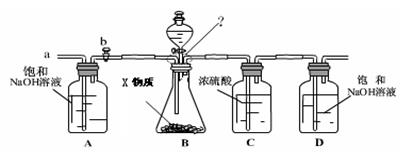
其主要实验步骤如下:
①按图组装仪器,关闭活塞b,将50gX物质的粉末放入锥形瓶中,逐滴加入足量稀硫酸,充分反应。
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气;
③称量D瓶内物质明显增加的质量;
④继续鼓入空气,直至D瓶内物质质量不变;
⑤经称量,D瓶内物质增加的质量为20g。
【评价】(1)A瓶中的NaOH溶液起到 作用。若A瓶中无NaOH溶液,D瓶中的质量将 (填“增大”、“不变”或“减小”)。
(2)分析X物质的可能组成是 (有几种写几种)。
在天平两边的烧杯中分别100g、10%的稀盐酸,然后在左盘烧杯中加入10g碳酸钙,在右盘的烧杯中加10g的混合物,待烧杯中固体物质完全消失后,天平指针保持平,则该混合物可能是
| A.碳酸钠和碳酸钙 | B.碳酸氢钠和碳酸镁 |
| C.碳酸氢钾和碳酸钠 | D.碳酸氢钠和碳酸钠 |
构建知识网络是学习化学的重要方法,下图是不同物质间相互转化关系图。其中 A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末。"→"表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:
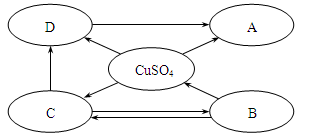
(1)C的化学式, A的化学式;
(2)写出由B生成硫酸铜的化学方程式;
(3)在该知识网络所涉及的化学反应中,可以归纳出能与盐发生反应的物质类别有。
A.单质
B.氧化物
C.酸
D.碱
E.盐
甲、乙、丙、丁四种物质的相互反应关系如图所示("-"表示相连的物质间能发生反应)下列符合对应反应关系的选项是()
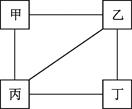
| 选项 |
A |
B |
C |
D |
|
| 物质 |
甲 |
|
|
|
|
| 乙 |
|
|
|||
| 丙 |
|
|
|
||
| 丁 |
|
|
小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现下图中所示的所有反应。若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是
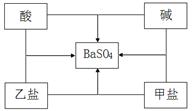
| A. | |
| B. | |
| C. | |
| D. |