下列除去杂质的方法中,错误的是 ( )
| 选项 |
物质 |
杂质 |
除杂质的方法 |
| A. |
稀硫酸 |
铜 |
过滤 |
| B. |
CaSO4溶液 |
稀硫酸 |
过量CaCO3、过滤 |
| C. |
FeCl2溶液 |
CuCl2 |
过量铁粉、过滤 |
| D. |
二氧化碳 |
一氧化碳 |
点燃 |
下图是a、b两种固体物质的溶解度曲线。下列说法不正确的是 ( )
A.a的溶解度大于b的溶解度
B.在t℃时,a、b的饱和溶液中溶质的质量分数相同
C.将t℃时b的饱和溶液升温至40℃,其溶液中溶质的质量分数不变
D .10℃时,分别用100 g水配制a、b的饱和溶液所需a的质量小于b的质量
食盐是日常生活中的必须品,也是重要的化工原料。一同学用某种粗盐进行提纯实验,步骤如图所示。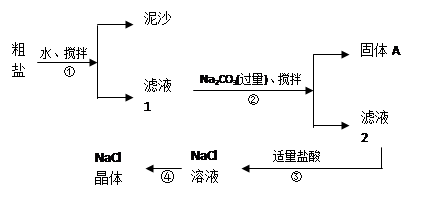
请回答:
Ⅰ.步骤①和②的操作名称是 (7) ;
Ⅱ.步骤④操作时要用玻璃棒不断搅拌,这是为了防止 (8) 。
Ⅲ.猜想与验证:
| 猜想 |
验证方法 |
实验现象 |
结论 |
| 猜想1: 固体A中含CaCO3 |
取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口。 |
(9) |
猜想1成立 |
| 猜想2: 固体A中含BaCO3 |
取少量固体A于试管中,先滴入 (10) ,再滴入 (11) 溶液。 |
有气泡放出,无白色沉淀 |
(12) |
| 猜想3: 最后制得的NaCl晶体中还含有Na2SO4 |
取少量NaCl晶体于试管中,加适量蒸馏水溶解,再 (13) 。 |
(14) |
猜想3成立 |
Ⅳ. 鉴别NaCl和KNO3溶液的两种方法分别是 (15) ;
(16) 。
对大量的实验事实进行分析,找出一些规律,并根据这些规律和物质的内在联系,对一些物质性质进行推测,这是化学学习中非常重要的科学方法。请你仿照下表中的思维过程,以学过的酸、碱、盐的化学性质为例,填写下表中的空格(所填规律不能重复)。
| 实验事实(每空举两例) |
规 律 |
推测同类物质所具有的相同性质 |
| 示例:盐酸、稀硝酸能使紫色石蕊试液变红 |
酸溶液能使紫色石蕊试液变红 |
稀硫酸也能使紫色石蕊试液变红 |
| Ⅰ.碳酸钙、碳酸钠都能与稀盐酸反应,生成二氧化碳气体 |
(2) |
(3) |
| Ⅱ. (4) |
(5) |
(6) |
.某地生产的一种食盐的配料如下:氯化钠、食用碳酸钙、碘酸钾。为了测定此盐中的钙元素含量,取10g这种盐,加入足量的稀盐酸,生成0.003molCO2。请计算此食盐中含(写出计算过程):
Ⅰ.碳酸钙的物质的量?
Ⅱ.钙元素的质量分数?
油脂是重要的营养物质。油脂有人体内完全氧化时,每克放出约39.3kJ的能量。如果油脂的化学式为C57H110O6,则:
(1)该油脂由_____________种元素组成,其相对分子质量是___________。
(2)正常人每天消耗9432kJ能量,如是能量的25%由油脂提供,则我们每天水约需要摄入__________g油脂,才能维持机体平衡。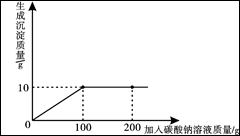
印刷铜制电路板的“腐蚀液”为FeCl3溶液。已知铜、铁均能与FeCl3溶液反应,反应方程式分别为:Cu+2FeCl3=2FeCl2+CuCl2,Fe+2FeCl3=3FeCl2。现将一包铜、铁的混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,关于烧杯中物质组成的说法正确的是
| A.溶液中一定含FeCl3,固体一定是铁和铜 |
| B.溶液中一定含FeCl2,固体一定含铜 |
| C.溶液中一定含FeCl2、CuCl2,固体一定含铜 |
| D.溶液中一定含FeCl2,固体一定是铁和铜 |
酸、碱、盐是初中化学学习的重要内容,同学们在实验室对酸、碱、盐的性质进行探究。
(1)酸和碱的组成中都含有氢元素,右图是氢在元素周期表中的一些信息,下列说法中错误的是___________。
| A.氢元素属于非金属元素 | B.氢原子核内质子数为1 |
| C.氢原子的质量为1.008 | D.氢原子的结构示意图为 |
(2)盐酸和硫酸具有很多相似的化学性质,这是因为其溶液中都含有________(填符号)。
(3)小华同学打开盛放浓硫酸和浓盐酸的试剂瓶盖后,立即就能把它们区分开来,这是为什么?
(4)在进行酸碱中和反应的实验时,小明同学向烧杯中的氢氧化钠溶液滴加稀硫酸,一会儿发现由于忘记了滴加酚酞指示剂,因而无法确定稀硫酸与氢氧化钠是否恰好完全反应。
①同学们对溶质的成分提出了自己的看法:
小贝同学说:溶质除了硫酸钠还有氢氧化钠;小华同学说:溶质除了硫酸钠还有稀硫酸;小明同学说:溶质________ _____________________。
②为了证明大家的猜想,老师取出少量反应后的溶液于一支试管中,并向试管中滴加几滴酚酞溶液,振荡,观察到溶液无明显变化。 则这三位同学的猜想中不正确的是 。
(5)小钢同学要配制70g溶质质量分数为5.4%的氯化铜溶液,经计算,他需要称量氯化铜的质量为__________g。
氯化铜溶液是蓝色的溶液,氯化铜溶液中主要含有Cu2+、Clˉ和水分子。某探究小组为探究氯化铜溶液中的哪种微粒能使氯化铜溶液显蓝色,设计了如下实验方案,得出了初步结论。请填写下表中的实验结论:
| 实 验 操 作 |
实验现象 |
实 验 结 论 |
| 取少量氯化钠固体,放入 试管中,加水,振荡 |
固体溶解, 溶液呈无色 |
|
(6)取50g溶质质量分数为5.4%的氯化铜溶液于烧杯中,向烧杯中加入50g氢氧化钠溶液,二者正好完全反应,求反应后生成沉淀的质量。
氨气是一种具有强烈刺激性气味的气体,密度比空气小,极易溶于水,其水溶液显碱性,实验室可用加热氯化铵与氢氧化钙固体混合物来制取氨气。
(1)请你从图甲中选择实验室用此方法制取氨气的发生装置。
(2)若用C装置收集氨气,则气体要从_______(填“a”或“b”)进入集气瓶。
(3)闻氨气时,在操作上应注意什么问题?
(4)图乙是利用氨气做的一个趣味实验(夹持设备已略去),烧瓶中装有干燥的氨气,胶头滴管中装有水,先关闭阀门,将胶头滴管中的水挤入烧瓶内,然后打开阀门,请你描述烧瓶中可能出现的现象。
在Cu(NO3)2、AgNO3和KNO3的混合溶液中加入一定量镁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,没有气泡产生。
(1)请说出滤出的固体中一定含有哪些成分?滤液中一定含有哪些成分?
(2)写出反应过程中一定发生的化学反应方程式:
如图是某趣味实验装置图,挤压胶头滴管后,可观察到什么现象?请分析其原因,并写出化学方程式。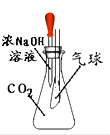
某同学将8g纯碱溶解在42g水中,配制了一瓶溶液,储放时忘记制作标签。
(1)请你为该瓶溶液制作一张标签。(填入右图中)
(2)如何用简单实验证明该溶液呈碱性,简述实验步骤和主要实验现象。
下列各组物质只用一种试剂无法鉴别出的是【 】
| A.NH4NO3、NaOH 、NaCl | B.NaCl溶液 、HCl溶液 、NaOH溶液 |
| C.Na2CO3 溶液、AgNO3溶液、NaCl溶液 | D.KCl溶液、 KNO3溶液、NaCl溶液 |
2012年春节第三天,广西柳州人以疯抢超市瓶装水开启了他们的2012年,约21吨重金属镉沿龙江如幽灵顺流而下,向广西的其他城市游荡而去。
(1)试举出防止水污染的具体措施。(写一条即可)
(2)试写出一个有水生成的分解反应。
(3)水是常用的溶剂。盛装氢氧化钠溶液的试剂瓶口常会出现白色碳酸钠粉末,请用化学方程式表示其原理。如何证实白色粉末是碳酸钠而不是氢氧化钠?
(4)如果用装满水的右图装置收集氢气,则氢气应从 端(填“a”或“b”)进入装置中。如果用右图装置干燥氧气,则装置中应装入的液体为 ;氧气应从 端(填“a”或“b”)进入装置中.
(5)实验室制备氧气的方法有多种。实验小组的同学们选择用氯酸钾和二氧化锰的混合物制取氧气,混合物共5.50 g,加热至质量不再改变时为止,冷却,称量剩余物的质量为3.58 g。求:原混合物中氯酸钾的质量是多少克?
请回答下列有关金属的问题。
(1)铁在潮湿的空气中容易生锈。小明同学发现生锈后的铁钉质量会增加,于是得出“质量守恒定律”也有例外,你认为该同学的推测正确吗?请加以解释。
(2)某化学兴趣小组为测定Al、Fe、Cu、Ag四种金属的活动性,设计了如下方法:
先将粗细相同的铝丝和铁丝分别放入稀盐酸溶液中,然后将铜丝放入硝酸银溶液中。试回答下面问题:
实验发现,短时间内铝丝表面无气泡产生,几分钟后产生大量气泡。产生该现象的原因可能是什么?
小明同学分析认为上述实验不足以得出四种金属的活动性顺序,想再补充一个实验,请你和他一起设计实验方案并进行实验,达到探究目的。