[上海]2011-2012学年上海市卢湾区中考模拟二模化学试卷
下列关于氢气的用途中,只利用了氢气的物理性质的是( )。
| A.充填探空气球 | B.作氢能源 |
| C.作火箭燃料 | D.冶炼金属 |
在公共场所吸烟,会使周围的人被动吸“二手烟”。“二手烟”中含有一种能与人体血液中血红蛋白结合的有毒气体,该气体是( )。
| A.N2 | B.O2 | C.CO2 | D.CO |
走进新装修的房屋常有一股异味,利用有关分子的性质解释该现象,最合理的是( )。
| A.分子的质量很小 | B.分子在不断运动 |
| C.分子间有间隙 | D.分子的体积很小 |
下面是几种农作物生长时对土壤要求的最佳pH范围:茶5—5.5;西瓜6;大豆6—7;甜菜7—7.5。如果某地区经常下酸雨,以上农作物最不适宜种植的是 ( )。
| A.茶 | B.西瓜 | C.大豆 | D.甜菜 |
.下列物质互为同素异形体的是( )。
| A.一氧化碳、二氧化碳 | B.白磷、红磷 |
| C.冰、水 | D.天然气、甲烷 |
欲将20℃时的硝酸钠不饱和溶液转变为饱和溶液,可以采取的方法是 ( )。
| A.升高温度 | B.加入水 |
| C.加入固体硝酸钠 | D.倒掉一半溶液 |
下列各组物质或其主要成分属于同一种物质的是( )。
| A.氢氧化铁、铁锈 | B.石灰石、生石灰 |
| C.熟石灰、氢氧化钙 | D.纯碱、烧碱 |
某无色溶液能使紫色石蕊试液变蓝,则该溶液能使无色酚酞试液变( )。
| A.蓝色 | B.红色 | C.紫色 | D.无色 |
我国最新研制的高温超导材料氮化硼,经测定该化合物中两种元素的化合价之比为1:1,其化学式为( )。
| A.BN | B.N2B | C.B3N2 | D.B2N3 |
纳米材料被誉为21世纪最有前途的新型材料,其中纳米碳管是一种由碳原子构成的直径为几个纳米(1纳米=10—9米)的空心管,则下列说法中错误的是( )。
| A.纳米碳管是一种新型的化合物 |
| B.纳米碳管如果完全燃烧后生成二氧化碳 |
| C.纳米碳管在常温下化学性质稳定 |
| D.纳米碳管属于纯净物 |
在焊接铁轨的反应:2Al+Fe2O3 2Fe+Al2O3中,氧化剂是( )。
2Fe+Al2O3中,氧化剂是( )。
| A.Al | B.Fe | C.Al2O3 | D.Fe2O3 |
某化学兴趣小组为测定Zn、Cu、Ag三种金属的活动顺序,设计了四种方案,每种方案所用试剂如下,其中可行的是( )。
| A.Zn、Cu、AgNO3溶液 | B.Cu、ZnSO4溶液、AgNO3溶液 |
| C.Zn、Cu、Ag、稀硫酸 | D.Ag、CuSO4溶液、AgNO3溶液 |
亚硝酸钠(NaNO2)的外观与食盐很相似,有咸味,误食易中毒。区别它们的一种方法是:将两者分别加热到320℃,不分解的是食盐,能分解并放出一种具有刺激性气味气体的是亚硝酸钠。该气体可能是( )。
| A.NH3 | B.SO2 | C.NO2 | D.N2 |
学习化学时会遇到许多“相等”,下列“相等”的说法中错误的是( )。
| A.化学反应前后原子的数量一定相等 |
| B.物质发生化学变化前后,质量总和一定相等 |
| C.溶液稀释前后溶质的质量一定相等 |
| D.中和反应中参加反应的酸和碱的物质的量一定相等 |
下列化学方程式符合题意且书写正确的是( )。
| A.验证铜的金属活动性比银强:Cu+2AgCl→CuCl2+2Ag |
| B.除去烧碱溶液中混有少量纯碱:Na2CO3+2 HCl→2NaCl+ H2O+CO2↑ |
| C.制取少量的硫酸镁:MgCl2+Na2SO4→MgSO4+2NaCl |
| D.用稀盐酸除去水垢:CaCO3+2HCl→CaCl2+H2O+CO2↑ |
已知铜、铁均能与FeCl3溶液反应,反应方程式分别为:
Cu+2FeCl3→2FeCl2+CuCl2,Fe+2FeCl3→3FeCl2。现将一包铜、铁的混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,关于烧杯中物质组成的说法中正确的是( )。
| A.溶液中一定含FeCl2,固体一定是铁和铜 |
| B.溶液中一定含FeCl3,固体一定含铜 |
| C.溶液中一定含FeCl2,固体一定含铜 |
| D.溶液中一定含FeCl2、CuCl2,固体一定含铜 |
生活中离不开水,净化水的知识在日常生活中有着广泛的应用。
要除去水中的异味和色素,常在自制净水器中加入 (1) ;
自来水厂可用氯气消毒杀菌,氯气的化学式为 (2) 。
露天烧烤不仅产生大量有害气体污染环境,而且烧焦的肉中还含有强烈致癌物质(3,4—苯并芘),其化学式为C20H12。3,4—苯并芘中含有 (3) 种元素,碳原子与氢原子的物质的量比为 (4) ,该物质的1mol分子中含有碳原子约 (5) 个。
在一定温度下,向质量均为50g的四份水中分别加入一定质量的KNO3固体,搅拌至充分溶解(如有不溶解的KNO3,则过滤除去),得到溶液。加入KNO3的质量与得到相应溶液的质量如下表所示。
| 实验编号 |
实验1 |
实验2 |
实验3 |
实验4 |
| 加入KNO3的质量(g) |
40 |
50 |
60 |
70 |
| 溶液质量(g) |
90 |
100 |
105 |
105 |
Ⅰ.该温度下KNO3的溶解度是 (6) g/100gH2O。
Ⅱ.设实验1到实验4配制的溶液中溶质的质量分数分别为a、b、c、d,则它们的大小为:a (7) b (8) c (9) d(填“大于”、“等于”或“小于”)。
一包黑色粉末可能由氧化铜、木炭粉中的一种或两种组成。为探究其组成,某化学兴趣小组的学生选择以下部分装置进行实验。
Ⅰ.小亮用装置A 与E连接,关闭弹簧夹X,给排尽空气后的盛有黑色粉末的硬质玻璃管加热。一段时间后,若黑色粉末变红色,澄清石灰水变浑浊,则可判断该黑色粉末的成分是 (10) (写化学式),写出产生上述现象时,玻璃管内物质发生反应的化学方程式 (11) ;
若黑色粉末不变色,澄清石灰水也不变浑浊,则无法确定黑色粉末的成分。
为进一步确定其成分,小明帮助小亮又进行如下实验:他将干燥的氢气与A中的黑色粉末反应,并检验其产物。你认为他应选择的仪器装置以及连接顺序依次为 (12) (填字母代号),在给黑色固体加热前,应先通入氢气,目的是 (13) 。
若实验现象为 (14) ,则黑色粉末的成分是氧化铜;若无上述实验现象则为木炭。
Ⅱ.除上述方法外,小强又设想出另一种简单易行的实验方法:取少量粉末于试管中,再加入过量 (15) 试剂(填试剂名称),实验中可能出现的现象与对应的结论如下表所示(表中未列完所有情况),请你完成下表:
| |
实验现象 |
结论 |
| ① |
有黑色不溶物,溶液呈蓝色 |
(16) |
| ② |
(17) |
只含木炭 |
| ③ |
(18) |
(19) |
.某地生产的一种食盐的配料如下:氯化钠、食用碳酸钙、碘酸钾。为了测定此盐中的钙元素含量,取10g这种盐,加入足量的稀盐酸,生成0.003molCO2。请计算此食盐中含(写出计算过程):
Ⅰ.碳酸钙的物质的量?
Ⅱ.钙元素的质量分数?
对大量的实验事实进行分析,找出一些规律,并根据这些规律和物质的内在联系,对一些物质性质进行推测,这是化学学习中非常重要的科学方法。请你仿照下表中的思维过程,以学过的酸、碱、盐的化学性质为例,填写下表中的空格(所填规律不能重复)。
| 实验事实(每空举两例) |
规 律 |
推测同类物质所具有的相同性质 |
| 示例:盐酸、稀硝酸能使紫色石蕊试液变红 |
酸溶液能使紫色石蕊试液变红 |
稀硫酸也能使紫色石蕊试液变红 |
| Ⅰ.碳酸钙、碳酸钠都能与稀盐酸反应,生成二氧化碳气体 |
(2) |
(3) |
| Ⅱ. (4) |
(5) |
(6) |
食盐是日常生活中的必须品,也是重要的化工原料。一同学用某种粗盐进行提纯实验,步骤如图所示。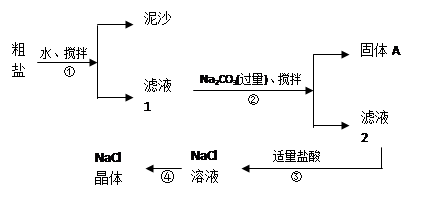
请回答:
Ⅰ.步骤①和②的操作名称是 (7) ;
Ⅱ.步骤④操作时要用玻璃棒不断搅拌,这是为了防止 (8) 。
Ⅲ.猜想与验证:
| 猜想 |
验证方法 |
实验现象 |
结论 |
| 猜想1: 固体A中含CaCO3 |
取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口。 |
(9) |
猜想1成立 |
| 猜想2: 固体A中含BaCO3 |
取少量固体A于试管中,先滴入 (10) ,再滴入 (11) 溶液。 |
有气泡放出,无白色沉淀 |
(12) |
| 猜想3: 最后制得的NaCl晶体中还含有Na2SO4 |
取少量NaCl晶体于试管中,加适量蒸馏水溶解,再 (13) 。 |
(14) |
猜想3成立 |
Ⅳ. 鉴别NaCl和KNO3溶液的两种方法分别是 (15) ;
(16) 。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号