下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D、E为无色气体,C能使湿润的红色石蕊试纸变蓝,B常温下为无色液体,X是一种酸式盐。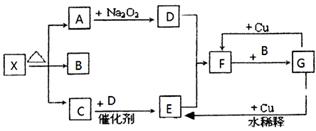
(1)写出下列各物质的化学式:X: ;F: ;G: 。
(2)利用Na2O2与A反应常作供氧剂,写出其反应方程式: 。写出G→E的化学反应方程式: 。
(3)E→F的实验现象是 ,G的稀溶液与少量Fe粉反应的离子方程式为 ,检验反应后溶液中金属阳离子的试剂为 ,实验现象为 。
(4)F→G的反应 (填是或不是)氧化还原反应,若是,则氧化产物是 ,若不是,则此空不填。
局部麻醉药普鲁卡因E(结构简式为 )的三条合成路线如图所示(部分反应试剂和条件已省略):
)的三条合成路线如图所示(部分反应试剂和条件已省略):
请完成下列填空.
(1)比A多一个碳原子,且苯环上只有一个支链的A的同系物的名称是_______.反应①所需试剂和条件为_____________________。
(2)设计反应②的目的是______________。
(3)B的结构简式为_______________;C中官能团的名称是______________。
(4)满足下列条件的D的同分异构体的一种结构简式为__________或____________;1mol该物质与NaOH溶液共热最多消耗_________molNaOH.
①芳香族化合物②能发生水解反应③有3种不同环境的氢原子
(5)写出以A为原料(其他试剂任选)合成邻氨基苯甲酸甲酯( )的合成路线流程图.
)的合成路线流程图.
①已知:苯环取代基定位基团中甲基是邻对位定位基团;-NO2在Fe/HCl条件下还原成-NH2
②合成路线流程图示例如下:
(10分)已知有如图所示物质的相互转化,试回答:
(1)写出B的化学式 ,D的化学式 。
(2)写出由E转变成F的化学方程式______________________________。
(3)向G溶液中加入A时反应的离子方程式为______________________。
(4)A与稀盐酸反应生成0.1 mol气体,转移电子数为_______ 。
酯类是工业上重要的有机原料,具有广泛用途。
下图是乙酸乙酯的合成路线图,已知A能与银氨溶液反应析出银镜,B的水溶液可以溶解CaCO3,E可作果实催熟剂。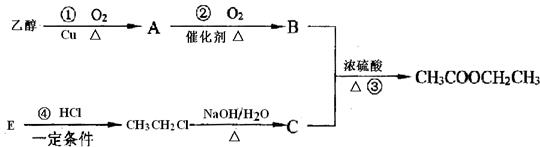
请完成下列问题:
(1)A的名称是 ;B中所含的官能团是 ;反应③的反应类型是 ;反应④的反应类型是 。
(2)A的结构简式为 ;E的结构简式为 。
(3)请写出反应①、④的化学方程式:
① ;
④ 。
选做(15分)【化学选修5:有机化学基础】
某芳香族化合物J常用作防腐剂,J可利用下列路线合成:
已知:①A的相对分子质量为92的烃
②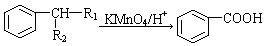 (—R1、—R2—表示氢原子或烃基)
(—R1、—R2—表示氢原子或烃基)
③
④D的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积之比为1:1。
回答下列问题:
(1)A的分子式为 ,由A→B的反应试剂和反应条件为 。
(2)写出C→D的反应方程式: 。
(3)同时符合下列条件的E的同分异构体共有 种。
①能发生银镜反应
②能使FeCl3溶液发生显色反应。
(4)F的结构式为 ,写出G→H的反应方程式: 。
(5)检验H中含氧官能团的试剂为 (填试剂名称),由H→I的反应类型为 。
(6)J的结构简式为 。
以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:
Ⅰ. 将黄铜矿精矿(主要成分为CuFeS2,含有少量CaO、MgO、Al2O3)粉碎
Ⅱ. 采用如下装置进行电化学浸出实验

将精选黄铜矿粉加入电解槽阳极区,恒速搅拌,使矿粉溶解。在阴极区通入氧气,并 加入少量催化剂。
Ⅲ. 一段时间后,抽取阴极区溶液,向其中加入有机萃取剂(RH)发生反应:
2RH(有机相)+ Cu2+(水相) R2Cu(有机相)+ 2H+(水相)
R2Cu(有机相)+ 2H+(水相)
分离出有机相,向其中加入一定浓度的硫酸,使Cu2+得以再生。
Ⅳ. 电解硫酸铜溶液制得金属铜。
(1)黄铜矿粉加入阳极区与硫酸及硫酸铁主要发生以下反应:
CuFeS2 + 4H+ = Cu2+ + Fe2+ + 2H2S 2Fe3+ + H2S = 2Fe2+ + S↓+ 2H+
① 阳极区硫酸铁的主要作用是 。
② 电解过程中,阳极区Fe3+的浓度基本保持不变,原因是 。
(2)阴极区,电极上开始时有大量气泡产生,后有固体析出,一段时间后固体溶解。
写出上述现象对应的反应式 。
(3)若在实验室进行步骤Ⅲ,分离有机相和水相的主要实验仪器是 ;加入有机萃取剂的目的是 。
(4)步骤Ⅲ,向有机相中加入一定浓度的硫酸,Cu2+得以再生的原理是 。
(5)步骤Ⅳ,若电解200mL0.5 mol/L的CuSO4溶液,生成铜3.2 g,此时溶液中离子浓度由大到小的顺序是 。(忽略电解前后溶液体积的变化)
A是乙烯与水加成后的产物,它易溶于水并有特殊香味,并能进行如图所示的多种反应。
(1)写出A的化学式 。
(2)下列反应的化学方程式及反应类型
反应① 反应类型: ;
反应② 反应类型: ;
反应③ 反应类型: ;
反应④ 反应类型: ;
(3)比较反应①与钠和水反应的现象有什么相同和不同
相同点: 。
不同点: 。
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素。
(1)若A为气体单质,则① B→E的化学方程式 ;
② 标准状况下,若将充满干燥D气体的烧瓶倒置于水槽中,烧瓶内液面逐渐上升,(不考虑烧瓶内溶液扩散因素),则最终烧瓶内所得溶液的物质的量浓度为
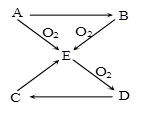
(2)若A为固体单质,且易溶于二硫化碳, 则 ① D的分子式 为 ;
② C→E的化学方程式为 ;
③ 将E通入某些单质的溶液中,可发生反应生成两种强酸,试举一例写出化学方程式 。
我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图:
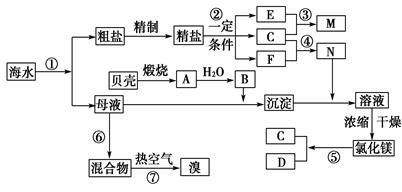
Ⅰ.(1)写出N的化学式_________________________;
(2)写出反应②的化学方程式_________________________。
Ⅱ.粗盐中含有Ca2+、Mg2+、
SO42-等杂质,精制时所用的
试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为____________。
A.②③④① B.③④②① C.④③②① D.③②④①
Ⅲ.提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2。
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是____________。
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(2)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是____________。
A.从外地购买 B.在当地新建生产厂
C.从本厂生产烧碱处循环 D.从本厂生产镁单质处循环
(3)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2 乙:母液先提取Br2,后提取Mg
请你判断哪个更合适?______(填“甲”或“乙),理由是____________________________ ___。
Ⅰ.某烃A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢。
(1)写出A的结构简式 。
(2)A中的碳原子是否都处于同一平面? (填“是”或者“不是”)。
Ⅱ.2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭。“亮菌甲素”的结构简式为:  。它配以辅料丙二醇溶成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性。请回答下列问题:
。它配以辅料丙二醇溶成针剂用于临床。假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性。请回答下列问题:
(3)下列有关“亮菌甲素”的叙述正确的是 (填字母)。
| A.“亮菌甲素”能与H2发生加成反应 |
| B.不能使酸性KMnO4溶液褪色 |
| C.“亮菌甲素” 的分子式是C12H10O5 |
| D.“亮菌甲素”分子中含氧官能团只有2种 |
(4)丙二醇的分子式是C3H8O2,已知两个羟基连在同一个碳原子上的物质不存在。写出其所有属于醇类的同分异构体的结构简式 。
(5)依据核磁共振氢谱分析,二甘醇分子中有3个吸收峰,其峰面积之比为2∶2∶1。又知二甘醇中含碳、氧元素的质量分数相同,且氢元素的质量分数为9.4%,1 mol二甘醇与足量金属钠反应生成1 mol H2。写出二甘醇的结构简式 。
聚芳酯(PAR)是分子主链上带有苯环和酯基的特种工程塑料,在航空航天等领域具有广泛应用。下图是利用乙酰丙酸(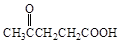 )合成聚芳酯E的路线:
)合成聚芳酯E的路线:
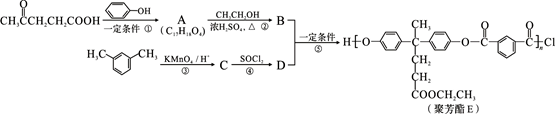
已知:①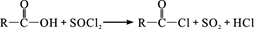
②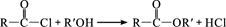 (R、R′表示烃基)
(R、R′表示烃基)
(1)乙酰丙酸中含有的官能团是羰基和 (填官能团名称)。
(2)D的结构简式为 。
(3)下列关于有机物B的说法正确的是 (填字母代号)。
a.能发生取代反应
b.能与浓溴水反应
c.能发生消去反应
d.能与H2发生加成反应
(4)A→B的化学方程式为 。
(5)C的分子式为 ,符合下列条件的C的同分异构体有 种。
①能发生银镜反应
②能与NaHCO3溶液反应
③分子中有苯环,分子中无 结构
结构
在上述同分异构体中,有一种苯环上有两个取代基且核磁共振氢谱图有4种峰的物质,写出该物质与足量NaOH溶液共热反应的化学方程式 。
已知A为一种盐,C、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、
H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。
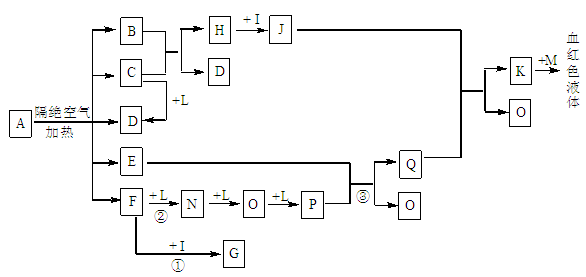
(1)写出D的电子式为_______________;
(2)写出反应②的化学方程式: ;反应③中氧化剂和还原剂的物质的量之比为_________________;
(3)将等体积、等浓度的G和F的溶液混合,溶液显碱性,则溶液中离子浓度从大到小的顺序为 ;
(4)检验J中阳离子的实验方法为 ;
(5)已知B中氧元素的质量分数为22.2﹪,且A分解产生的各物质的物质的量之比为n(B):n(C):
n(D):n(E):n(F)=1:2:2:1:2,则A的化学式为__________________________。
[化学—选修 有机化学基础]
现有分子式为CnH8O2X2的物质M,可发生如下所示转化:
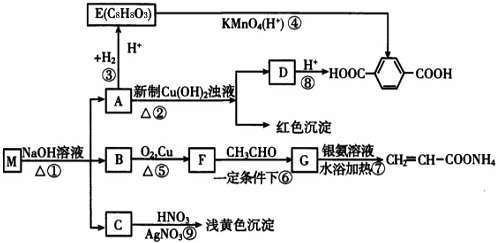
已知:①物质B在质谱分析中,在质谱图显示存在多种质荷比不相同的粒子,其中质荷比最大的为32,物质B在核磁共振氢谱分析中,有两个吸收峰,吸收峰面积之比为3:1。
②两个-OH同时连在一个C原子上,结构不稳定,会自动失水,如:
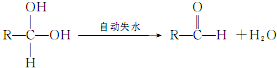
请回答下列问题:(1)n值为_______,M中官能团名称为__________。
(2)①、③的反应类型:①_______,③__________。
(3)写出M、E、G的结构简式;M:_______;G:_______。
(4)写出下列反应的化学方程式:A→D:__________。
(5)符合下列条件的E的同分异构体有_______种,写出其中核磁共振氢谱有五组峰,峰面积之比为1:1:2:2:2的同分异构体的结构简式为__________________(写一种)。
①能发生水解反应 ②能发生银镜反应 ③遇FeCl3溶液显紫色
有四种化合物W、X、Y、Z,它们都是由短周期元素A、B、C、D、E中的两种元素组成的。已知:
(a)A、B、C、D、E五种元素的原子序数依次增大,且A、D同主族,C、E同主族,B、C同周期。
(b)W由B、C组成,分子中原子个数比为B:C=1:2,固体易升华。
(c)X由A、C组成,分子中原子个数比为A:C=1:1。
(d)Y由C、D形成的离子化合物,且Y中相应元素的微粒之比为:C:D=1:1。
(e)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阴、阳离子数之比为1:2。
试回答下列各小题:
(1)各元素符号:A B C D E
(2)W的电子式: 。
(3)X的结构式: 。
(4)Y的电子式: 。
(5)Z的化学式: 。
(6)写出Y与水反应的化学方程式: 。
【原创】(18分)甲、乙、丙是常见的三种物质,它们之间有如图所示的转化关系。根据要求回答下列问题:
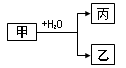
I.已知:甲是由两种短周期元素组成的化合物,丙的水溶液显碱性。
(1)若构成甲的阴、阳离子个数比为2:3,丙是气体。则构成甲的阴、阳离子半径大小关系为 (用具体的微粒表示)。
(2)若乙是O2,则甲的一种重要用途是 ;产物丙与Cl2按2:1(物质的量)反应得到丁溶液,丁溶液中阴离子浓度从大到小的顺序是 。
Ⅱ.一种灰白色固体粉末X是由两种常见元素组成的化合物,其中金属元素与另一元素的质量比为14:l。在一定条件下X可发生如下图的转化关系,有的反应标出全部产物,有的反应标出部分产物。已知P为混合气体,R是无色无味能使澄清石灰水变浑浊的气体,C为红褐色物质,M为常见金属单质,Q为常见非金属单质。请回答下列问题:

(1)X的化学式为______________;R的电子式为_________________。
(2)写出气体P的组成 。
(3)写出D→G的离子反应方程式 。
(4)M与钛构成的合金是一种常用的不锈钢材料,某同学在探究该合金的性质时,往含有TiO2+、M3+溶液中加入M至溶液显紫色,该过程中发生的反应有:
①2TiO2+(无色)+Fe+4H+==2Ti3+(紫色)+Fe2++2H2O
②Ti3+(紫色)+Fe3++H2O ="=" TiO2+(无色)+Fe2++2H+
③ 。
请写出③可能的反应方程式 。
(5)人们对X的结构研究后发现其金属元素有0价、+2价两种化合价,写出X与稀硫酸反应的化学方程式 。
(6)聚合硫酸M是一种常见的净水剂,化学式为:[M2(OH)n (SO4)3- ]m (n>2,m≤10),其制备可由硫酸M经水解后再聚合得到,其中聚合反应的原理为m[M2(OH)n(SO4)3-
]m (n>2,m≤10),其制备可由硫酸M经水解后再聚合得到,其中聚合反应的原理为m[M2(OH)n(SO4)3- ]
]  [M2(OH)n(SO4)3-
[M2(OH)n(SO4)3- ]m,则写出硫酸M水解的化学方程式为 。
]m,则写出硫酸M水解的化学方程式为 。
【命题立意】本题综合考查元素及其化合物的知识,融入信息型化学方程式的书写,旨在考查考生知识迁移能力以及应用化学原理解决实际问题的能力。