新疆乌鲁木齐地区高三第二次诊断性测试化学试卷
化学与生产生活、环境保护密切相关。下列说法中不正确的是
| A.食盐既可作调味品也可作食品防腐剂 |
| B.向海水中加入净水剂明矾可以使海水淡化 |
| C.加大石油、煤炭的开采速度,增加化石燃料的供应不利于“蓝天工程”的建设 |
| D.高铁车厢材料大部分采用铝合金,因为铝合金强度大、质量轻、抗腐蚀能力强 |
下列化学用语的表示正确的是
A.CS2的比例模型: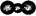 |
| B.乙醇的结构简式:C2H6O |
| C.核内有8个中子的碳原子:86C |
| D.HClO的结构简式:H—Cl—O |
下列有关物质的性质和应用都正确的是
| A.氢氟酸具有强酸性,可用于雕刻玻璃 |
| B.氨气显碱性,可用碱石灰或无水CaCl2干燥 |
| C.MgO、A12O3熔点高,它们都可用于制作耐火材料 |
| D.铜的活动性比铁弱,可在海轮外壳装铜块减缓海轮腐蚀 |
下列实验操作不能达到预期目的的是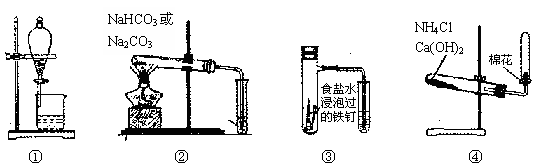
| A.①分离CH3COOC2H5和饱和碳酸钠溶液 |
| B.②鉴别碳酸钠和碳酸氢钠 |
| C.③铁的吸氧腐蚀实验 |
| D.④实验室制备氨气 |
下列关于有机物的描述正确的是
| A.葡萄糖和果糖互为同分异构体,淀粉和纤维素也互为同分异构体 |
| B.淀粉、油脂和蛋白质都能发生水解反应 |
| C.多糖、蛋白质、脂肪和聚丙烯都属于高分子化合物 |
| D.汽油、柴油和植物油都是碳氢化合物 |
短周期主族元素X、Y、W、Z的原子序数依次增大。其中X、Z同主族,Z的单质是一种良好的半导体材料,W3+与Y2—具有相同的核外电子数。下列叙述正确的是
| A.Y2—的离子半径大于W3+的离子半径 |
| B.Y、Z形成的化合物为离子化合物 |
| C.Z的最高价氧化物对应的水化物的酸性比X的强 |
| D.X的气态简单氢化物的稳定性比Y的强 |
下列反应的离子方程式正确的是
| A.钠和硫酸铜溶液反应:2Na+Cu2+=2Na++Cu |
| B.AlCl3溶液中加入足量的氨水制Al(OH)3:Al3++3OH—=Al(OH)3↓ |
| C.向碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca2++HCO3—+OH—=CaCO3↓+H2O |
| D.二氧化硅溶于NaOH溶液:SiO2+2OH—=SiO32—+H2O |
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.200 mL1 mol Al2(SO4)3溶液中,Al3+和SO42—离子数的总和为NA |
| B.标准状况下,2.24 L乙醇中含有的C—H键数目为0.5NA |
| C.0.1 mol Na完全被氧化生成Na2O2,转移电子的数目为0.1NA |
| D.0.1 mol O2和O3的混合气体中含氧原子数目为0.2NA |
已知如下两个热化学反应 (l)+H2(g)→
(l)+H2(g)→ (l)
(l)  H>0 ①
H>0 ① (l)+2H2(g)→
(l)+2H2(g)→ (l)
(l)  H<0 ②
H<0 ②
下列说法不正确的是
| A.反应①、②都属于加成反应 |
| B.l,3一环己二烯比苯稳定 |
| C.反应①、②的热效应说明苯环中含有的并不是碳碳双键 |
| D.反应①、②中的所有有机物均可使溴水褪色,但褪色原理不完全相同 |
镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。如图为“镁一次氯酸盐”燃料电池示意图,电极为镁合金和铂合金。关于该电池的叙述正确的是
| A.E为该燃料电池的正极 |
| B.负极发生的电极反应式为ClO—+2e—+H2O=Cl—+2OH— |
| C.电池工作时,正极周围溶液的pH将不断变小 |
| D.镁燃料电池负极能发生自腐蚀产生氢气,使负极利用率降低 |
已知平衡:①C2H4(g) C2H2(g)+H2(g),②2CH4(g)
C2H2(g)+H2(g),②2CH4(g) C2H4(g)+2H2(g)。当升高温度时,①和②式皆向右移动。
C2H4(g)+2H2(g)。当升高温度时,①和②式皆向右移动。
(1)C(s)+2H2(g) CH4(g)
CH4(g)  H1
H1
(2)2C(s)+H2(g) C2H2(g)
C2H2(g)  H2
H2
(3)2C(s)+2H2(g) C2H4(g)
C2H4(g)  H3
H3
下列有关(1)、(2)和(3)中的 H1、
H1、 H2、
H2、 H3大小顺序排列正确的是
H3大小顺序排列正确的是
A. H1> H1> H2> H2> H3 H3 |
B. H2> H2> H3>2 H3>2 H1 H1 |
C. H2> H2> H1> H1> H3 H3 |
D. H3> H3> H2>2 H2>2 H1 H1 |
CH4和N2在一定条件下能直接生成氨:3CH4(g)+2N2(g)  3C(s)+4NH3(g)
3C(s)+4NH3(g)  H>0,700 ℃时,
H>0,700 ℃时,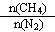 与CH4的平衡转化率的关系如图所示。下列判断正确的是
与CH4的平衡转化率的关系如图所示。下列判断正确的是
A.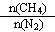 越大,CH4的转化率越高 越大,CH4的转化率越高 |
B.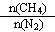 不变时,升温,NH3的体积分数会减小 不变时,升温,NH3的体积分数会减小 |
| C.b点对应的平衡常数比a点的大 |
| D.a点对应的NH3的体积分数约为13% |
(8分)元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)Cl2的电子式是 。新制的氯水可用于漂白,工业上将氯气制成漂白粉的目的是 ,漂白粉是一种 (填“混合物”或“纯净物”)。
(2)碘元素在元素周期表中的位置是 ;为防缺碘,食盐中常添加碘酸钾,该物质内存在 键(填化学键类型)。
(3)溴单质是唯一常温下呈液态的非金属单质,液溴的保存通常采取的方法是 。
(4)已知:X2(g)+H2(g)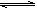 2HX(g) (X2表示Cl2、Br2和I2)。下图表示平衡常数K与温度T的关系。
2HX(g) (X2表示Cl2、Br2和I2)。下图表示平衡常数K与温度T的关系。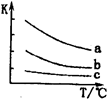
①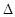 H表示X2与H2反应的晗变,H 0。(填“>”、“<”或“=”)
H表示X2与H2反应的晗变,H 0。(填“>”、“<”或“=”)
②曲线a表示的是 (填“Cl2”、“Br2”或“I2”)与H2反应时K与T的关系。
(7分)实验室里用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁[Fe2(OH)n(SO4)3—n/2]m和绿矾(FeSO4·7H2O),其过程如下:
(1)过程①中,FeS和O2、H2SO4反应的化学方程式是 。
(2)验证固体W焙烧后产生的气体含有SO2的方法是 。
(3)制备绿矾时,向溶液X中加入过量 ,充分反应后,经 操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。
(4)溶液Z的pH将影响聚铁中铁的质量分数,若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏 (填“高”或“低”),过程②中将溶液加热到70~80 ℃的目的是 。
(10分)甲醇合成反应为:CO(g)+2H2(g)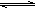 CH3OH(g)
CH3OH(g)
(1)合成甲醇的反应过程中物质能量变化如图所示。写出合成甲醇的热化学方程式 。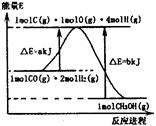
(2)实验室在lL密闭容器中进行模拟合成实验。将1 mol CO和2 mol H2通入容器中,分别恒温在300 ℃和500 ℃反应,每隔一定时间测得容器中甲醇的浓度如下:(表中数据单位:mol•L—l)
| 温度\时间 |
10min |
20min |
30min |
40min |
50min |
60min |
| 300 ℃ |
0.40 |
0.60 |
0.75 |
0.84 |
0.90 |
0.90 |
| 500 ℃ |
0.60 |
0.75 |
0.78 |
0.80 |
0.80 |
0.80 |
①300 ℃时反应开始10分钟内,H2的平均反应速率为 ;
②500 ℃时平衡常数K的数值为 ;
③300 ℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是 (选填编号)。
a.c(H2)减小
b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加
d.重新平衡时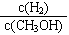 减小
减小
(3)下图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。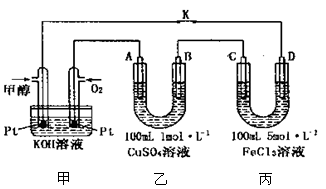
①甲中负极的电极反应式为 ;
②乙中A极析出的气体在标准状况下的体积为 ;
③反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要 mL5.0 mol•L—lNaOH 溶液。
(10分)已知磺酰氯(SO2Cl2)是一种有机氯化剂,SO2(g)+Cl2(g) SO2C12(g)
SO2C12(g) 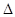 H<0,SO2Cl2是一种无色液体,熔点—54.1 ℃,沸点69.1 ℃,极易水解,遇潮湿空气会产生白雾。
H<0,SO2Cl2是一种无色液体,熔点—54.1 ℃,沸点69.1 ℃,极易水解,遇潮湿空气会产生白雾。
(1)化合物SO2Cl2中S元素的化合价是 。
(2)用二氧化锰和浓盐酸制氯气的化学方程式为 。
(3)用如图所示的装置制备SO2Cl2,下列说法正确是 (选填编号)
a.A、E处洗气瓶中盛放的可能分别是饱和食盐水和饱和NaHSO3溶液
b.B处反应管内五球中玻璃棉上的活性碳作催化剂
c.装置C处吸滤瓶应放在冰水中冷却,更有利于SO2Cl的收集
(4)B处反应管冷却水应从 (填“m”或“n”)接口通入,
从化学平衡移动角度分析,反应管通水冷却的目的是 ,D处U形管中盛放的试剂可以是 。
(5)向C中所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子只有SO42—、Cl—(OH—除外),写出SO2Cl2与H2O反应的化学方程式 。
(6)已知室温下,Ksp[AgCl]=2.0×10—10,Ksp[Ag2SO4]=1.6×10—5,在SO2Cl2溶于水所得溶液中逐滴加入AgNO3稀溶液,使SO42—和Cl—完全沉淀。当浊液中Ag+浓度为0.1 mol/L时,此浊液中Cl—与SO42—的物质的量浓度之比为 。
(8分)
Ⅰ.醋酸是常见的弱酸。用0.1 mol•L—1NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 mol•L—1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH体积而变化的两条滴定曲线。
(1)滴定醋酸的曲线是 (填“I”或“Ⅱ”)。
(2)滴定开始前,三种溶液中由水电离出的c(H+)最大的溶液名称是 。
(3)V1和V2的关系:V1 V2(填“>”、“=”或“<”)
(4)M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是 。
Ⅱ.草酸钴是制备钴的氧化物的重要原料。下图为二水合草酸钴(CoC2O4•2H2O)在空气中受热的质量变化曲线,曲线中300 ℃及以上所得固体均为钴氧化物。
(1)通过计算确定C点剩余固体的化学成分为 (填化学式)。试写出B点对应的物质与O2在225 ℃~300 ℃发生反应的化学方程式: 。
(2)取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL5 mol/L盐酸恰好完全溶解固体,得到CoCl2溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物质的量之比 。
选做(15分)【化学选修2:化学与技术】
硫酸铜在生产、生活中应用广泛。某化工厂用含少量铁的废铜渣为原料生产胆矾的流程如下: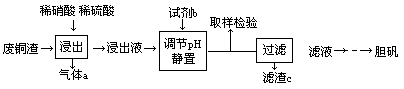
(1)“浸出”时,原料中的铜均转化为硫酸铜。写出相应的化学方程式: 。
(2)试剂b是 (填物质名称),其反应的离子方程式: 。
(3)调节pH的目的是 。滤渣c是 。
(4)在农业上,将胆矾、生石灰和水按一定比例混合制成波尔多液,其反应的化学方程式为 。
(5)气体a可以被循环利用,用化学方程式表示其被循环利用的原理为: 。
(6)一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和O2气体,写出硫酸铜受热分解的化学方程式: 。
选做(15分)【化学选修3:物质结构与性质】
原子序数依次增大的X、Y、Z、Q、E五种元素中,X元素原子核外有三种不同的能级且各个能级所填充的电子数相同,Z是地壳内含量(质量分数)最高的元素,Q原子核外的M层中只有两对成对电子,E+核外各能层电子均已充满。请回答下列问题:
(1)X、Y、Z的第一电离能由小到大的顺序为 。(用元素符号表示)
(2)已知YZ2+ 与XQ2互为等电子体,则l mol YZ2+ 中含有π键数目为 。
(3)Z的气态氢化物沸点比Q的气态氢化物高得多,其原因是 。
(4)Y、Z与氢元素可形成化合物HYZ3,是实验室常用试剂。HYZ3分子中Y的杂化方式为 ,YZ3—的空间构型是 。
(5)E原子的价层电子排布式为 ;E有可变价态,它的基价态的离子与Z的阴离子形成晶体的晶胞如图所示。
①该晶体的化学式为 ,Z的阴离子的配位数为 。
②Z的阴离子的堆积模型为 。
A.简单立方 B.六方最密 C.面心立方
③已知晶胞边长为apm,则晶胞的密度为 g• cm—3(阿伏加德罗常数用NA表示)。
选做(15分)【化学选修5:有机化学基础】
某芳香族化合物J常用作防腐剂,J可利用下列路线合成:
已知:①A的相对分子质量为92的烃
②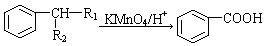 (—R1、—R2—表示氢原子或烃基)
(—R1、—R2—表示氢原子或烃基)
③
④D的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积之比为1:1。
回答下列问题:
(1)A的分子式为 ,由A→B的反应试剂和反应条件为 。
(2)写出C→D的反应方程式: 。
(3)同时符合下列条件的E的同分异构体共有 种。
①能发生银镜反应
②能使FeCl3溶液发生显色反应。
(4)F的结构式为 ,写出G→H的反应方程式: 。
(5)检验H中含氧官能团的试剂为 (填试剂名称),由H→I的反应类型为 。
(6)J的结构简式为 。
 的一氯代物种类有(不考虑立体异构)
的一氯代物种类有(不考虑立体异构) 粤公网安备 44130202000953号
粤公网安备 44130202000953号