X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的基态原子L层电子数是K层电子数的2倍 |
| Y |
Y的基态原子最外层电子排布式为:nsnnpn+2 |
| Z |
Z存在质量数为23,中子数为12的核素 |
| W |
W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)X的电负性比Y的______(填“大”或“小”);
(2)写出W的价电子排布式 写出Z2Y2与XY2反应的化学方程式, 当1摩尔Z2Y2参加反应时,转移电子的数目:______________。
(3)X、Y的原子可共同形成多种分子和某种常见无机阴离子,写出其中一种分子与该无机阴离子在水溶液中反应的离子方程式:______________。
(4)X元素的氢化物的沸点与同主族下一周期的元素的氢化物的沸点比较,沸点高的是 (写化学式)
有以下一系列反应,最终产物为草酸。已知B的相对分子质量比A的大79。
试回答下列问题:
(1)B的结构简式为__________, B→C的反应类型__________;
E→F的化学方程式:____________________________________________________。
(2)由B发生水解反应或C与H2O发生加成反应均生成化合物G。在乙二酸、水、苯酚、G四种分子中,羟基上氢原子的活泼性由强到弱的顺序是(请用“>”将四种物质的化学式连接起来表示)________________________________________________。
(3)MTBE是一种重要的汽油添加剂,它是1-戊醇的同分异构体,又与G的某种同分异构体互为同系物,且分子中含有四个相同的烃基。则MTBE的结构简式为_________,它的同类别同分异构体有___________种(包括它本身)。
已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1∶1。
请回答:
(1)组成A分子的原子的核外电子排布图是 ;
(2)B和C的分子式分别是 和 ;C分子的空间构型为 形,该分子属于 分子(填“极性”或“非极性”);
(3)向D的稀溶液中加入少量氯化铁溶液现象是 ,该反应的化学方程式为 ;
(4)若将1 mol E在氧气中完全燃烧,只生成1 mol CO2和2 mol H2O,则E的分子式是 。
(共14分)已知化合物A与B、丙与丁的组成元素分别相同,且四种物质中都含有同一种元素。A与B在常温下均呈液态。D与F都为固体单质,且D、 F与甲的浓溶液在常温下都会出现钝化现象,加热时有大量气体产生。(相关转化及部分反应条件和生成物未标出)。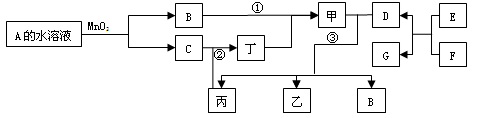
(1)A的结构式 , E与F的反应是 (填反应名称),写出2种该反应在工业生产中的用途: 、 。
(2)若反应①除生成甲外,还生成丙,写出过量D与甲的稀溶液反应的离子方程式:
(3)若A与丙可以化合生成甲;D与甲的浓溶液加热条件下可以生成三种化合物乙、丙、B,写出下列化学方程式②: ③:
2-甲基-2-丁烯酸甲酯是一种重要的化工原料。下面是该物质的一种合成路线: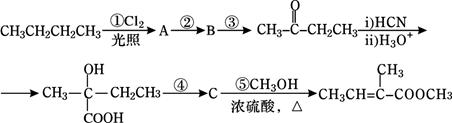
已知:R-CN 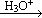 R-COOH。
R-COOH。
请回答下列问题:
(1)A是一氯代烷,则其结构简式为______________________;反应②的反应条件是_____________;
(2)写出反应③的化学方程式:____________________________________________;
(3)C的结构简式为______________,其所含官能团的名称是________________;
(4)步骤④的反应条件是_______________,反应类型是______________。
(5)2-甲基-2-丁烯酸甲酯的某种羧酸类链状同分异构体X,分子中含有3个甲基。则X的结构简式为 。
E的产量是衡量一个国家石油化工水平发展的标志,F为高分子化合物,能进行如图所示的反应。
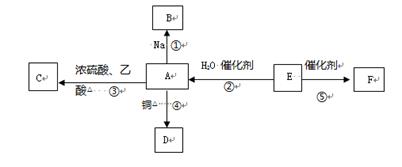
(1)请写出E的电子式 。
(2)下列反应的化学方程式:(要求有机物必须写结构简式)
反应②: ,反应类型 。
反应④: ,反应类型 。
反应⑤: ,反应类型 。
(3)比较反应①剧烈程度 (填>、= 或<)钠和水反应的剧烈程度。
短周期元素A、B、C、D、E、F原子序数依次增大,A与C可形成A2C2和A2C两种化合物;B的最高价氧化物对应的水化物甲与气体BA3化合生成离子化合物乙;D与A位于同一主族;E与C形成的化合物是大气污染物,容易形成酸雨;F元素最高化合价与最低化合价的代数和为6。
(1)E在元素周期表中的位置是 。
(2)由A、C、F三种元素按原子个数比1∶1∶1组成的化合物与BA3反应生成B的单质, 写出该反应的化学方式 。
(3)常温下,若甲、乙两溶液的pH均等于5,则由水电离出的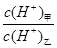 = ;乙溶液中所含离子的物质的量浓度由大到小的顺序是 。
= ;乙溶液中所含离子的物质的量浓度由大到小的顺序是 。
(4)用图所示装置电解由D与F形成盐的饱和溶液时,若阴、阳极都用铁作电极,则阳极的电极反应式为 ,溶液中出现的现象是 。
化合物 是鞘氨醇激酶抑制剂,其合成路线如图:
(1)化合物A的酸性比环己醇的_____(填“强”或“弱”或“无差别”)。
(2)B的分子式为 ,可由乙酸与 反应合成,B的结构简式为_____。
(3)A→C中加入 是为了结构反应中产生的_____(填化学式)。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:_____。碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使 酸性 溶液褪色;加热条件下,铜催化另一产物与氧气反应,所得有机产物的核磁共振氢谱中只有 个峰。
(5)G的分子式为 ,F→H的反应类型为_____。
(6)写出以 、
、 和
为原料制备
和
为原料制备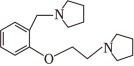 的合成路线流程图(须用
和
,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图(须用
和
,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
下列各物质转化关系如图所示,A是一种高熔点固体,D是一种红棕色固体。
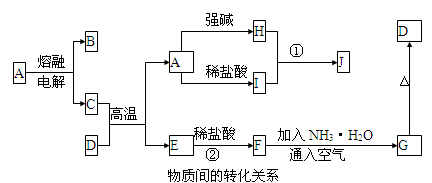
根据上述一系列关系回答:
(1)填写物质的化学式:B , G 。
(2)写出D物质中金属元素基态原子的核外电子排布图 。
(3)写出下列反应的离子方程式:
①H溶液和I溶液混合生成J___________ 。
②E和盐酸反应 。
(4)在电解熔融状态A的过程中,当电路中通过1mol电子时,阳极上产生的气体体积为 L。(标准状况下)
高分子材料E和含扑热息痛高分子药物的合成流程如下图所示:
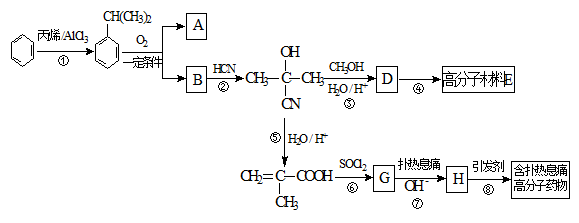
已知:I.含扑热息痛高分子药物的结构为: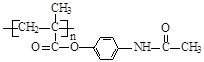 。
。
II.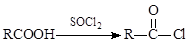
III.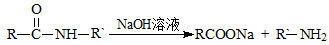
试回答下列问题:
(1)①的反应类型为____________,G的分子式为____________。
(2)若1 mol  可转化为1 mol A和1 mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式_____________。
可转化为1 mol A和1 mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式_____________。
(3)反应②为加成反应,则B的结构简式为__________;扑热息痛的结构简式为______________。
(4)写出含扑热息痛高分子药物与足量氢氧化钠溶液发生反应的化学方程式 。
(5)D蒸气密度是相同状态下甲烷密度的6.25倍,D中各元素的质量分数分别为碳60%,氢8%,氧32% 。D有多种同分异构体,其中属于链状酯类,且能发生银镜反应的同分异构体有_______种(考虑顺反异构)。
现有A、B、C、D、E五种原子序数依次增加的短周期元素,其中A的最低负价和最高正价代数和为零,且A2常温下为气态,B与其他元素形成的化合物种类最多,C与E可形成EC2和EC3两种物质,D是短周期最活泼的金属元素,用化学用语回答下列问题:
(1)D离子结构示意图_________________,B在元素周期表的位置_______________;
(2)A与C形成含18个电子的化合物的电子式是_______________;
(3)C与D形成的一种化合物颜色为淡黄色,其阴阳离子个数比为_____________,含有的化学键类型为___________;
(4)C、D、E的常见离子的离子半径由大到小的顺序__________________;
(5)B、E两元素得电子能力B________E(填“>”或“<”),试写出证明该结论的一个化学方程式_______;
(6)工业上常用氨水吸收尾气中的EC2,离子方程式为_______________________。
右图A→E是五种中学化学常见物质其中A、B、C、D常温下都是气体,B 为红棕色,A为气体单质。
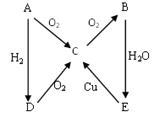
(1)写出化学式:B C
(2)实验室制备D实验中所用的干燥剂是: 。
(3)B与H2O反应,该反应的氧化剂和还原剂的物质的量之比为 。
(4)A与O2的反应方程式: ;D与O2的反应方程式:
;A与H2的反应方程式: 。
A、B、C、D、E为原子序数依次增大的短周期元素。A、C处于同一主族,C、D、E处于同一周期,E原子的最外层电子数是A、B、C原子最外层电子数之和,D是地壳中含量最高的金属元素;A、B组成的常见气体甲能使湿润的红色石蕊试纸变蓝;E的单质与甲反应能生成B的单质,同时生成两种水溶液均呈酸性的化合物乙和丙(该反应中氧化产物只有一种),25℃时0.1 mol/L的乙溶液pH>l;D的单质既能与C元素最高价氧化物的水化物的溶液反应生成盐丁,也能与丙的水溶液反应生成盐。
请回答下列问题:
(1)甲的化学式为 ;B单质的电子式为 。
(2)D元素的名称是 。
(3)写出丁溶液中通入过量二氧化碳时的离子方程式
(4)工业上利用A、B的单质合成甲(BA3):B2 (g)+3A2 (g)  2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=______________。
2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=______________。
(5)E的单质与甲反应生成的乙和丙的物质的量之比为2:4.反应中被氧化的物质与被还原的物质的物质的量之比为 。
A、B、C、D、X均为中学化学常见的物质。它们之间存在如下图所示转化关系(图中反应条件略去) 填写下列空白:

(1)若A为金属铝,B为氧化铁,写出反应A+B→C+D的一种用途 。
(2)若A为两性氢氧化物, B为NaOH溶液,写出反应A+B→C+D的离子方程式 。
(3)若A为金属单质,B、C、D都是化合物,A与B发生的反应常用于制作印刷电路板,该反应的离子方程式 。
(4)若A、B、C为化合物,D、X为单质,A、B、C中肯定含有X元素的是 。