测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数。现有下列实验用品:800mL烧杯、100mL量筒、短颈漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19g·L-1)、水。按图示装置进行实验,完成下列问题。(设合金样品完全反应,产生的气体体积不超过100mL)
补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在800 mL烧杯底部,把短颈漏斗倒扣在样品上面。
②________________。
③________________。
④________________。
某化学兴趣小组按照下列方案进行“由含铁废铝制备硫酸铝晶体”的实验:
步骤1:取一定量含铁废铝,加足量的NaOH溶液,反应完全后过滤。
步骤2:边搅拌边向溶液中滴加稀硫酸至溶液pH=8~9,静置、过滤、洗涤。
步骤3:将步骤2中得到的固体溶于足量的稀硫酸。
步骤4:将得到的溶液范发浓缩、冷却、结晶、过滤、干燥。
请回答以下问题:
(1)上述实验中的过滤操作需要玻璃棒、_______、_______等玻璃仪器。
(2)步骤1过滤的目的是______________。
(3)当步骤2中溶液的pH=8~9时,检验沉淀是否完全的方法是______________。
(4)步骤2中溶液的pH较难控制,可改用_______。
著名化学家罗伯特·波义耳(RobertBoyle)在一次实验中,不小心将盐酸溅到紫罗兰花瓣上,过了一会儿,他惊奇地发现,紫色的花瓣上出现了红点。波义耳对这一意外的发现作出了多种假设,经过多次实验验证,探究普遍规律,终于获得了成功。对紫罗兰花瓣遇盐酸变红的现象,你有哪些假设?请将你的各种假设以及验证假设的实验方案填写在下表中。
| 你对紫罗兰花瓣遇盐酸变红现象的各种假设 |
你验证假设的实验方案 |
| |
|
为探究淀粉的水解,某同学设计了下列实验:
银氨溶液,温水浴 现象A


 淀粉
淀粉  水解液
水解液  中和液
中和液
 碘溶液 现象B
碘溶液 现象B
⑴取少量反应液,用碱中和硫酸,加入银氨溶液,水浴加热,如果现象A是出现光亮的银镜,说明淀粉 (填“已水解”或“未水解”),反应的化学方程式为
⑵另取少量反应液,加入少量碘溶液,观察是否有颜色变化,如果无明显现象,证明淀粉已经 ,如果溶液出现蓝色,证明淀粉 (填“部分水解”或“完全水解”)
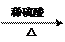 |
某课外活动小组利用如图所示装置分别做如下实验:

①在试管中注入某红色溶液,加热试管,溶液颜色变浅,冷却后
恢复红色,则原溶液可能是________________溶液;加热时溶液由红色逐渐变浅的原因是:_________________________。②在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色, 则此溶液可能是_____________溶液;加热时溶液由无色变为红色的原因是:__________________________________。
在学习“塑料、橡胶和纤维”时,我们对几种纤维的性质进行了科学探究。
①取一小块纯棉布、羊毛织物(或蚕丝织物)和尼龙布,分别在酒精灯火焰上灼烧,观察现象。②另取上述材料各一小块,分别浸入10%H2SO4溶液和3%NaOH溶液中,微热5~6min,取出用水漂洗、烘干。③把通过②处理过的织物与没有用酸、碱处理的织物进行对比。
回答下列问题:⑴完成实验现象记录表。
| |
灼烧情况 |
受10%H2SO4溶液影响情况 |
受3%NaOH溶液影响请况 |
| 纯棉布 |
易燃烧,有烧纸的气味,灰烬一触即碎 |
轻微 |
轻微 |
| 羊毛(或蚕丝织物) |
接近火焰卷缩,有 味,灰烬为黑色、膨胀易碎的颗粒 |
|
|
| 尼龙布 |
接近火焰卷缩,有特殊气味,趁热可拉成丝,灰烬为灰褐色玻璃球状 |
几乎不变 |
几乎不变 |
⑵通过本次探究,你认为合成纤维(如尼龙)与天然纤维相比较,其突出性能是 ;
⑶对于纯棉布、羊毛(或蚕丝)和尼龙布衣物,你认为可以在较高温度下熨烫的是 ;
⑷加酶洗衣粉中的碱性蛋白酶制剂可以使奶渍、血渍等多种蛋白质污垢降解成易溶于水的小分子肽。在洗涤纯棉布、羊毛(或蚕丝)和尼龙布衣物时,你认为不能使用加酶洗衣粉的是 。
将Zn投入一定浓度一定体积的盐酸中,H2的生成速率与时间的关系如图所示,试解释图中曲线变化的原因(纵坐标为H2的生成速率,横坐标为时间)。
答:① ;
② 。
有A、B、C三块金属浸泡在稀硫酸中,用导线两两相连要以组成各种原电池。若A、B相连,A为负极;B、C相连,B上有气泡逸出;A、C相连,A极减轻。则三种金属的活动性顺序由大到小排列为 。
向一个小烧杯中加入20克蔗糖,加3~4滴水,再加入20ml浓硫酸,观察到的实验现象是:烧杯发热、蔗糖变黑、体积膨胀,变成疏松多孔的海棉状的炭,并放出有制激性气味的气体。这个过程表现出浓硫酸的特性是 。
下图是教师演示的两个实验(铁架台等辅助仪器略去未画)。回答下列问题
(1)实验一的两烧杯中可以观察到的实验现象是:
I、 II、 。加热,试管里发生反应的化学方程式是:
(2)实验二用来验证Na2O2与CO2的反应,观察到的实验现象是:含有Na2O2的棉花燃烧。由该实验可以得出许多结论,请写出你所得出的两个结论:
结论1: 结论2:
某化学课外活动小组将氯化钠固体中混有的硫酸钠、碳酸氢铵杂质除去并得到氯化钠溶液,设计了如下方案:

|
|
|
某化学课外小组用下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1)写出A中反应的化学方程式______________________。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________________,写出有关的化学方程式__________________________________________________。
(3)C中盛放CCl4的作用是__________________。
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入________,现象是______________。
(安徽省芜湖市一中2008届高三第二次模拟考试,化学,16)下面a~e是中学化学实验中常见的几种定量仪器:
(a)量筒 (b)容量瓶 (c)滴定管 (d)托盘天平 (e)温度计
(1)其中标示出仪器使用温度的是 (填写编号)
(2)由于操作错误,使得到的数据比正确数据偏小的是 (填写编号)
A.实验室制乙烯测量混合液温度时,温度计的水银球与烧瓶底部接触
B.中和滴定达终点时俯视滴定管内液面读数
C.使用容量瓶配制溶液时,俯视液面定容所得溶液的浓度
(3)称取10.5g固体样品(1g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为 g。
有A、B、C三种不溶于水的固体。A是某元素的一种单质,它在氧气中完全燃烧得到一种无色气体,此气体能使澄清石灰水变浑浊,另外测得这种气体密度为同温、同压下氧气密度的1.375倍。B固体能溶于热氢氧化钠溶液,再往所得溶液中加入过量盐酸时,析出白色胶状沉淀。此沉淀干燥后,成为不溶于水的白色粉末,这是一种比碳酸酸性还弱的酸。将B与石灰石、纯碱按比例混合加热得到C,C在高温时软化,无固定熔点。







根据以上事实,判断A为哪种元素的单质?B、C各是什么物质?写出有关反应的化学方程式。