下图是教师演示的两个实验(铁架台等辅助仪器略去未画)。回答下列问题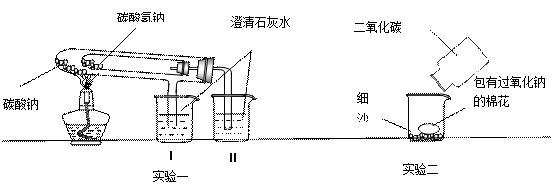
(1)实验一的两烧杯中可以观察到的实验现象是:
I、 II、 。加热,试管里发生反应的化学方程式是:
(2)实验二用来验证Na2O2与CO2的反应,观察到的实验现象是:含有Na2O2的棉花燃烧。由该实验可以得出许多结论,请写出你所得出的两个结论:
结论1: 结论2:
下图是教师演示的两个实验(铁架台等辅助仪器略去未画)。回答下列问题
(1)实验一的两烧杯中可以观察到的实验现象是:
I、 II、 。加热,试管里发生反应的化学方程式是:
(2)实验二用来验证Na2O2与CO2的反应,观察到的实验现象是:含有Na2O2的棉花燃烧。由该实验可以得出许多结论,请写出你所得出的两个结论:
结论1: 结论2: