(1)滑石一种硅酸盐矿物,其化学式为Mg3Si4O10(OH)2,用氧化物的形式表示为 。
(2)除去下列物质中所含杂质(括号内为杂质),写出除去杂质的试剂。
①Fe2O3(Al2O3) ②NO(NO2)
③Cl2 (HCl) ④FeCl3 (FeCl2)
(3)用铝箔包裹0.1mol金属钠,用针扎若干小孔,放入水中,完全反应后,用排水取气法收集到标准状况下气体的体积是_________(填字母序号)
a.1.12Lb.>1.12Lc.<1.12L
物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图所示,回答下列问题:
(1)Y是 (化学式)。
(2)将X与Y混合,可生成淡黄色固体,书写相关化学方程式 。
(3)将X的水溶液久置于空气中会变浑浊,说明X具有 性质。
(4)烧杯中加一些蔗糖,滴几滴水,并倒入一些W的浓溶液,用玻璃棒搅拌,观察到的所有现象为 ,说明W的浓溶液具有 、 和 性质。
(5)欲制备Na2S2O3,从氧化还原角度分析,合理的是 (填序号)。
a.Na2S + S b.Na2SO3 + S c.Na2SO3 + Na2SO4 d.SO2 + Na2SO4
【化学-选修3:物质结构与性质】
A、B、C、D、E五种常见元素的核电荷数依次增大。A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物,E的基态3d轨道上有2个电子。请回答下列问题:
(1)E的基态原子价层电子排布式为________________。
(2)AB2分子中,A的杂化类型为________________;在元素周期表中A、B及与两者紧邻的元素的第一电离能由大到小的顺序为(用元素符号表示)__________________。
(3)B的氢化物与D的氢化物的沸点较高的是____________(用化学式表示),原因是______________。
(4)AB2形成的晶体的熔点____________(填“高于”“低于”或“无法判断”)CD形成的晶体的熔点,原因是___________________。
(5)E与B形成的一种橙红色晶体晶胞结构如图所示,其化学式为____________(用元素符号表示)。ED4是制取航天航空工业材料的重要原料。取上述橙红色晶体,放在电炉中,通入D2和A的单质后高温加热,可制得ED4,同时产生一种造成温室效应的气体,写出反应的化学方程式:_________________________。
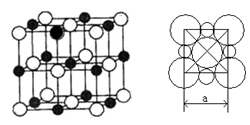
(6)由C、D两元素形成的化合物组成的晶体中,晶体结构图以及晶胞的剖面图如下图所示,若晶胞边长是acm,则该晶体的密度为____________g/cm3.(已知阿伏加德罗常数为NA)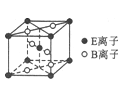
“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了高热值的煤炭气,其主要成分是CO和H2。CO和H2可作为能源和化工原料,应用十分广泛.生产煤炭气的反应之一是:C(s)+H2O(g) CO(g)+H2(g) H=+131.4kJ/mol
CO(g)+H2(g) H=+131.4kJ/mol
(1)在容积为3L的密闭容器中发生上述反应,5min后容器内气体的密度增大了0.12g/L,用H2O表示0~5min的平均反应速率为______________。
(2)关于上述反应在化学平衡状态时的描述正确的是___________.
A.CO的含量保持不变
B.v正(H2O)=v正(H2)
C.容器中混合气体的平均相对分子质量保持不变
(3)若上述反应在t0时刻达到平衡(如图),在t1时刻改变某一条件,请在图中继续画出t1时刻之后正反应速率随时间的变化: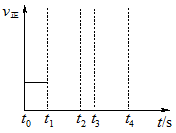
①缩小容器体积,t2时到达平衡(用实线表示);
②t3时平衡常数K值变大,t4到达平衡(用虚线表示).
(4)在一定条件下用CO和H2可以制得甲醇,CH3OH和CO的燃烧热分别为725.8kJ/mol,283.0kJ/mol,1molH2O(l)变为H2O(g)吸收44.0 kJ的热量,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式_______________________
(5)如下图所示,以甲醇燃料电池作为电源实现下列电解过程.乙池中发生反应的离子方程式为_____________。当甲池中增重16g时,丙池中理论上产生沉淀质量的最大值为_________g。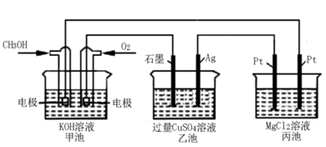
铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛.
(1)真空碳热还原氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g)△H="a" kJ•mol﹣1
3AlCl(g)═2Al(l)+AlCl3(g)△H="b" kJ•mol﹣1
①反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H= kJ•mol﹣1(用含a、b的代数式表示).
②Al4C3是反应过程中的中间产物.Al4C3与盐酸反应(产物之一是含氢量最高的烃)的化学方程式为 .
(2)镁铝合金(Mg17Al12)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg、Al单质在一定温度下熔炼获得.该合金在一定条件下完全吸氢的反应方程式为Mg17Al12+17H2═17MgH2+12Al.得到的混合物Y(17MgH2+12Al)在一定条件下可释放出氢气.
①熔炼制备镁铝合金(Mg17Al12)时通入氩气的目的是 .
②在6.0mol•L﹣1HCl溶液中,混合物Y能完全释放出H2.1mol Mg17Al12完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出H2的物质的量为 .
③在0.5 mol•L﹣1NaOH和1.0 mol•L﹣1MgCl2溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质X﹣射线衍射谱图如下图所示(X﹣射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同).在上述NaOH溶液中,混合物Y中产生氢气的主要物质是 (填化学式).
(3)铝电池性能优越,Al﹣AgO电池可用作水下动力电源,其原理如右下图(图2)所示.该电池反应的化学方程式为: .
t℃时,将3molA和1molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g) xC(g).2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g).2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)从反应开始至达到平衡状态,生成C的平均反应速率为 .
(2)x= ;平衡常数K= .
(3)若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母) .
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(4)若向原平衡混合物的容器中再充入amolC,在t℃时达到新的平衡,此时B的物质的量为n(B)= mol.
(5)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入三种物质的物质的量n(A)、n(B)、n(C)之间应该满足的关系式为 .
已知:2SO2 (g) + O2 ═ 2SO3 (g) △H = ﹣196.6kJ•mol﹣1 , 2NO (g) + O2 ═ 2 NO2(g) △H = ﹣ 113.0kJ•mol﹣1.则反应 NO2 (g) + SO2 (g) ═ SO3 (g) + NO (g) 的 △H= .
已知:下列两个热化学方程式:
Fe(s)+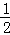 O2(g)═FeO(s)△H=﹣272.0KJ/mol
O2(g)═FeO(s)△H=﹣272.0KJ/mol
2Al(s)+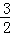 O2(g)═Al2O3(s)△H=﹣1675.7KJ/mol
O2(g)═Al2O3(s)△H=﹣1675.7KJ/mol
则 Al(s)的单质和FeO(s)反应的热化学方程式是 .
某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题: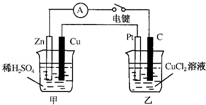
(1)甲装置的名称是 ;乙装置的名称是 ;Zn为 极;Pt为 极.
(2)写出电极反应式:Cu极 ;C极 .
(3)若乙中溶液不变,将其电极都换成铜电极,电键闭合一段时间后,乙中溶液的颜色 (填“变深”、“变浅”或“无变化”).
(4)若乙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将 (填“增大”、“减小”或“不变”,下同);乙中溶液的pH将 .
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中△H的表示生成1mol产物的数据).
根据图回答下列问题: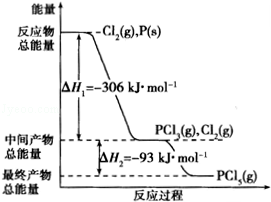
(1)P和Cl2反应生成PCl3的热化学方程式为: .
(2)PCl5分解成PCl3和Cl2的热化学方程式为: .
上述分解反应是一个可逆反应.温度为T1时,在密闭容器中加入0.80mol PCl5,反应平衡时PCl5还剩0.60mol,其分解率等于 .
(3)P和Cl2分两步反应生成1mol PCl5的△H3= ,P和Cl2一步反应生成1mol PCl5的△H4 △H3(填“大于”、“小于”或“等于”).
(4)PCl5与足量水反应,最终生成两种酸,其化学方程式为: .
(1)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出热量649.5 中kJ,则表示乙硼烷燃烧热的热化学方程为 .
又已知:H2O(l)═H2O(g);△H=+44.0kJ/mol.则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量为 .
(2)恒温、恒压(1.01×105Pa)下,将2.0molSO2与amolO2的混合气体通入一个容积可变的密闭容器中,发生如下反应:2SO2(g)+O2(g)⇌2SO3(g);△H<0,T1℃下反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol,则a= .
某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示.由图中数据分析:
(1)该反应的化学方程式: ;
(2)反应开始至2min末,X的反应速率为 ;
(3)平衡时Z的转化率为 .
(4)3min后图中曲线所表示的含义是 .
化学与人们生活质量的提高以及社会发展有着密切的关系.
(1)①保护环境已经成为全人类的共识.下列物质会破坏臭氧层的是 (填字母).
a.二氧化碳 b.二氧化硫 c.氮氧化物
②工业上制造水泥、玻璃和高炉炼铁都要用到的原料是 (填字母).
a.纯碱 b.石灰石 c.黏土
③光导纤维的主要成分是 (填化学式).
(2)泡沫铝是一种新型材料,它是在熔融的铝合金中加入发泡剂制成的,其优点是硬度高,密度小,比木材还轻,可浮于水面,又有很大的刚性,且隔音、保温,是一种良好的建筑材料和轻质材料.
①下列关于泡沫铝的说法错误的是 (填字母).
a.是纯净物 b.可用来制造飞机 c.可用作隔热材料
②铝元素在人体中积累可使人慢性中毒,1989年世界卫生组织正式将铝确定为食品污染源之一而加以控制.铝及其化合物在下列场合使用时必须加以控制的是 (填字母).
a.制电线电缆 b.用明矾净水 c.制防锈油漆
③铝在空气中能表现出良好的抗腐蚀性,是因为它与空气中的氧气反应生成 并牢固地覆盖在铝表面,阻止了内部的铝与空气接触,从而防止铝被进一步氧化.
(3)如图为实验室中盐酸试剂瓶标签上的部分内容.试回答下列问题:
①下列有关浓盐酸的说法中正确的是 (填字母).
a.属于含氧酸 b.和氯化氢的性质相同 c.很容易挥发
②该盐酸的c(HCl)为 L mol/L.
③欲用该盐酸配制1.19mol/L的盐酸480mL.请完成下列有关操作中的空白:
a.用量筒准确量取该盐酸 mL,注入烧杯中,加入适量的水,混合均匀;
b.将操作a所得的盐酸沿玻璃棒注入 mL容量瓶中;
c.用适量的水洗涤烧杯、玻璃棒2~3次,洗涤液均注入容量瓶中,振荡;
d.缓缓地将蒸馏水注入容量瓶中,直到瓶中的液面接近容量瓶的刻度线l~2cm处,改用 加蒸馏水至溶液的凹液面正好与刻度线相切;
e.将容量瓶盖好,反复上下颠倒摇匀.
近来,制备和利用氢气这一清洁能源已有多项成果。
(1)德国克莱斯公司成功研制了甲醇(CH3OH)制氢车载燃料电池工艺,其原理如下流程图所示:
①流程图中,甲醇与水在选择氧化器中反应生成二氧化碳和氢气,写出该反应的化学方程式
②该车载燃料电池的介质为碱性环境,请写出该燃料电池的正极反应式为
(2)美国Bay等工厂成功研制了以甲烷来制取氢气,其生产流程如下图:
①此流程的第Ⅱ步反应为:CO(g)+H2O(g) H2(g)+CO2(g),该反应的化学平衡常数表达式K=
H2(g)+CO2(g),该反应的化学平衡常数表达式K=
②此流程的第Ⅱ步反应的平衡常数随温度的变化如下表,在830 ℃、以表中的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有________(填实验编号)。
| 温度/℃ |
400 |
500 |
830 |
1 000 |
| 平衡常数K |
10 |
9 |
1 |
0.6 |
| 实验编号 |
n(CO) |
n(H2O) |
n(H2) |
n(CO2) |
| A |
1 |
5 |
2 |
3 |
| B |
2 |
2 |
1 |
1 |
| C |
3 |
3 |
0 |
0 |
| D |
0.5 |
2 |
1 |
1 |
③若400 ℃时,第Ⅱ步反应生成1 mol氢气的热效应值为33.2kJ,第Ⅰ步反应的热化学方程式为:CH4(g) + H2O(g) === 3H2(g) + CO(g) ΔH=-103.3 kJ·mol-1则400 ℃时,甲烷和水蒸反应生成二氧化碳和氢气的热化学方程式为:
(3)我国科学家研究了常温下利用Pt等催化剂在可见光作用下使水分解制氢气的方法,下图是三种催化剂在光照分解水实验中的效果比较图。
要得出如图所示的实验结果,需要测定的实验数据是 ,本实验的目的是 。
(1) 图中A为直流电源,B为浸透饱和氯化钠和酚酞溶液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色。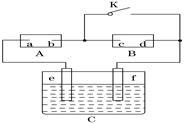
①电源A中a点为________极。
②滤纸B上发生的总反应的离子方程式为 。
③欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为 ,电镀槽中盛放的电镀液可以是________或________。
(2)加碘盐中的KIO3也可以用电化学氧化法制取:电解KI溶液可以制取KIO3。则电解时阳极材料可选用 (填“石墨”或“铜”)。写出该电极反应方程式