(4分)200℃时,11.6 g CO2和水蒸气的混合气体与足量的Na2O2充分反应后固体的质量增加了3.6 g ,求原混合气体中CO2和水蒸气的质量比
某有机化合物A含碳77.8%,氢为7.40%,其余为氧,A的相对分子质量为甲烷的6.75倍。求:
⑴该有机物的分子式。
⑵红外光谱测定,A分子结构中含有苯环和羟基。在常温下A可与浓溴水反应,1molA最多可与2molBr2作用,据此确定该有机物可能的结构简式。
恒温下,将a mol N2和b mol H2按一定比例混合,在相同状况下其密度是H2的 3.6倍,取5mol该混合气体通入密闭容器内,使之发生反应并在一定条件下达到平衡。已知反应达到平衡后容器内压强是相同条件下反应前压强的0.92倍,试求:
(1)反应前混合气体中N2和 H2的体积比a﹕b=__________;
(2)达到平衡时混合气体中的H2、NH3的物质的量分别是_____mol、_____mol;
(3)平衡时N2的转化率为 ________________。
一定量的氢气在氯气中燃烧,所得混合物用100 mL 3.00 mol·L-1的NaOH溶液(密度为1.12 g·mL-1)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500 mol。 (1)原NaOH溶液的质量分数为__________。
(1)原NaOH溶液的质量分数为__________。
(2)所得溶液中Cl-的物质的量为__________mol。
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl2)︰n(H2)__________。
在200mL稀硫酸和稀盐酸的混合溶液中,加入5.13g Ba(OH)2粉末,充分反应后过滤,得沉淀2.33g;又测知反应后的溶液中OH—的物质的量浓度为0.1mol·L—1。试求混合酸溶液中Cl—和SO42—的物质的量浓度。(假设反应前后溶液的总体积不变)
20mL0.20mol/L的某金属元素R(相对原子质量不小于20)的硫酸盐溶液与足量的BaCl2溶液反应后,产生的沉淀经干燥称重为9.23g,又知此金属0.24g与足量的盐酸反应,放出H2体积为0.224L(标准状况),求元素R相对原子质量。
根据反应8NH3 + 3Cl2 ="=" 6NH4Cl + N2 ,回答下列问题:
(1) 还原剂是 (写化学式);
(2) 用双线桥法表示该反应电子转移的方向和数目;
(3)当反应中转移1.806×1024个电子时,被氧化的气体在标准状况下的体积为 升
将70 g过氧化钠和氧化钠的混合物跟98 g水充分反应后,所得氢氧化钠溶液的质量分数为50%。计算原混合物中过氧化钠和氧化钠的质量各为多少克?
美籍埃及人泽维尔用激光闪烁照相机拍摄到化学反应中化学键断裂和形成的过程,因而获得1999年诺贝尔化学奖。激光有很多用途,例如波长为10.3微米的红外激光能切断B(CH3)3分子中的一个B—C键,使之与HBr发生取代反应.
B(CH3)3+HBr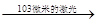 B(CH3)2Br+CH4
B(CH3)2Br+CH4
而利用9.6微米的红外激光却能切断两个B—C键,并与HBr发生二元取代反应。
(1)试写出由B(CH3)3和HBr反应生成其二溴代物的代学方程式.
(2)现用5.6g B(CH3)3和9.72g HBr正好完全反应,则生成物中除了甲烷外,其他两种产物的物质的量之比为多少?(请写出必要的计算过程)
已知可逆反应:请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=" 1" mol/L, c(N)="2.4" mol/L ;达到平衡后,M的转化率为60%,此时N的转化率为 ;
(2)若反应温度升高,M的转化率 (填“增大”“减小”或“不变”);
(3)若反应温度不变,反应物的起始浓度分别为:c(M)=" 4" mol/L,
c(N)=" a" mol/L;达到平衡后,c(P)="2" mol/L,a= ;
(4)若反应温度不变,反应物的起始浓度为:c(M) = c(N)=" b" mol/L,达到平衡后,M的转化率为_______。
c(N)=" b" mol/L,达到平衡后,M的转化率为_______。
计算题(每题3分,共9分)(1)浓度不等的两种硫酸溶液等质量混合时,其质量分数为a%,而等体积混合时为b%;浓度不等的两种乙醇溶液等质量混合后,其质量分数为a%,而等体积混合时则为c%。则a、b、c由大到小排序为
(2)由钾和氧组成的某种离子晶体含钾的质量分数是78/126,其阴离子只有过氧离子(O22-)和超氧离子(O2-)两种。在此晶体中,过氧离子和超氧离子的物质的量之比为
(3)有BaCl2和NaCl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀。反应中消耗x mol H2SO4、y mol AgNO3。据此得知原混合溶液中的c(Na+)为 mol/L。
(9分) 将标准状况下的11.2L氨气溶于100mL水中,得到密度为0.868 g·cm-3的氨水。
(1)该气体的物质的量= mol;溶液的体积= L;
所得氨水的物质的量浓度= mol·L-1。
(2)若取上述氨水30.0mL与70.0mL2.00mol·L-1的AlCl3溶液相混合,产生白色沉淀的质量是 g。
(3)若取某浓度的NaOH溶液50.0mL与50.0mL2.00mol·L-1的AlCl3溶液相混合,有白色沉淀产生,测得溶液中铝元素与沉淀中铝元素质量相等,则NaOH溶液的物质的量浓度为 mol·L-1
向50mL0.018mol/L的AgNO3溶液中,加入50mL0.02mol/L的盐酸,生成了沉淀.如果溶液中c(Ag+)、c(Cl-)的乘积是一个常数:Ksp =c(Ag+)•c(Cl-)=1.0×10-10,求:
(1)沉淀生成后溶液中c(Ag+)是多少?
(2)沉淀生成后溶液的pH值是多少?
(8分)在隔绝空气的条件下,某同学将一块部分被氧化的钠块用一张已除氧化膜、并用针刺一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待钠块反应完全后,在容器中仅收集到1.12 L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27g,水槽和容器内溶液的总体积为2.0 L,溶液中NaOH的浓度为0.050mol·L-1,(忽略溶液中离子的水解和溶解的氢气的量)。
(1)写出该实验中发生反应的化学方程式。
(2)试通过计算确定该钠块未氧化时的质量。(要求写计算步骤)