地球上海水资源丰富,但淡水资源紧缺。据专家们估计,地球表面积的71%是海洋,地球上淡水只占总水量的2.5%,而淡水中很大一部分又被南极洲、格陵兰和北极的冰山或冰川以冰的形式封存起来,剩下来的大部分为地下水。所有的湖泊、溪流、江河和雨水则仅占淡水总量的0.1%还不到。
(1)已知海洋的平均深度为3.8 km,地球的平均半径为6 371 km,海水的平均密度为1.03×103 kg/m3。你能估算地球上海水的总体积和海水的总质量吗?(用3位有效数字表示)
(2)你能估算地球上所有的湖泊、溪流、江河中淡水总质量吗?(用3位有效数字表示)
(3)地球上海水资源丰富,但淡水资源紧缺。你知道可用哪些物理方法淡化海水吗?
关于百慕大三角区之谜目前猜想是水合天然气引起的,在海底,由于温度低、压力大,动植物遗体腐烂变成的天然气与水结合,形成了固态的水合天然气。当这些水合天然气稳定的条件一旦受破坏,它们就可分解出气态天然气,以气泡上升。上升的气泡流导致海底压力变小,更多的固态水合天然气汽化,这样导致大量天然气溢出洋面。大量天然气气泡使海水密度变小,浮力下降,当船舶驶入这个区域时。海水浮力支撑不住船舶重力,而使船舰沉入洋底。飞机飞入这个地带,则可引燃天然气,而被烧毁坠入海中。
(1)把动植物遗体变成天然气的生物是生态系统中的什么成分?
(2)潜艇舱内各空气过滤口放了盛有Na2O2颗粒的装置,请说出该装置的用途并说明原理,写出化学反应方程式。有时潜艇也用KO2代替Na2O2,这有什么好处?试通过简单分析说明。
阳离子交换膜能在直流电场的作用下选择性地透过电解液中的阳离子使向阴极迁移,阴离子交换膜则能在直流电场的作用下选择性地透过电解液中的阴离子使向阳极迁移。同时在电解槽(称为“电渗析器”)中使用合适型号的这两种膜(简称“阳膜”和“阴膜”),可以在直流电场的作用下进行海水的电渗析脱盐而使海水淡化。
海水中主要离子的含量平均值如下:
Cl-18 980 mg·L-1,Na+:10 560 mg·L-1, :2 560 mg·L-1,Mg2+:1 272 mg·L-1,Ca2+:400 mg·L-1,K+:380 mg·L-1,HCO3-:142 mg·L-1
:2 560 mg·L-1,Mg2+:1 272 mg·L-1,Ca2+:400 mg·L-1,K+:380 mg·L-1,HCO3-:142 mg·L-1
海水在电渗析器中部分变成淡水的原理,示意图如图2-21所示电渗析器中由许多对阳、阴膜围成的许多“隔室”的宽度都很窄。脱盐时,各隔室相间流动着“淡水”和“浓水”;在流动着“极水”的以石墨为电极材料的两极发生电解反应。根据需要,可将几台电渗析器串联使用。图中标写的离子符号,提供思考其在电场中的迁移方向。
图2-21
回答下列问题:
(1)分别写出海水在电渗析器中脱盐时所得主要阳极产物和主要阴极产物的化学式。用以石棉布为隔膜的一般的惰性阳极电解槽来电解海水,能用以生产H2吗?为什么?
(2)致力于发展电渗析法、反渗透法等海水淡化新技术的直接社会效益是什么?
(3)已成功地联合应用海水淡化新技术和一般的离子交换树脂净水法,由海水制得纯水。又知海洋水能源(海洋水能发电)有其巨大的开发前景。你认为应怎样综合开发海洋能源,促成人类进入氢能时代?
工业上制取铝的流程如下:

注:冰晶石的作用是使E在较低温度下熔化。
(1)试写出下列物质的化学式:
A____________,B____________,C____________,D____________,E____________。
(2)在用此法制取铝时,分析铝土矿和赤泥(提取Al2O3之后的残渣)所得数据如下:
| Al2O3 |
Fe2O3 |
Na2O |
铝土矿 |
| 55% |
16% |
0% |
赤泥 |
| 15% |
48% |
8% |
|
试求制取1 t Al2O3所需铝矾土和苛性钠的质量。
聚甲基丙烯酸羟乙脂的结构简式为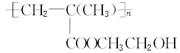 ,它是制作软质隐形眼镜的材料。请写出下列有关反应的化学方程式:
,它是制作软质隐形眼镜的材料。请写出下列有关反应的化学方程式:
(1)由甲基丙烯酸羟乙脂制备聚甲基丙烯酸羟乙脂。
(2)由甲基丙烯酸制备甲基丙烯酸羟乙脂。
(3)由乙烯制备乙二醇。
雷鸣电闪是日常生活中司空见惯的现象。设某次雷电中,两块云团间的电势差约为109 V,放电电量约为30 C。在闪电过程中,空气中有氮气和氧气直接化合,已知每摩尔氮气和氧气化合时要吸收180.74 kJ的能量,闪电时有1/1000的能量用于这一反应。试求:
(1)此次闪电所产生NO的物质的量为多少?
(2)此次雷雨闪电的生成物相当于给土壤施了多少千克尿素?
(10分)含CuSO4和H2SO4的混合溶液200 mL,其中CuSO4物质的量浓度为1 mol·L-1,H2SO4物质的量浓度为0.5 mol·L-1,若用此溶液配成0.2 mol·L-1 CuSO4和2 mol·L-1 H2SO4的混合溶液,试求:
(1)所得溶液的体积是多少毫升?
(2)需加入密度为1.84 g·cm-3,质量分数为98%的浓硫酸多少毫升?
2,4,5三氯苯酚和氯乙酸反应可制造除草剂2,4,5三氯苯氧乙酸。某生产该除草剂的工厂曾在一次事故中泄漏出一种有毒的二NF749英,简称TCDD。有关物质的结构式如下:


2,4,5三氯苯酚 氯乙酸 2,4,5三氯苯氧乙酸 TCDD
请写出:
(1)生成2,4,5三氯苯氧乙酸反应的化学方程式。
(2)由2,4,5三氯苯酚生成TCDD反应的化学方程式。
2个空格不要动 模块综合测试
(14分)利用天然气合成氨的工艺流程示意图如下:
依据上述流程,完成下列填空。
(1)天然气脱硫时的化学方程式是________________。
(2)n mol CH4经一次转化后产生CO 0.9n mol,产生H2________mol。(用含n的代数式表示)
(3)K2CO3(aq)和CO2反应在加压下进行,加压的理论依据是__________。(多选扣分)
a.相似相溶原理
b.勒夏特列原理
c.酸碱中和原理
(4)由KHCO3分解得到的CO2可以用于__________ (写出CO2的一种重要用途)。
(5)整个流程有三处循环,一是Fe(OH)3循环,二是K2CO3(aq)循环,请在上述流程图中标出第三处循环(循环方向、循环物质)。

(1)请写出加入NaOH溶液的体积由V2→V3时,所发生的化学反应方程式:___________________ _ _______,并由此计算合金中铝的质量。
(2)计算合金中镁的质量。
(3)合金在溶于稀硫酸时,释放出的气体体积(标准状况)是多少?
(4)康康同学所用稀硫酸的物质的量浓度是多少?
工业上常用漂白粉跟酸反应放出的氯气的质量分数x%来表示漂白粉的优劣。漂白粉与酸反应为:Ca(ClO)2+CaCl2+2H2SO4=2CaSO4+2H2O+2Cl2↑,又知I2与Na2S2O3溶液反应为I2+2Na2S2O3=Na2S4O6+2NaI。
现为了测定一瓶漂白粉的x%,进行了如下实验。称取漂白粉样品2.00g,加水研磨后,转入250mL容量瓶内,用水稀释至刻度。摇匀后,取出25.0mL,加入过量的KI溶液和过量的稀H2SO4,静置。待漂白粉放出的氯气与KI完全反应后,用0.100mol/L Na2S2O3溶液20.0mL。试由上述数据计算该漂白粉的x%。
工业上常用漂白粉跟酸反应放出的氯气的质量分数x%来表示漂白粉的优劣。漂白粉与酸反应为:Ca(ClO)2+CaCl2+2H2SO4=2CaSO4+2H2O+2Cl2↑,又知I2与Na2S2O3溶液反应为I2+2Na2S2O3=Na2S4O6+2NaI。
现为了测定一瓶漂白粉的x%,进行了如下实验。称取漂白粉样品2.00g,加水研磨后,转入250mL容量瓶内,用水稀释至刻度。摇匀后,取出25.0mL,加入过量的KI溶液和过量的稀H2SO4,静置。待漂白粉放出的氯气与KI完全反应后,用0.100mol/L Na2S2O3溶液20.0mL。试由上述数据计算该漂白粉的x%。
用消石灰与Cl2反应制漂白粉,假定消石灰100%转化为漂白粉。某游泳池消毒一次需要4.26 kg Cl2,现改用上述漂白粉,假定起消毒作用的是HClO,要达到与Cl2相当的消毒效果,需向游泳池中投放这种漂白粉多少千克?