根据下列化学方程式:①2FeCl3+2KI=2FeCl2+2KCl+I2, ②2FeCl2+Cl2=2FeCl3,判断各物质氧化性由大到小的顺序正确的是
| A.I2>Cl2>FeCl3 | B.Cl2>I2>FeCl3 | C.Cl2>FeCl3>I2 | D.FeCl3>Cl2>I2 |
下列各组物质的性质比较中,正确的是
| A.氢化物的沸点:HI>HBr>HCl>HF | B.稳定性:HF>HCl>HBr>HI |
| C.离子的还原性:I—>S2—>Br—>Cl— | D.单质的熔点:Li<Na<K<Rb |
日常生活中常用下列方法处理相关问题,其中不涉及化学变化的是
| A.硫酸钡作X光透视肠胃的药剂 |
| B.蜂蚁螫咬处涂抹稀氨水以消除疼痛 |
| C.用食醋蒸熏对房间消毒杀菌 |
| D.用明矾净化河水 |
下列各溶液中,微粒的物质的量浓度关系正确的是
A.10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合:
c(Cl-)>c(Na+)>c(OH-)>c(H+)
B.0.1 mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-)
D.c(NH4+)相等的(NH4)2SO4溶液.(NH4)2CO3溶液和NH4Cl溶液:c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl)
下列反应的离子方程式正确的是
|
A.氢氧化铁溶于氢碘酸中:Fe(OH)3 + 3H+ = Fe3+ + 3H2O
B.用惰性电极电解饱和食盐水:2Cl一 + 2H2O 2 OH一 + H2↑+ Cl2↑下列有关热化学方程式及其叙述正确的是
| A.氢气的燃烧热为-285.5kJ/mo1,则水电解的热化学方程式为: 2H2O(1) =2H2(g)+O2(g);△H=+285.5KJ/mo1 |
| B.1mol甲烷完全燃烧生成CO2和H2O(1)时放出890kJ热量,它的热化学方程式为 1/2CH4(g)+O2(g)= 1/2CO2(g)+H2O(1);△H= 一445kJ/mol |
| C.已知2C(s)+O2(g)=2CO(g);△H= 一221kJ·mol-1,则C的燃烧热为一110.5kJ/mo1 |
| D.HF与NaOH溶液反应:H+(aq)+OH—(aq)=H2O(1);△H= 一57.3kJ/mol |
一定能在下列溶液中大量共存的离子组是
| A.水电离产生的H+浓度为1×10-12mol·L-1的溶液:NH4+.Na+.Cl-.HCO3- |
| B.含有大量Fe3+的溶液:SCN-.I-.K+.Br- |
| C.能使pH试纸变蓝色的溶液:Na+.AlO2-.S2-.CO32- |
| D.澄清透明的无色溶液:ClO-.MnO4-.Al3+.SO42- |
设NA为阿佛加德罗常数,下列说法中正确的是
| A.0.1mol钠和O2在一定条件下反应生成Na2O和Na2O2混合物时,失去电子数为0.1NA |
| B.0.1mol铁和O2在一定条件下生成FeO和Fe2O3混合物时,失去电子数为0.2NA |
| C.标况下,1L乙醇完全燃烧时产生CO2的分子数为NA/11.2 |
| D.通常状态下,16克O2含氧原子数为0.5NA |
分类是学习和研究化学的一种常用的科学方法。下列分类合理的是
①根据酸分子中含有的H原子个数将酸分为一元酸.二元酸.多元酸
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③电解质:明矾.冰醋酸.纯碱;干冰.液氯都是非电解质
④同位素:1H.2H.3H;同素异形体:C60.金刚石.石墨
⑤根据分散系的稳定性大小将混合物分为胶体.溶液和浊液
| A.只有②④ | B.只有②③⑤ | C.只有①②④ | D.只有②③⑤ |
某化学反应其△H="=" —122 kJ/mol,∆S="=" 231 J/(mol·K),则此反应在下列哪种情况下可自发进行
| A.在任何温度下都能自发进行 | B.在任何温度下都不能自发进行 |
| C.仅在高温下自发进行 | D.仅在低温下自发进行 |
下列图示与对应的叙述相符的是
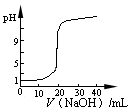
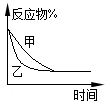

图1 图2 图3 图4
| A.图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 |
| B.图2表示0.1000 mol·L-1CH3COOH溶液滴定20.00mL0.1000 mol·L-1NaOH溶液所得到的滴定曲线 |
C.图3表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右 |
下列实验操作完全正确的是
| 编号 |
实验 |
操作 |
| A |
证明SO2有漂白性 |
将SO2气体通入紫色石蕊试液中,观察溶液是否退色 |
| B |
配制一定物质的量浓度的硫酸溶液1000mL |
准确量取一定体积浓硫酸,放入到1000mL的容量瓶中,加水稀释,振荡摇匀定容 |
| C |
除去FeCl3溶液中混有的FeCl2 |
向溶液中通入过量氯水,然后加热煮沸就得到了纯净的FeCl3溶液 |
| D |
检验Br—的存在 |
在溶液中先加入氯水再加入CCl4,振荡、静置,观察下层溶液显橙红色 |
高功率Ni/MH(M表示储氢合金)电池已经用于混合动力汽车。总反应方程式如下: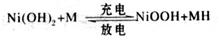
下列叙述不正确的是
| A.该电池放电时的正极和充电时的阴极均发生还原反应 |
| B.放电时负极反应为:MH+OH——e—=M+H2O |
| C.充电时阳极反应为:NiOOH+H2O+e—=Ni(OH)2+OH— |
| D.放电时每转移1mol电子,正极有1molNiOOH被还原 |
可逆反应A(s)+B(g)
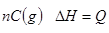 (n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如右图所示。下列有关叙述中一定正确的是
(n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线如右图所示。下列有关叙述中一定正确的是
A.其他条件相同,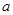 表示使用了催化剂, 表示使用了催化剂,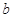 没有使用催化剂 没有使用催化剂 |
B.其他条件相同,若只改变压强,则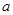 比 比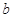 的压强大且 的压强大且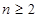 |
C.其他条件相同,若只改变温度,则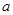 比 比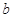 的温度高且Q>0 的温度高且Q>0 |
D.其他条件相同,若改变A的物质的量,则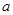 比 比 消耗A的物质的量少 消耗A的物质的量少 |