下列溶液中的Na+与50 mL 1 mol·L-1 Na3PO3溶液中Na+的物质的量浓度相等的是
| A.150 mL 3 mol·L-1 NaCl溶液 | B.75 mL 2 mol·L-1 NaNO3溶液 |
| C.150 mL 2 mol·L-1 Na2SO4溶液 | D.75 mL 1 mol·L-1的Na2S溶液 |
对于溶液中某些离子的检验及结论一定正确的是( )
| A.加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32- |
| B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C.加入足量稀盐酸,再加入氯化钡溶液后有白色沉淀产生,一定有SO42- |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸沉淀消失,一定有Ba2+ |
设阿伏加德罗常数的值为NA,下列说法中正确的是:
| A.标准状况下,2.24LCHCl3含有的分子数为0.1NA |
| B.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| C.0.1molCnH2n+2中含有的C-C键数为0.1nNA |
| D.1mol苯乙烯中含有的C=C数为4NA |
在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g/cm3,溶质的质量分数为w,溶质的物质的量浓度为c mol/L。下列叙述中正确的是( )
①w=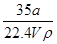 ×100%
×100%
②c=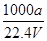
③向上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5 w
④向上述溶液中再加入1.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:
c(Cl-)> c(NH )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
| A.①③ | B.②③ | C.②④ | D.①④ |
某同学想用实验证明FeCl3溶液显黄色不是Cl-造成的,下列实验中无意义的是
| A.观察KCl溶液没有颜色 |
| B.加水稀释后FeCl3溶液黄色变浅 |
| C.向FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失 |
| D.向FeCl3溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液黄色消失 |
下列化学方程式不能用离子方程式2H++CO32-=H2O+CO2↑表示的是
| A.2HCl + Na2CO3 =" 2NaCl" + H2O+ CO2↑ |
| B.2HNO3 + BaCO3 = Ba(NO3)2 + H2O + CO2↑ |
| C.H2SO4 + Na2CO3 = Na2SO4 + H2O + CO2↑ |
| D.H2SO4 +(NH4)2CO3 = (NH4)2SO4 + H2O + CO2↑ |
在0.1 mol·L-1 CH3COOH溶液中存在如下电离平衡: CH3COOH CH3COO-+H+对于该平衡,下列叙述正确的是( )
CH3COO-+H+对于该平衡,下列叙述正确的是( )
| A.加入水时,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
下列事实中,不能用勒夏特列原理解释的是( )
| A.对熟石灰的悬浊液加热,悬浊液中固体质量增加 |
| B.实验室中常用排饱和食盐水的方式收集氯气 |
| C.打开汽水瓶,有气泡从溶液中冒出 |
| D.向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 |
反应A(g)+3B(g) 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
A.v(C)=0.04mol·(L·s)-1 B.v(B)=0.06mol·(L·s)-1
C.v(A)=0.03mol·(L·s)-1 D.v(D)=0.01mol·(L·s)-1
下列说法错误的是( )
| A.碱性锌锰电池是二次电池 |
| B.铅蓄电池是二次电池 |
| C.二次电池又叫蓄电池,它放电后可以再充电使活性物质获得再生 |
| D.燃料电池的活性物质没有储存在电池内部 |
可以充分说明反应P(g)+Q(g) R(g)+S(g)在恒温下已达到平衡的是( )
R(g)+S(g)在恒温下已达到平衡的是( )
| A.反应容器内的压强不随时间改变 |
| B.反应容器内P、Q、R、S四者浓度之比为1:1:1:1 |
| C.P的生成速率和S的生成速率相等 |
| D.反应容器内的气体总物质的量不随时间变化 |
用铂电极电解下列溶液时,阴极和阳极上的主要产物分别为H2和O2的是( )
| A.稀NaOH溶液 | B.HCl溶液 | C.CuSO4溶液 | D.AgNO3溶液 |
化学与日常生活紧密相关。下列说法中,不正确的是
| A.甲醛可作食品防腐剂 | B.氢氧化铝可作抗酸药 |
| C.氯化钠可作食品调味剂 | D.生石灰可作食品干燥剂 |
短周期元素X、Y、Z、W、Q的原子序数依次增大,且只有一种金属元素。其中X与W 处于同一主族,Z元素原子半径在短周期中最大(稀有气体除外)。Z与W、W与Q的原子序数之差均为3,五种元素原子的最外层电子数之和为21,下列说法正确的是
| A.Z、W、Q三种元素的单质属于三种不同的晶体类型 |
| B.Q氢化物的熔点高于Z氢化物的熔点 |
| C.一定条件下,Q单质可把Y从其氢化物中置换出来 |
| D.最高价氧化物对应水化物的酸性顺序:Q>Y>W>X |