老师用下图所示装置为同学们做了一个兴趣实验。已知装置B、C、D中依次盛有紫色石蕊试液、足量的澄清石灰水和稀盐酸。小资料:HCl气体极易溶于水。

(1)打开A中的玻璃塞和活塞,B中实验现象是 。B中的现象不能说明二氧化碳与水反应的原因是 。C中的化学反应的方程式是 。
(2)一段时间后,关闭A中的活塞和玻璃塞,打开弹簧夹K2及E中的玻璃塞和活塞,待足量的过氧化氢溶液流入锥形瓶后,立即关闭E中的活塞,并用弹簧夹K2夹紧橡皮管。C中可能出现的现象是 ,解释C中呈现的现象的原因是 。
(3)将A中产生的气体通入过量的NaOH溶液中,为了确定反应后的溶液中含有NaOH 的实验方法为 。
甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.
| 操 作 |
现 象 |
 |
I.A中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
(1)B中反应的离子方程式是 .
(2)A中溶液变红的原因是 .
(3)为了探究现象Ⅱ的原因,甲同学进行如下实验.①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在 .②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。甲同学的实验证明产生现象Ⅱ的原因是SCN﹣与Cl2发生了反应.
(4)甲同学猜想SCN﹣可能被Cl2氧化了,他又进行了如下研究.资料显示:SCN﹣的电子式为 。
。
①甲同学认为SCN﹣中碳元素没有被氧化,理由是 。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,此证明SCN﹣ 中被氧化的元素是 .
③通过实验证明了SCN﹣中氮元素转化为NO3﹣,他的实验方案是 .
④若SCN﹣与Cl2反应生成1mol CO2,写出反应离子方程式 并计算转移电子的物质的量是 mol。
过氧化钠(Na2O2)是中学常见物质,常见的过氧化物还包括过氧化钙(CaO2)。已知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成。有人提出CO2、SO2与过氧化钠的反应原理相同,但也有人提出SO2具有较强的还原性,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断。

实验一:向一定量的过氧化钠固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。
(1)提出假设:
假设1:反应后固体中只有Na2SO3,证明SO2未被氧化;
假设2:反应后固体中只有 Na2SO4,证明SO2完全被氧化;
假设3: ,证明 。
实验探究:
实验二:通过测量气体的体积判断发生的化学反应,实验装置如下:
(2)试剂A可以选用____________________,试剂B的作用是________________________。
(3)实验测得装置C中过氧化钠质量增加了m1g,装置D质量增加了m2g,装置E中收集到的气体为VL(已换算成标准状况下),用上述有关测量数据判断SO2未被氧化、完全被氧化的V-m1关系式。
未被氧化:____________________,完全被氧化:_______________________。
(4)若SO2完全被氧化,写出反应的化学方程式: __________________________。
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通过实验来探究一红色粉末可能是Fe2O3、Cu2O或二者混合物。探究过程如下:
【查资料】Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。
【提出假设】假设1:红色粉末是Fe2O3。假设2:红色粉末是Cu2O。假设3:两者混合物。
【设计探究实验】取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂。
设1成立,则实验现象是__________________________________。
(2)若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为
这种说法合理吗?____________,简述你的理由(不需写出反应的方程式)_______________。
(3)若粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则原固体粉末是_____________。
【探究延伸】经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。
(4)实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再
变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为____________________。
[化学]三氧化二铁和氧化亚铜是红色粉末,常作颜料。某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者的混合物。探究过程如下:
查阅资料知:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。
提出假设:假设 l:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计实验:取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN溶液。
(1)若假设1成立,则实验现象是__
(2)若滴入 KSCN溶液后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为这种说法合理吗?_____________。筒述你的理由
(3)若固体粉末完全溶解无固体存在,滴加KSCN溶液时溶液不变红色,则证明原固体粉末是Fe2O3和Cu2O的混合物,则其质量比为__ _,写出其中发生的氧化还原反应的离子方程式 。探究延伸:经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。
(4)实验小组欲用加热法测定Cu2O的质量分数。取ag固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg ,则混合物中Cu2O的质量分数为 。
,则混合物中Cu2O的质量分数为 。
附加题某学生对SO2与漂粉精的反应进行实验探究:
| 操作 |
现象 |
| 取4 g漂粉精固体,加入100 mL水 |
部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH |
pH试纸先变蓝(约为12),后褪色 |
 |
i.ii.稍后,出现浑浊,溶液变为黄绿色; iii.稍后,产生大量白色沉淀,黄绿色褪去 液面上方出现白雾; |
(1)Cl2和Ca(OH)2制取漂粉精的化学方程式是__________________________。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是____________________。
(3)向水中持续通入SO2,未观察到白雾。推测现象i的白雾由HCl小液滴形成。进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀。
① 实验a的目的是__________________________。
②由实验a、b不能判断白雾中含有HCl,理由是________________________
(4)现象ii中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应。通过进一步实验确认了这种可能性,其实验方案是_________________________
(5)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaCl2溶液,产生白色沉淀。则沉淀X中含有的物质是____________________
②用离子方程式解释现象iii中黄绿色褪去的原因:_________________ ____________
左图是某同学在实验室中进行铝热反应(铝过量)的实验装置,实验中可观察到的现象之一为“纸漏斗的下部被烧穿,有熔融物落入沙中”。

(1)试剂A的名称是 。
(2)探究铝热反应后固体的性质:将反应后容器中的残余固体置于烧杯中,加入100mL稀硝酸,固体完全溶解,(假设固体全部溶解后溶液体积不变),反应过程中无气体放出(活泼金属可把稀 HNO3还原为NH4NO3)。向反应后的溶液中缓慢滴加4 mol·L-1的NaOH溶液,产生沉淀的物质的量与加入 NaOH溶液 的体积的关系如上右图所示:
①写出DE段发生反应的离子方程式:___________________________
②求c(HNO3)= _____③B与A的差值为_________________
(3)若铝和氧化铁能恰好完全反应。则该铝热剂与盐酸反应时转移电子与所耗H+的物质的量之比
硫酸工业产生的废气A(主要成分:SO2、O2、N2、CO2等)排放到空气中会污染环境。某化学兴趣小组对废气A的组成进行探究,请回答下列问题。
(1)同学甲设计实验检验废气A中含有CO2,应选择的试剂有 。
| A.NaOH溶液 | B.酸性KMnO4溶液 | C.澄清石灰水 | D.盐酸 |
(2)同学乙欲测定废气A中SO2的含量,取a L废气A并设计了如下装置进行实验。

①为了保证实验成功,装置A应具有的现象是 ,搅拌的目的是 。
②同学丙认为A装置前后的质量差就是a L废气中含有的SO2的质量,然后进行含量计算。经小组讨论后,同学丁提出疑问,按照同学丙的实验,若废气中SO2完全被吸收,则最后测定的结果应该偏大,同学丁推断的理由是 。
(3)兴趣小组的同学查阅资料发现可利用硫酸工业废气A制备皓矾(ZnSO4•7H2O)。实验模拟制备皓矾工业流程如下:

①“氧化”中加入硫酸铁发生反应的离子方程式是 。
②加入Zn粉的目的是 。
③固体A主要成分是 。
④操作b得到纯净皓矾晶体,必要的操作是 、 、过滤、洗涤、干燥。
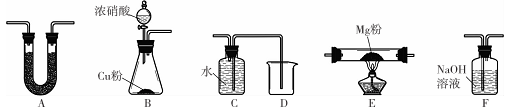
(12分)铝热反应是铝的一个重要性质。某校化学兴趣小组同学为了克服传统铝热反应纸漏斗易燃烧,火星四射等缺点,将实脸改成以下装置,取磁性氧化铁在如图A实验进行铝热反应,冷却后补到“铁块”混合物.

(1)实验中可以用蔗糖和浓硫酸代替镁条作引火剂,共原因是 。
(2)该铝热反应的化学方程式为 。
(3)取反应后的“铁块”研碎取样称量,加入如图B装置,滴入足量NaOH溶液充分反应,测量生成气休体积以测量样品中残留铝的百分含量.试回答下列问题:
①量气管的量具部分是一个中学实验常见量具改装而成,该仪器的名称为 。
②量气管在读数时必须进行的步骤是 。
③取1g样品进行上述实验,共收集到44.8mL气体(换算成标准状况下),则铝的百分含量为 。
④装置中分液漏斗上端和烧瓶用橡胶管连通,除了可以平衡压强让液体顺利滴入试管之外,还可以起到降低实验误差的作用。如果装置没有橡胶管,测出铝的百分含量将会 (填“偏大”或“偏小”)。
Mg能在NO2中燃烧,产物为Mg3N2、MgO和N2。某科学小组通过实验验证反应产物并探究产物的比例关系。资料信息:
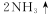
限用如下装置实验(夹持装置省略,部分仪器可重复使用)
(1)装置连接的顺序为 (填字母序号);
(2)连接好仪器,装入药品前检验装置气密性的方法是____;
(3)装置A中盛装的干燥剂是 ;装置F的作用__ __;
(4)验证产物中存在Mg3 N2的具体实验操作为 .确定产物中有N。生成的实验现象为 ;
(5)已知装置E中初始加入Mg粉质量为13.2 g,在足量的NO2中充分燃烧,实验结束后,硬质玻璃管冷却至室温、称量,测得硬质玻璃管中剩余固体的质量为21.0 g,产生N2的体积为1120 mL(标准状况)。写出玻璃管中发生反应的化学方程式:_ _。
(1)已知反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下:
| 实验编号 |
实验温度/℃ |
c(Na2S2O3)/mol·L-1 |
V(Na2S2O3)/mL |
c(H2SO4)/mol·L-1 |
V(H2SO4)/mL |
V(H2O)/mL |
| ① |
25 |
0.1 |
5.0 |
0.1 |
10.0 |
a |
| ② |
25 |
0.1 |
10.0 |
0.1 |
10.0 |
0 |
| ③ |
25 |
0.2 |
5.0 |
0.1 |
5.0 |
b |
| ④ |
50 |
0.2 |
5.0 |
0.1 |
10.0 |
5.0 |
其他条件不变时:探究温度对化学反应速率的影响,应选择实验 (填实验编号);若同时选择实验①②、实验②③,测定混合液变浑浊的时间,可分别探究Na2S2O3浓度和H2SO4的浓度对化学反应速率的影响,则表中a和b分别为 和 。
(2)某同学设计如下实验流程探究Na2S2O3的化学性质。

实验操作①中测试时pH试纸的颜色应该接近 。
A.红色 B.黄色 C.深蓝色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的 性。
铝热反应是铝的一个重要性质。某校化学兴趣小组同学为了克服传统铝热反应纸漏
斗易燃烧,火星四射等缺点,将实验改成以下装置,取磁性氧化铁在如图A实验进行铝热反应,冷却后得到“铁块”混合物.
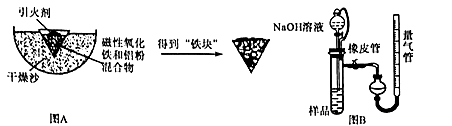
(1)实验中可以用蔗糖和浓硫酸代替镁条作引火剂,共原因是 。
(2)该铝热反应的化学方程式为 。
(3)取反应后的“铁块”研碎取样称量,加入如图B装置,滴入足量NaOH溶液充分反应,测量生成气体体积以测量样品中残留铝的百分含量.试回答下列问题:
①量气管的量具部分是一个中学实验常见量具改装而成,该仪器的名称为
②量气管在读数时必须进行的步骤是 。
③取1g样品进行上述实验,共收集到44.8mL气体(换算成标准状况下),则铝的百分含量为 。
④装置中分液漏斗上端和试管用橡胶管连通,除了可以平衡压强让液体顺利滴入试管之外,还可以起到降低实验误差的作用。如果装置没有橡胶管,测出铝的百分含量将会 填“偏大”或“偏小”)。
(13分)三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者的混合物。探究过程如下:
查阅资料:Cu2O溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO
提出假设
假设l:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
(1)若假设1成立,则实验现象是 (2分)。
(2)若假设2成立,则实验现象是有 (2分)。
(3)若固体放入足量稀硫酸中,经充分反应后,固体全部溶解,滴加KSCN试剂时,溶液不变红色,则证明假设 (1分)(填数字)成立,写出可能发生的离子方程式 (6分)。
(4)经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。实验小组欲用加热法测定Fe2O3的质量分数。取ag固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Fe2O3的质量分数为 (2分)。
己知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
回答下列问题:
(1)A中生成氨气反应的化学方程式是 _________________;
(2)B中加入的干燥剂是_______(填序号)①浓硫酸②无水氯化钙③碱石灰;
(3)能证明氨与氧化铜反应的现象:①C中______、②D中有无色液体生成;
设计实验检验D中无色液含有水:取少量液体于试管中,加入少量_______粉末,现象为______。
(4)写出氨气与氧化铜反应的化学方程式 _______________。若收集到2.24L(STP)氮气,计算转移电子数为______________。
下图是实验室中制备气体或验证气体性质的装置图

(1)写出用发生装置A中制取氯气的化学方程式______________。
(2)利用上图装置制备纯净的氯气,并证明氧化性:C12>Fe3+,则装置B中的溶液的作用是______;装置D中加的最佳试剂是(填序号)_________________:
供选试剂:a.浓H2SO4 b.FeCl2溶液 c.KSCN与FeCl2的混合溶液 d.无水氯化钙
(3)在上图所示圆底烧瓶内加入碳,a中加入浓硫酸,开始实验,加热产生的气体缓慢通过后续装置同时完成如下实验:
实验1:证明SO2具有氧化性和漂白性
实验2:证明碳元素的非金属性比硅元素的强
证明SO2具氧化性和漂白性:B中为少量Na2S溶液、C中加品红溶液,D中应加入足量的___________(填溶液名称),E中加入___________溶液(填化学式)。
(4)证明碳元素的非金属性比硅元素的强的现象为_________;实验2不严谨之处应如何改进________。