下列事实不能用金属活动性解释的是:
| A.生活中可用铝制的水壶烧水 |
| B.镀锌铁制品破损后,镀层仍能保护铁制品 |
| C.工业上常用热还原法冶炼铁,用电解法冶炼钠 |
| D.电解法精炼铜时,其含有的Ag、Au杂质沉积在电解槽的底部 |
下列关于铁电极的说法中,正确的是
| A.钢铁的吸氧腐蚀中铁是正极 | B.在铁片上镀铜时铁片作阳极 |
| C.电解饱和食盐水时可用铁作阴极 | D.镀锌铁板发生电化学腐蚀时铁是负极 |
下列叙述的原因不是由于原电池造成的是
| A.运输液氯的铁管被腐蚀 | B.金属在潮湿空气中更容易腐蚀 |
| C.铁与酸反应滴加硫酸铜后反应加快 | D.含杂质的锌比纯锌与酸反应快 |
下列说法正确的是
| A.在CuSO4溶液中加入PbS,可转变为铜蓝(CuS),则Ksp(PbS)<Ksp(CuS) |
| B.在NaHS溶液中,加入少量CuCl2粉末产生黑色沉淀,则pH增大 |
| C.加热条件下并加入大量水促进TiCl4水解,以制备TiO2固体 |
| D.铜制器皿放置过程中会生成铜绿是因为发生了析氢腐蚀 |
如图是模拟电化学反应装置图。下列说法正确的是( )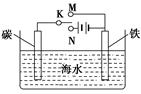
| A.开关K置于N处,则铁电极的电极反应式为:Fe-2e-=Fe2+ |
| B.开关K置于N处,可以减缓铁的腐蚀 |
| C.开关K置于M处,则铁电极的电极反应式为:2Cl--2e-=Cl2↑ |
| D.开关K置于M处,电子从碳棒经开关K流向铁棒 |
下列描述不符合生产、生活实际的是
| A.家用炒锅残留盐溶液时易发生吸氧腐蚀 |
| B.电解法精炼粗铜,用纯铜作阴极 |
| C.电解水制氢气时,用铜作阳极 |
| D.在镀件上电镀锌,用锌作阳极 |
化学用语是学习化学的重要工具,下列化学用语中正确的是
A.Na2S的水解:S2-+ 2H2O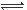 H2S + 2OH- H2S + 2OH- |
B.NaHCO3的电离:NaHCO3 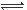 Na + + H+ + CO32- Na + + H+ + CO32- |
C.HSO3-的电离:HSO3- 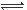 H+ + SO32- H+ + SO32- |
| D.钢铁的电化学腐蚀的负极反应式:Fe-3e-Fe3+ |
据环保部门测定,我国一些大城市的酸雨pH=3.5。在酸雨季节铁制品极易腐蚀,则在其腐蚀中正极发生的反应是 ( )。
| A.Fe-2e-=Fe2+ |
| B.2H2O+O2+4e-=4OH- |
| C.2H++2e-=H2↑ |
| D.4OH--4e-=2H2O+O2↑ |
下列叙述错误的是
| A.生铁中含有碳,抗腐蚀能力比纯铁弱 |
| B.铁在潮湿空气中发生腐蚀,其负极反应是2H++2e-=H2↑ |
| C.用锡焊接的铁质器件,焊接处易生锈 |
| D.铁管上镶嵌锌块,铁管不易被腐蚀 |
下列事实不能用电化学理论解释的是
| A.轮船水线以下的船壳上镶嵌有一定量的锌块 |
| B.黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| C.锌跟稀硫酸反应制取氢气,加入少量硫酸铜能加快反应速率 |
| D.铝在空气中不易腐蚀,不用特殊方法保存 |
在面盆、痰盂等铁制品表面烧制搪瓷的目的是
| A.防止铁生锈且美观 | B.增大厚度防止磨损 |
| C.增大硬度防止撞坏 | D.美观及杀菌消毒作用 |
钢铁腐蚀发生得最普遍的是
| A.化学腐蚀 | B.析氢腐蚀 | C.吸氧腐蚀 | D.摩擦损耗 |
如图,缠上金属条的铁钉插在含有酚酞的NaCl溶液中,可以看到在金属条表面的溶液出现粉红色。该金属条可能是 ( )。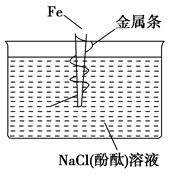
| A.铜 | B.镁 | C.铝 | D.锌 |
制造焊锡时,把铅加进锡的重要原因是
| A.增加强度 | B.降低熔点 | C.增加硬度 | D.增强抗腐蚀能力 |