向盛有一定量的Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)近似的用下图中的曲线表示是( )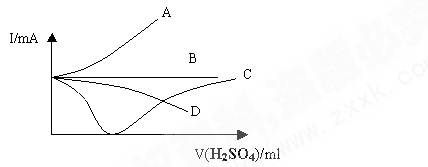
有关电解质的说法正确的是 ( )
| A.纯水的导电性很差,所以水不是电解质 |
| B.SO3水溶液的导电性很好,所以SO3是电解质 |
| C.液态的铜导电性很好,所以铜是电解质 |
| D.Na2O液态时能导电,所以Na2O是电解质 |
下列电离方程式,书写正确的是
| A.Al2(SO4)3 =2Al3+ + 3SO42- | B.Na2CO3= Na++ CO32 |
| C.Mg(NO3)2 = Mg+2 +2NO3- | D.KMnO4 =K+ +Mn7+ +4O2- |
关于强弱电解质的叙述不正确的是
| A.强电解质在溶液中完全电离,不存在电离平衡 |
| B.同一弱电解质溶液,温度不同时,导电能力不同 |
| C.强电解质溶液导电能力一定很强,弱电解质溶液导电能力一定很弱 |
| D.强电解质在固态或液态时,可能不导电 |
下列各组物质的水溶液均能导电,但前者属是电解质、后者属于非电解质的是
| A.CuSO4、HCl | B.CH3COOH 、Na2O |
| C.NaClO 、NH4HCO3 | D.NaCl、 NH3 |
三种正盐的混合溶液中含有0.2molNa+,0.25molMg2+,0.4molCl—,则SO42—的物质的量为
| A.0.1 mol | B.0.3 mol | C.0.5 mol | D.0.15 mol |
向0.1mol·L-1的H2SO4溶液中滴入0.1mol·L-1过量的Ba(OH)2溶液,溶液的导电能力发生变化,其电流强度(1)随加入Ba(OH)2溶液的体积(V)的变化曲线正确的是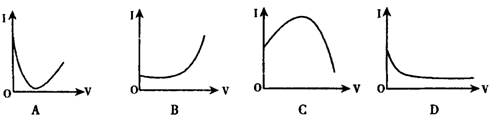
下列叙述正确的是
A.氯化钠溶液在电流作用下电离成氯离子和钠 离子 离子 |
| B.溶于水后电离出氢离子的化合物都是酸 |
| C.硫酸钡难溶于水.但硫酸钡是强电解质 |
| D.氨气溶于水能部分电离,故氨气属于弱电解质 |
下列电离方程式书写正确的是 ( )
A.HClO  H+ + ClO H+ + ClO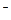  |
B.H2SO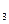  2H+ + SO 2H+ + SO |
C.Ba(OH)2 ="===" Ba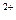 +2O +2O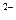 +2H +2H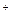 |
D.NaHCO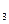 ====Na ====Na +H +H +CO +CO |
某化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2
连接好线路发现灯泡亮,由此得出的结论正确的是
| A. NaCl是非电解质 |
| B. NaCl溶液是电解质。 |
| C. NaCl在水溶液中电离出了可以自由移动的离子。 |
| D. NaCl溶液中水电离出大量的离子 |
下列电离方程式,书写正确的是( )
A. Al2(SO4)3 =2Al3+ + 3SO42- B.AlCl3 = Al3++ Cl3-
D. Mg(NO3)2 = Mg+2 +2NO3- D.KMnO4 =K+ +Mn7+ +4O 2-
2-