下列关于电解质的说法正确的是
| A.Cu能导电,所以Cu是电解质 |
| B.液态HCl不导电,所以HCl不是电解质 |
| C.NH3溶于水形成的溶液能导电,所以NH3是电解质 |
| D.BaSO4在水溶液中难导电,但熔融下能导电所以BaSO4是电解质 |
分,每空有四瓶失去标签的溶液A、B、C、D,它们可能分别是硫酸、盐酸、碳酸钠和硝酸钾溶液中的某一种。各取少量分别放入四支试管里,先向各试管中滴加BaCl2溶液,则A、B有白色沉淀,C、D无明显现象,再向A、B白色沉淀中加入稀硝酸,则A试管中白色沉淀溶解,并有无色气体产生,B试管无变化。另取C、D各少量,分别加入AgNO3溶液,则C试管有白色沉淀,D试管无变化。由此判断:(填化学式)
A. B. C. D.
下列关于物质分类的说法正确的是( )
| A.根据酸分子中含有的氢原子个数、将酸分为一元酸、二元酸和多元酸 |
| B.根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素 |
| C.铝热剂、福尔马林、水玻璃、漂白粉均为混合物 |
| D.明矾、水银、烧碱、硫酸均为强电解质 |
不用其它试剂鉴别①KNO3 ②Ba(OH)2 ③MgSO4 ④CuSO4四种溶液,正确的鉴别顺序是
| A.①④③② | B.④①③② | C.④②③① | D.①③④② |
下列有关说法正确的是
| A.在同温同压下,相同体积的任何气体含有相同数目的原子 |
| B.氧化还原反应的本质是有电子转移 |
| C.Na2SO4溶液在电流作用下电离出Na+与SO42-而导电 |
| D.NaCl固体不导电,所以NaCl不是电解质 |
现有以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④汞 ⑤BaS04固体 ⑥纯蔗糖 ⑦酒精⑧熔化的KNO3.请回答下列问题(用序号)
(1)以上物质能导电的是 .
(2)以上物质中属于电解质的是 .
(3)以上物质中属于非电解质的是 .
(4)以上物质溶于水后形成的水溶液能导电的是 .
今有七种物质:①铝片 ②KNO3 ③氯气 ④NaCl晶体 ⑤液态氯化氢 ⑥石灰水 ⑦乙醇,属于电解质的是 ,属于非电解质的是 。
室温下,向10mLpH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
| A.溶液中导电粒子的数目减少 |
| B.溶液中C(OH-)增大 |
| C.醋酸的电离程度增大,C(H+)亦增大 |
| D.再加入10mLpH=11的NAOH溶液,混合液的pH=7 |
【化学ーー选修2:化学与技术】
高锰酸钾( )是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主要成分为 )为原料生产高锰酸钾的工艺路线如下:
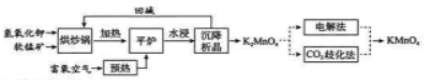
回答下列问题:
(1) 原料软锰矿与氢氧化钾按 的比例在 "烘炒锅"中混配,混配前应将软锰矿粉碎, 其作用是 。
(2) "平炉"中发生的化学方程式为 .
(3)"平炉"中需要加压,其目的是 。
(4) 将 转化为 的生产有两种工艺。
① 歧化法" 是传统工艺, 即在 溶液中通入 气体, 使体系呈中性或弱碱性,
发生歧化反应,反应中生成 和 (写化学式)。
② "电解法" 为现代工艺, 即电解 水溶液, 电解槽中阳极发生的电极反应为 , 阴极逸出的气体是_ 。
③ "电解法" 和 歧化法" 中, 的理论利用率之比为 _ 。
(5)高锰酸钾纯度的测定:称取 样品, 溶解后定容于 容量瓶中, 摇匀。取浓度为 的 标准溶液 , 加入稀硫酸酸化,用 溶液平行滴定三次, 平均消耗的体积为 , 该样品的纯度为 。
(列出计算式即可, 已知 ) 。
化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。装置中的离子膜只允许 离子通过,氯气的逸出口是 (填标号)。
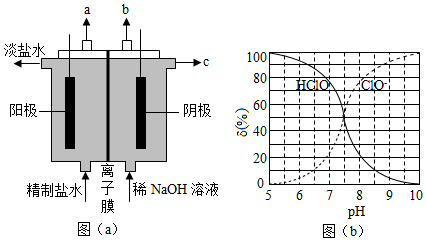
(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数δ[δ(X) ,X为HClO或ClO ﹣]与pH的关系如图(b)所示。HClO的电离常数K a值为 。
(3)Cl 2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl 2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl 2O的化学方程式为 。
(4)ClO 2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO 2、NaHSO 4、NaHCO 3的"二氧化氯泡腾片",能快速溶于水,溢出大量气泡,得到ClO 2溶液。上述过程中,生成ClO 2的反应属于歧化反应,每生成1mol ClO 2消耗NaClO 2的量为 mol;产生"气泡"的化学方程式为 。
(5)"84消毒液"的有效成分为NaClO,不可与酸性清洁剂混用的原因是 (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000kg该溶液需消耗氯气的质量为 kg(保留整数)。
下列说法中正确的是
| A.氯化钠水溶液在电流的作用下电离出Na+和Cl- |
| B.二氧化碳的水溶液能够导电,故二氧化碳属于电解质 |
| C.碳酸氢钠在水中电离的离子方程式为NaHCO3=Na++H++CO2- 3 |
| D.碳酸钠属于电解质 |
下列物质能导电的是 ;属于电解质的是 ;属于非电解质的是 (填编号)。
①HCl气体、② NH3、③熔融的NaOH 、④SO2、⑤Cu 、 ⑥氨水 ⑦KNO3溶液 、⑧液态醋酸 、⑨蔗糖、⑩硫酸钡固体
(1)现有下列物质 ①Fe、② HCl气体、③NaOH固体、④NH3气体、⑤ KCl溶液、⑥CH3COOH、⑦SO3、⑧乙醇、⑨BaSO4固体请用以上物质回答下列问题。(填序号)电解质: ;非电解质: ;上述状态能导电的是: 。
(2)按要求写出方程式。
①Mg(OH)2和盐酸: (写出离子方程式)
②足量澄清石灰水通入少量CO2: (写出离子方程式)
③Fe2(SO4)3: (写出电离方程式)
④H++OH—=H2O: (写出对应的化学方程式)
⑤CO32—+2H+=CO2↑+H2O: (写出对应的化学方程式)
下图为五个椭圆交叉构成的图案,椭圆内分别写了C2H5OH、CO2、Fe2O3、FeCl3和NaOH五种物质,图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号。请回答下列问题:

(1)两种物质都是电解质的是_______(填分类标准代号,下同),两种物质都是氧化物的是________。
(2)分类标准代号A表示______________(多项选择)
a.两物质都是非电解质 b.两物质都是有机物
C.两物质都是含碳化合物 d.两物质都是氧化物
(3)上述五种物质中的某相邻两种物质间能发生反应且有离子反应,写出该反应的离子方程式为: ____________________ _____________________。
(4)用洁净的烧杯取25 mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热呈红褐色,得到的分散系称为_____________。