甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的两个反应:
反应I: CO(g)+2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II:CO2(g)+3H2(g) CH3OH(g)+ H2O(g) ΔH2
CH3OH(g)+ H2O(g) ΔH2
① 上述反应符合“原子经济”原则的是 (填“I”或“II”)。
② 下表所列数据是反应I在不同温度下的化学平衡常数(K)。
| 温度 |
250℃ |
300℃ |
350℃ |
| K |
2.041 |
0.270 |
0.012 |
由表中数据判断反应I为______热反应(填“吸”或“放”)。
③ 某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 (从表中选择)。
(2) 已知在常温常压下:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1 kJ/mol
② 2CO(g)+ O2(g)= 2CO2(g) ΔH2 kJ/mol
③ H2O(g)= H2O(l) ΔH3 kJ/mol
则反应CH3OH(l)+ O2(g)= CO(g)+ 2H2O(l) ΔH= kJ/mol
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O2‾7)时,实验室利用下图装置模拟该法:

① N电极的电极反应式为 。
② 请完成电解池中Cr2O2‾7转化为Cr3+的离子反应方程式:
Cr2O7 2‾+ Fe2+ + [ ] ═= Cr3++ Fe3++ H2O
(4) 处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10‾5 mol•L﹣1时,Cr3+沉淀完全,此时溶液的pH= 。(已知, Ksp[Cr(OH)3]=6.4×10‾31,lg2=0.3)
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池。其构造如图所示:两个电极均由多孔性碳制成,通入的气体由孔隙中进入,并在电极表面放电。

(1)a是_____________极(填正或负),b是___________极(填正或负),电极反应式分别为:a__________________,b_______________。
(2)下图是一个化学过程的示意图。已知甲池的总反应式为:

2CH3OH+3O2+4KOH=2K2CO3+6H2O
①请回答:甲池是 装置,B(石墨)电极的名称是 。
②写出下列电极反应式:通入CH3OH的电极的电极反应式是 ,A(Fe)电极的电极反应式为 。
③乙池中反应的化学方程式为 。
④当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上转移电子 mol。
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
① 已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH1= +489.0 kJ/mol
C(石墨)+CO2(g)=2CO(g) ΔH2=+172.5 kJ/mol
则CO还原Fe2O3的热化学方程式为 ;
②氯化钯(PdCl2)溶液常被应用于检测空气中微量CO,PdCl2被还原成单质,反应的化学方程式为 ;
(2)将两个石墨电极插入KOH溶液中,向两极分别通入C3H8和O2构成丙烷燃料电池。
① 负极电极反应式是: ;
②某同学利用丙烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是 (填序号)

A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H++2e-=H2↑
(3)将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g)  CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
|
| H2O |
CO |
CO2 |
|||
| 1 |
650 |
2 |
4 |
1.6 |
5 |
| 2 |
900 |
1 |
2 |
0.4 |
3 |
| 3 |
900 |
1 |
2 |
0.4 |
1 |
①该反应的正反应为 (填“吸”或“放”)热反应;
②实验2中,平衡常数K= ;
③实验3跟实验2相比,改变的条件可能是 (答一种情况即可)
下图为相互串联的甲乙两个电解池,请回答:

(1)甲池若为用电解原理精炼铜的装置,A是 极,材料是 电极反应为 ,B是 极,材料是 ,电极反应为 ,[电解质溶液为 。(注:杂质发生的电极反应不必写)电解后,原溶液中溶质的物质的量浓度 。(填“变大”“变小”和“不变”)
(2)乙池中若滴入少量酚酞试液,开始一段时间后,Fe极附近呈 色。
(3)若甲槽阴极增重12.8 g,则乙槽阳极放出气体在标准状况下的体积为 。
(4)若乙槽剩余液体为400 mL,则电解后得到碱液的物质的量浓度为
氨气在生产、生活和科研中应用十分广泛
(1)传统工业上利用氨气合成尿素
①以CO2与NH3为原料合成尿素的主要反应如下:
2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.47 kJ·mol-1
NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+ 72.49 kJ·mol-1
反应2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) ΔH= kJ·mol-1。
②液氨可以发生电离:2NH3(l) NH2- + NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式 。
NH2- + NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式 。
(2)氨气易液化,便于储运,可利用NH3作储氢材料
已知:2NH3(g) N2(g) + 3H2(g) ΔH=+92.4 kJ·mol-1
N2(g) + 3H2(g) ΔH=+92.4 kJ·mol-1
① 氨气自发分解的反应条件是 (填“低温” 或 “高温”)。
②其他条件相同,该反应在不同催化剂作用下反应,相同时间后,氨气的转化率随反应温度的变化如右图所示。
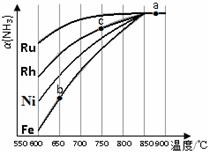
在600℃时催化效果最好的是 (填催化剂的化学式)。c点氨气的转化率高于b点,原因是 。
(3)垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,把垃圾渗滤液加入到如图所示的电解池(电极为惰性材料)进行电解除去NH3,净化污水。该净化过程分两步:第一步电解产生氧化剂,第二步氧化剂氧化氨氮物质生成N2。
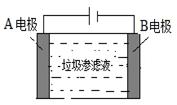
①写出电解时A极的电极反应式: 。
②写出第二步反应的化学方程式: 。
(一)已知水的电离平衡曲线如图所示,试回答下列问题:

(1)E对应的温度下,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为_______ _
(2)B对应温度下,将pH=11的苛性钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积与原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=___________________
(二)膜技术原理在化工生产中有着广泛的应用。有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下。
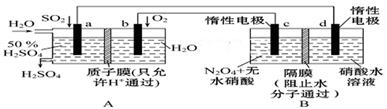
(1)A装置是________________,B装置是____________(填“原电池”或“电解池”)。
(2)N2O5在电解池的______________(填“c极”或“d极”)区生成,其电极反应式为__________________
(3)A装置中通入SO2一极的电极反应式为
(4)若A装置中通入SO2的速率为2.24 L·min-1(标准状况),为稳定持续生产,硫酸溶液的浓度应维持不变,则左侧水的流入速率应为_______________mL·min-1。
面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的主要方向。
(1) “生物质”是由植物或动物生命体衍生得到的物质的总和。生物质能主要是指用树木、庄稼、草类等植物直接或间接提供的能量.秸秆、杂草等废弃物经微生物发酵之后,便可以产生沼气,利用沼气是解决人类能源危机的重要途径之一。下面说法不正确的是( )
| A.利用生物质能就是间接利用太阳能,生物质能是可再生能源 |
| B.生物质能是解决农村能源的重要途径之一 |
| C.生物质能的缺点是严重污染环境 |
| D.若建立沼气发电站,则可以实现把生物质能转化为电能 |
(2)工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO和H2,已知CH4、H2和CO的燃烧热(△H)分别为 -890.3 KJ·mol-1、-285.8 KJ·mol-1、-283.0 KJ·mol-1,则该重整的热化学方式为 ;
(3)一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:
C(s) +CO2(g ) 2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:已知气体分压(P分 )=气体总压(P总 )×体积分数,则925℃时,用平衡分压代替平衡浓度表示的化学平衡常数= 。T℃时,若充入等体积的CO2和CO,平衡 (填“正向移动、逆向移动、不移动”)。
2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:已知气体分压(P分 )=气体总压(P总 )×体积分数,则925℃时,用平衡分压代替平衡浓度表示的化学平衡常数= 。T℃时,若充入等体积的CO2和CO,平衡 (填“正向移动、逆向移动、不移动”)。


(4)如下图是一个二甲醚(CH3OCH3)燃料电池工作时的示意图,
①若乙池为粗铜的电解精炼,电解质为硫酸铜,则N电极材料为 。
②若乙池中M、N为惰性电极,电解质为足量硝酸银溶液,写出乙池中电解的化学方程式 。乙池中某一电极析出金属银2.16g时,溶液的体积为200mL,则常温下乙池中溶液的pH为 。
③通入二甲醚的铂电极的电极反应式为 。若该电池的理论输出电压为1.0V,则该电池的能量密度= kW·h·kg-1(结果保留小数点后一位).(能量密度=电池输出电能/燃料质量,1kW·h=3.6×106J,法拉第常数F=9.65×l04C·mol-1 )。
(12分)某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu。


(1)将上述反应设计成原电池如图甲所示,请回答下列问题:
①图中X溶液的溶质是____(填化学式),Cu电极上发生的电极反应方程式为 。
②原电池工作时,盐桥中的_____________ (填“K+”或“Cl-”)不断进入X溶液中。
(2)将上述反应设计成电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量关系如图丙,请回答下列问题:
①M是直流电源的__________极;图丙中的②线是_________的物质的量的变化。
②当电子转移为2mol时,向乙烧杯中加入________ L5mol·L-1NaOH溶液,才能使溶液中所有的金属阳离子沉淀完全。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O Na2FeO4+3H2↑,则电解时阳极的电极反应方程式为__________________________________。
Na2FeO4+3H2↑,则电解时阳极的电极反应方程式为__________________________________。
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为___________________________________。
甲烷作为一种新能源在化工领域应用广泛,请回答下列问题:
(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:CH4(g)+CO2(g)===2CO(g)+2H2(g) ;ΔH=+260 kJ·mol-1
已知:2CO(g)+O2(g)===2CO2(g) ;ΔH=﹣566 kJ·mol-1
则CH4与O2反应生成CO和H2的热化学方程式为: _____________________.
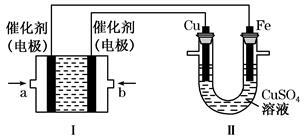
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
①a处应通入_____(填“CH4”或“O2”),b处电极上发生的电极反应式是:
②电镀结束后,装置Ⅰ中溶液的pH值_____(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度 .
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH―以外还含有_____(忽略水解).
④在此过程中若完全反应,装置Ⅱ中阴极质量变化为12.8 g,则装置Ⅰ中理论上消耗甲烷_______L(标准状况下).
铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各 种性能的不锈钢,CrO3 大量地用于电镀工业中。
(1)在下图装置中,观察到图 1 装置铜电极上产生大量的无色气泡,而图 2 装置中铜电 极上无气体产生,铬电极上产生大量有色气体。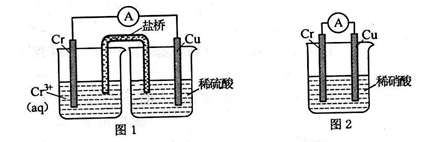
图 2 装置中铬电极的电极反应式______________________
(2)最近赣州酒驾检查特别严,利用 CrO3具有强氧化性,有机物(如酒精)遇到 CrO3时,猛烈反应,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3],另该过程中乙醇被氧化成乙酸, 从而增强导电性,根据电流大小可自动换算出酒精含量。写出该反应的化学方程式为_________________________
(3)虽然铬加到铁中可将铁做成不锈钢可减少金属腐蚀,但 生产成本高,生活中很多情况下还是直接使用钢铁,但易腐蚀, 利用右图装置,可以模拟铁的电化学防护。若 X 为碳棒,为 减缓铁的腐蚀,开关 K 应置于________处。若 X 为锌,开关K 置于________处。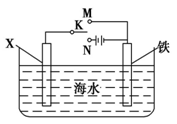
(4)CrO3 和 K2Cr2O7 均易溶于水,这是工业上造成铬污染的 主要原因。净化处理方法之一是将含+6 价 Cr 的废水放入电解槽内,用铁作阳极,加入 适量的 NaCl 进行电解:阳极区生成的 Fe2+和 Cr2O72-发生反应,生成的 Fe3+和 Cr3+在阴极 区与OH-结合生成 Fe(OH)3和 Cr(OH)3沉淀除去【已知某条件下的KspFe (OH)3 = 3.0×10-31, KspCr(OH)3 = 6.0×10-38】。已知电解后的溶液中 c(Fe3+)为 2.0×10-6 mol·L1,则溶液中c(Cr3+)为______________mol·L-1。
工业废水随意排放会造成严重污染,根据成分不同可采用不同的处理方法。
(1)电池生产工业废水中常含有Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去。已知室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。
①请用离子方程式说明上述除杂的原理______________________。
②FeS高温煅烧产生的SO2气体通入下列溶液中,能够产生沉淀的是_________(填序号)
A.Ba(NO3)2 B.BaCl2
C.Ba(OH)2 D.溶有NH3的BaCl2溶液
③已知元素在高价态时常表现氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,则生成CuCl的离子方程式是___________。
(2)电解法处理酸性含铬废水(主要含有Cr2O72-)时,在废水中加入适量NaCl,以铁板作阴、阳极,处理过程中存在如下反应Cr2O72+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+ 以Cr(OH)3形式除去,下列说法不正确的是______(填序号)
A.阳极反应为Fe-2e-═Fe2+
B.电解过程中溶液pH减小
C.过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有2mol Cr2O72-被还原
(3)废氨水可以转化成氨,氨再设计成碱性燃料电池。右图是该燃料电池示意图,产生的X气体可直接排放到大气中,a电极作_________极(填“正”“负”“阴”或“阳”),其电极反应式为___________。

I.炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红色锈斑。请回答:
写出铁锅腐蚀时正极的电极反应式: 。
II.氯碱工业中电解饱和食盐水的原理示意图如下图所示:

(1)溶液A的溶质是 ;
(2)电解饱和食盐水的离子方程式是 ;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用平衡移动移动原理解释盐酸的作用: 。
Ⅲ.(1)按右图电解氯化钠的稀溶液可制得漂白液,写出该电解池中发生反应的总反应方程式: ;

(2)将充分电解后所得溶液逐滴加入到酚酞试液中,观察到的(3)现象是 。
如图所示的电解装置中,乙池盛有200mL饱和CuSO4溶液,丙池盛有200mL饱和NaCl溶液.通电一段时间后,C极增重0.64g,则:

(1)P是电源的_________极。甲池中,A极的质量_________g。电解一段时间,甲池溶液的pH为_________。(2)D极的电极反应式为 ,丙池电解反应的总离子方程式为 。
相同状况下,D电极与E电极产生的气体体积比为_______________。
(3)若乙池溶液通电一段时间后,向所得的溶液中加入0.1mol的Cu(OH)2后恰好恢复到电解前的浓度。则电解过程中转移电子的数目为__________________。(用NA表示)
NH4NO3主要用作肥料、军用炸药、冷冻剂、制造笑气等。
(1)铵态氮肥NH4NO3________(填“能”或“不能”)与草木灰混合施用,用盐类水解的知识简述原因__________。
(2)NH4NO3受热分解温度不同,分解产物也不同。在185~200°C时,NH4NO3分解生成笑气(N2O)和水,分解生成的氧化产物与还原产物的质量比为__________。超过400°C,NH4NO3剧烈分解生成N2、NO2和H2O,并发生爆炸,若32g NH4NO3爆炸放出12.3 kJ的热量,则NH4NO3分解爆炸的热化学方程式为______________。
(3)电解NO制备 NH4NO3,其工作原理如图所示,阴极反应式为___________________;电解反应的总方程式为___________________;为使电解产物全部转化为NH4NO3,需补充物质A,A是__________。
电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与右图中电解池相连,其中,a为电解液,X和Y是两块电极板,则:

(1)若X、Y依次为铜和铁,a仍为CuSO4溶液,且反应过程中未生成Fe3+,则Y极的电极反应式为
(2)若用此装置电解精炼铜, 做阳极,电解液CuSO4的浓度 (填“增大”、“减小”或“不变”)。
(3)PbO2可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生反应的电极反应式为 ;若电解液中不加入Cu(NO3)2,阴极发生的电极反应式为 。
(4)如图:A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。

比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为 (填字母序号)。