用下图Ⅰ所示装置通电10分钟后,去掉直流电源,连接成图Ⅱ所示装置,可观察到U形管左端铁电极表面析出白色胶状物质,U形管右端液面上升。下列说法正确的是 
| A.同温、同压下,装置Ⅰ中石墨电极上方得到的气体比铁电极上方得到的气体多 |
| B.用装置Ⅱ进行实验时铁电极的电极反应为Fe-2e-+2OH-===Fe(OH)2 |
| C.用装置Ⅱ进行实验时石墨电极的电极反应为2H++2e-===H2↑ |
| D.装置Ⅰ通电10分钟后铁电极周围溶液pH降低 |
下列叙述正确的是
| A.在电解池的阴极和原电池的负极上都发生氧化反应 |
| B.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
| C.用惰性电极电解KOH溶液,阴、阳两极产物的物质的量之比为1:2 |
| D.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH |
用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是
| A.稀NaOH溶液 | B.HCl溶液 |
| C.酸性MgCl2溶液 | D.酸性AgNO3溶液 |
用惰性电极电解100mL4mol ·L-1的CuSO4溶液,一定时间后在阳极收集到1.12 L气体,向电解后的溶液中加入足量的铁粉,充分作用后溶液中的Fe2+浓度为(设溶液的体积不变,反应前后均为标准状况)( )
| A.2.7 mol· L-1 | B.3 mol· L-1 | C.4 mol· L-1 | D.1 mol· L |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O  3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH
下列叙述不正确的是( )
| A.放电时负极反应为:Zn-2e—+2OH—=Zn(OH)2 |
| B.充电时阳极反应为:Fe(OH)3 -3e—+ 5OH—=FeO42-+ 4H2O |
| C.放电时每转移3mol电子,正极有1molK2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
下列有关电化学装置完全正确的是( )
| A |
B |
C |
D |
 |
 |
 |
 |
| 铜的冶炼 |
铁上镀银 |
防止Fe被腐蚀 |
构成铜锌原电池 |
A.A B.B C.C D.D
利用电解法可将含有、
、
、
等杂质的粗铜提纯,下列叙述正确的是()
| A. | 电解时以纯铜作阳极 |
| B. | 电解时阴极发生氧化反应 |
| C. |
粗铜连接电源负极,电极反应是
|
| D. |
电解结束,电解槽底部会形成含少量
|
下列关于电解的说法正确的是
| A.电解是把化学能转变成电能 |
| B.电解池的阳极发生氧化反应,阴极发生还原反应 |
| C.电解时溶液中靠电子导电 |
| D.工业上通过电解熔融MgO制备Mg单质 |
用铂电极电解100mL HNO3 与 AgNO3的混合液,通电一段时间后,两极均收集到
2.24 L气体(标准状况),则原混合液中Ag+的物质的量浓度为
A.1mol·L-1 B.2 mol·L-1 C.2.5 mol·L-1 D.3 mol·L-1
CuCl2溶液中的铜主要以Cu (H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu (H2O)42+(蓝色)+4Cl- CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
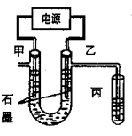
(1)甲电极的电极反应式为_________________。
(2)丙中溶液变蓝是乙电极产物与KI反应导致的,该反应的化学方程式为_________________。
(3)随电解的不断进行,U型管中溶液的颜色变化为__________;
A.由黄色变为浅蓝色 B.由蓝色变为浅黄色
溶液颜色变化的原因是_________________。
(4)当电解到一定程度,甲电极附近出现蓝色Cu(OH)2絮状物。经测,甲电极附近溶液的pH=a,此时甲电极附近c(Cu2+)="________" mol·L-1。(已知:Cu(OH)2的Ksp=2.2*10-20)。
如图所示,下列有关装置的分析中正确的是( )

| 选项 |
开关控制 |
X溶液 |
装置叙述 |
| A |
接通K2, 断开K1 |
HCl |
Fe极为正极, 该极质量减小 |
| B |
接通K2, 断开K1 |
CuCl2 |
Fe极为负极, 该极质量增加 |
| C |
接通K1, 断开K2 |
CuSO4 |
Fe极为阴极, 该极有Cu析出 |
| D |
接通K1, 断开K2 |
NaCl |
Fe极为阳极, 该极逐渐溶解 |
金属镍有广泛的用途。粗镍中含有少量杂质Fe、Zn、Cu、Pt,可用电解法制备高纯度的镍(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是( )。
| A.阳极发生还原反应,其电极反应式:Ni2++2e-=Ni |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C.电解后,溶液中存在的阳离子只有Fe2+和Zn2+ |
| D.电解后,电解槽底部的阳极泥中只有Cu和Pt |
下列过程需要通电才能进行的是( )
①电离 ②电镀 ③电解 ④电化学腐蚀 ⑤电泳
| A.①② | B.②③⑤ | C.②③ | D.全部 |
某学生在课堂上学到了卤素、电解等化学知识后,想为自己家中制作一只简易的消毒液发生器。他用石墨(废干电池中的炭棒)作电极,饱和氯化钠溶液作为电解液,制成了如图所示的装置。通电数分钟后,果真制得了消毒液。他的实验居然一举获得成功!该装置中电源电极的名称和消毒液的主要成分正确的是....…………..( )
| A.a为正极,b为负极;NaClO和NaCl |
| B.a为负极,b为正极;NaClO和NaCl |
| C.a为阳极,b为阴极;HClO和NaCl |
| D.a为阴极,b为阳极;HClO和NaCl |