原电池产生电流的本质原因是
| A.原电池中溶液能电离出自由移动的离子 |
| B.有导线将两个活动性不同的电极连接 |
| C.正极发生了氧化反应,而负极发生了还原反应 |
| D.电极上进行的氧化还原反应中会有电子的转移 |
有关原电池的工作原理中,下列说法中不正确的是
| A.电池负极发生氧化反应 | B.电池正极发生还原反应 |
| C.电子流向是从负极流向正极(外电路) | D.电流方向是从负极流向正极(外电路) |
关于铅蓄电池的说法正确的是( )
| A.在放电时,正极发生的反应是Pb(s)+SO42-(aq)=PbSO4(s)+2e- |
| B.在放电时,该电池的负极材料是铅板 |
| C.在充电时,电池中硫酸的浓度不断变小 |
| D.在充电时,阳极发生的反应是 PbSO4(s)+2e-=Pb(s)+SO42-(aq) |
下列关于右图所示装置的叙述,不正确的是
| A.铁是负极,铁失去电子形成Fe2+进入溶液 |
| B.铁片质量逐渐减少,碳棒上有气泡产生 |
| C.电流由铁片经导线沿外电路流向碳棒 |
D.该装置总的化学反应为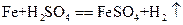 |
根据下图,下列判断中正确的是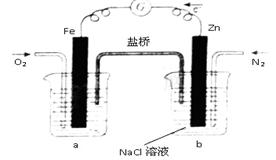
| A.烧杯b中发生还原反应 |
| B.烧杯a中的溶液pH升高 |
| C.烧杯a中发生的反应为2H+ +2e-="==" H2 |
| D.烧杯b中发生的反应为2Cl--2e-="==" Cl2 |
有A、B、C、D四种金属,将A和B用导线连接起来,浸入电解质溶液中,B上有电子流入,将A、D分别投入等浓度的盐酸中,D比A反应剧烈,将铜浸入B的盐溶液中,无明显变化,如果把铜浸入C的盐溶液中,有金属C析出,据此判断A、B、C、D四种金属的活泼性由强到弱的顺序是
A.D>C>A>B B.D>A>B>C C.D>B>A>C D.B>A>D>C
下图所示装置的叙述,正确的是
| A.铜是阳极,铜片上有气泡产生 |
| B.盐桥中的阳离子会移向CuSO4溶液 |
| C.正极附近的SO42-离子浓度逐渐增大 |
| D.锌离子在锌片表面被还原 |
铜锌原电池(如图)工作时,下列叙述正确的是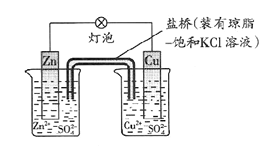
| A.一段时间后铜片增重,盐桥中K+移向CuSO4溶液 |
| B.正极反应为:Zn-2e-=Zn2+ |
| C.电子从铜片经导线流向锌片 |
| D.电池工作时Zn2+和Cu2+ 的浓度保持不变 |
下列关于电化学的理解正确的是
| A.原电池一定是负极材料失电子,发生氧化反应 |
| B.电解池的电极材料一定不参与电极反应 |
| C.原电池的负极和电解池的阳极一定发生氧化反应 |
| D.原电池中的阳离子移向负极,电解池中的阳离子则移向阴极 |
有如图所示的装置,当电流表中产生持续电流时,下列说法正确的是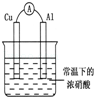
| A.Cu是原电池的负极 |
| B.Al是原电池的负极 |
| C.电子由Al沿导线流向铜 |
| D.铝片上的电极反应式为:Al﹣3e﹣═AL3+ |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。RFC工作原理如图所示,下列有关说法正确的是
A.当有0.1mol电子转移时,a电极产生2.24LH2
B.b极上发生的电极反应是:4H2O+4e- =2H2↑+4OH-
C.c极上进行还原反应,B池中的H+可以通过隔膜进入A 池
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
下列关于铁电极的说法中,正确的是
| A.钢铁的吸氧腐蚀中铁是正极 | B.在铁片上镀铜时铁片作阳极 |
| C.电解饱和食盐水时可用铁作阴极 | D.镀锌铁板发生电化学腐蚀时铁是负极 |
右图是研究铁钉腐蚀的装置图,下列说法不正确的是
| A.铁钉在两处的腐蚀速率:a < b |
| B.a、b两处铁钉中碳均正极 |
| C.a、b两处铁钉中的铁均失电子被氧化 |
| D.a、b两处的正极反应式均为O2+4e-+4H+ ===2H2O |