河南省焦作市高一下学期期末测试化学(必修2)试题
19世纪中叶,俄国化学家门捷列夫对化学学科的巨大贡献是
| A.提出了原子学说 |
| B.提出了元素周期律 |
| C.提出了分子学说 |
| D.制定了科学的元素周期表 |
通常用于衡量一个国家石油化工发展水平的标志是
| A.石油的产量 | B.乙烯的产量 |
| C.天然气的产量 | D.汽油的产量 |
正确掌握化学用语是学好化学的基础。下列化学用语中正确的是
| A.乙烯的结构简式为:CH2CH2 |
| B.乙醇的结构简式为:C2H6O |
C.Ca2+的结构示意图为: |
D.羟基的电子式: |
下列说法不正确的是
| A.16O、18O互为同位素 |
| B.金刚石和石墨互为同素异形体 |
| C.分子式符合通式CnH2n+2且n值不同的两种烃互为同系物 |
D.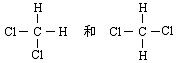 互为同分异构体 互为同分异构体 |
美国科学家将铅和氪两种元素的原子核对撞,获得了一种质子数为118,质量数为293的新元素,则该元素原子核内的中子数和核外电子数之差为
| A.57 | B.47 | C.61 | D.175 |
下列性质的递变规律不正确的是
| A.NaOH、KOH、CsOH碱性依次增强 |
| B.HCl、H2S、PH3稳定性依次减弱 |
| C.Al、Mg、Na的原子半径依次减小 |
| D.HC1O4、H2SO4、H3PO4的酸性依次减弱 |
某有机物的结构简式为CH2=CH—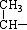 CH2OH。下列关于该有机物的叙述不正确的是
CH2OH。下列关于该有机物的叙述不正确的是
| A.能与金属钠发生反应并放出氢气 |
| B.此有机物中有三种官能团:碳碳双键、羟基、甲基 |
| C.能在催化剂作用下与H2发生加成反应 |
| D.在浓H2SO4催化下能与乙酸发生酯化反应 |
自然界为人类提供了多种多样的营养物质,下列有关营养物质的说法正确的是
| A.蔗糖、淀粉、油脂等都可以发生水解反应 |
| B.摄入人体的纤维素在酶的作用下能水解为葡萄糖 |
| C.糖类、蛋白质、油脂都属于天然高分子化合物 |
| D.所有糖类物质都有甜味,但不一定都溶于水 |
可逆反应2SO2+O2 2SO3在密闭容器中达到了平衡,下列说法正确的是
2SO3在密闭容器中达到了平衡,下列说法正确的是
| A.SO2和O2不再化合,反应停止了 |
| B.容器内压强保持不变 |
| C.SO2、O2和SO3的浓度相等 |
| D.SO2、O2和SO3的物质的量之比为2:1:2 |
下列各组液体混合物,能用分液漏斗分离的是
| A.乙酸乙酯和乙醇 | B.苯和溴苯 |
| C.苯和水 | D.乙醇和水 |
下列关于右图所示装置的叙述,不正确的是
| A.铁是负极,铁失去电子形成Fe2+进入溶液 |
| B.铁片质量逐渐减少,碳棒上有气泡产生 |
| C.电流由铁片经导线沿外电路流向碳棒 |
D.该装置总的化学反应为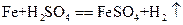 |
下列说法正确的是
| A.反应是放热还是吸热是由反应物和生成物所具有的能量的相对大小决定的 |
| B.放热反应在常温下一定容易进行 |
| C.需加热才能发生的反应一定是吸热反应 |
| D.质量数相同的原子,其化学性质也一定相同 |
海带中含有碘元素,某校研究性学习小组设计了如下实验步骤来提取碘:①通足量氯气 ②将海带烧成灰,向灰中加水搅拌 ③加CC14振荡④过滤 ⑤用分液漏斗分液。合理的操作顺序为
| A.①→③→⑤→②→④ |
| B.②→①→③→④→⑤ |
| C.③→①→②→⑤→④ |
| D.②→④→①→③→⑤ |
下列叙述正确的是
| A.卤素单质的颜色随核电荷数的增大而逐渐加深 |
| B.卤素形成的氢化物稳定性随核电荷数增大而增大 |
| C.碱金属都比水轻 |
| D.碱金属都保存在煤油中 |
常温常压下,取下列四种有机物各1mol,分别在足量的氧气中燃烧,消耗氧气最多的是
| A.C2H5OH | B.CH4 |
| C.C3H8O2 | D.C2H4O |
标准状况下,0.56 L CH4和C2H4的混合气体通入足量溴水中,溴水增重0.28g(假设C2H4完全被吸收),则乙烯占混合气体体积的
| A.20% | B.40% |
| C.60% | D.80% |
冶炼金属常用以下几种方法:
①热分解法 ②以活泼金属Na、Mg等还原 ③以C、CO或H2做还原剂 ④电解法 ⑤利用铝热反应原理还原。
下列金属各采用哪种方法还原最佳。(用序号填写下列空白。)
(1)Fe、Zn、Cu等中等活泼金属 。
(2)Na、Mg、Al等活泼或较活泼金属 。
(3)Hg、Ag等不活泼金属 。
(4)V、Cr、Mn、W等高熔点金属 。
请将所选下列物质的转化或分离方法的序号填在横线上(每一项只填写一种方法)。
①溶解 ②裂解 ③干馏 ④蒸馏 ⑤分馏
⑥裂化 ⑦电解 ⑧过滤 ⑨萃取
(1)把煤转化为焦炉气、煤焦油和焦炭等 。
(2)从原油中分离出汽油、煤油、柴油等 。
(3)将重油转化为汽油 。
(4)将海水淡化 。
(5)从海水得到的无水MgC12中提取金属镁 。
短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素。试回答下列问题:
(1)A的元素符号 ;D元素在第 周期 族
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是 。(写具体的离子符号)
(3)A、B两元素形成的含有非极性键的化合物的化学式为 ,它属于 (“离子”或“共价”)化合物。
(7分)某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
(1)该反应的化学方程式为: ;
(2)反应开始至2min末,X的反应速率为 (mol·L-1·min-1);
(3)3min后图中曲线所表示的含义是: 。
21世纪最富有挑战性的课题之一是使汽油氧化直接产生电流,新研制的某汽油燃料电池的一个电极通入空气,另一个电极通入汽油蒸气,填写下列空格。
(1)提练汽油的原料是石油,石油是一种__________(选填“可再生”或“不可再生” )能源。
(2)汽油_____________(选填“有”或“没有” )固定的熔沸点。
(3)汽油燃料电池的能量转换形式是将________能直接转化为______能。
(4)通入空气的那个电极是燃料电池_________极(选填“正”或“负” )该电极上若有32 g O2参加反应,则反应过程中转移了_________mol e-。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号