关于原电池和电解池的叙述正确的是( )
| A.原电池中失去电子的电极为阴极 |
| B.原电池的负极、电解池的阳极都发生氧化反应 |
| C.原电池的两极一定是由活动性不同的两种金属组成 |
| D.电解时电解池的阴极一定是阴离子放电 |
若将反应:Zn+H2SO4= ZnSO4+H2↑设计成原电池(如右图),则下列说法不正确的是
| A.该装置实现了化学能转化为电能 |
| B.b 极表面发生了还原反应 |
| C.c 溶液可以是ZnSO4溶液 |
| D.盐桥中的Cl-移向右边烧杯 |
已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质)。现用A与石墨作电极,B的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图:(注意:其中有些反应的条件及部分生成物被略去)

请填写下列空白:
(1)比较①~⑦七个反应,请归纳它们的共同特点是
(2)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为
(3)写出物质B的电子式
(4)从D溶液制备D的无水晶体的“操作a”为 。
(5)反应②的化学方程式为
(6)反应⑤的化学方程为
(7)原电池反应①中正极的电极反应为
如下图是一个化学过程的示意图。已知甲池的总反应式为:2CH3OH+3O2+4KOH===2K2CO3+6H2O。
(1)甲池是________装置。
(2)乙池中A(石墨)电极的名称是________。
(3)写出通入CH3OH的电极的电极反应式:_________________________。
(4)乙池中反应的化学方程式为______________________________________。
(5)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2________ mL(标准状况);此时丙池某电极上析出0.60 g某金属,则丙池中的某盐溶液可能是________(填序号)。
| A.MgSO4 | B.CuSO4 | C.NACl | D.AgNO3 |
普通纸张的主要成分是纤维素。在早期的纸张生产中,常采用纸张表面涂敷明矾的工艺,以填补其表面的微孔,防止墨迹扩散。请回答下列问题:
(1)人们发现纸张会发生酸性腐蚀而变脆、破损,严重威胁纸质文物的保存。经分析检验,发现酸性腐蚀主要与造纸中涂敷明矾的工艺有关,其中的化学原理是_____________________________________为了防止纸张的酸性腐蚀,可在纸浆中加入碳酸钙等添加剂,该工艺原理的离子方程式为__________。
(2)为了保护这些纸质文物,有人建议采取如下措施:喷洒Zn(C2H5)2。Zn(C2H5)2可以与水反应生成氧化锌和乙烷,生成的氧化锌可以防止酸性腐蚀。用该方法生成氧化锌的化学方程式为__________________。
(3)现代造纸工艺常用钛白粉(TiO2)替代明矾。钛白粉的一种工业制法是以钛铁矿(主要成分为FeTiO3)为原料按下列过程进行的,请完成下列化学方程式:
① FeTiO3+ C+ Cl2 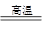 TiCl4+ FeCl3+ CO
TiCl4+ FeCl3+ CO
② TiCl4+O2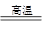 TiO2+2Cl2
TiO2+2Cl2
(4)某新型“纸电池”以碳纳米管和金属锂为两极,造纸用的纤维素在一种离子液体M中溶解作隔离膜,电池工作时的总反应式为xLi+C(碳纳米管) LixC,下列有关说法正确的是
LixC,下列有关说法正确的是
| A.放电时Li+由正极向负极移动 |
| B.充电池的阳极反应式为LixC-xe-= xLi++ C |
| C.M可能为羧酸、醇等含活泼氢的有机物 |
| D.锂离子电池的比能量(单位质量释放的能量)低 |
锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
| A.电池工作时,锌失去电子,电解液内部OH-向负极移动 |
| B.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e-=Mn2O3(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
锂碘电池的正极材料是聚2-乙烯吡啶(简写为P2VP)和I2的复合物,正极的电极反应式为P2VP·nI2+2Li++2e-=P2VP·(n-1)I2+2LiI,电解质是固态薄膜状碘化锂。下列说法正确的是
| A.P2VP和I2的复合物是绝缘体,不能导电 |
| B.电池工作时,碘离子移向P2VP和I2的复合物 |
| C.电池的总反应为2Li+P2VP·nI2=P2VP·(n-1)I2+2LiI |
| D.若该电池所产生的电压较高,则该电池使用寿命比较长 |
把a、b、c、d四块金属片浸泡在稀硫酸中,用导线两两相连可以组成各种原电池。若a、b相连时,a为负极;c、d相连时, d上有气泡逸出;a、c相连时,a极减轻;b、d相连时,b为正极。则这四种金属的活泼性由强到弱的顺序为( )
| A.a>b>c>d | B.a>c>b>d | C.a>c>d>b | D.b>d>a>c |
将洁净的金属片A、B 、C、D 分别放置在浸有盐溶液的滤纸上面并压紧(如图所示)。在每次实验时,记录电压指针的移动方向和电压表的读数如右表所示:


已知构成原电池两电极的金属活动性相差越大,电压表读数越大。则A、B、C、D四种金属中活泼性最强的是( )
A.A B. B C.C D.D
有a、b、c、d四种金属,将a与b用导线连接起来,浸入电解质溶液中,b不易腐蚀;将a、d分别投入等浓度的盐酸中,d比a反应剧烈;将铜浸入b盐溶液中,无明显变化;将铜浸入c的盐溶液中,有金属c析出。据此可推知它们的活动性顺序由强到弱为
| A.dcab | B.dbac | C.dabc | D.badc |
微电解法是利用原电池原理处理、净化高浓度有机废水的一种理想方法。在酸性、充入氧
气条件下的铁碳微电解法处理有机废水的过程中,有如下一些反应:
① O2+ 4H++4e-= 2H2O
② O2+ 2H2O+ 4e-= 4OH-
③ 4Fe2++O2+4H+= 2H2O+ 4Fe3+
......
下列有关这种铁碳微电解法处理有机废水说法不合理的是
| A.在处理废水的过程中,pH升高 |
| B.铁做负极,电极反应式是 Fe-2e-= Fe2+ |
| C.处理、净化过程中发生的反应都是氧化还原反应 |
| D.Fe(OH)3胶体,可净化除去废水中的悬浮物 |
X、Y、Z、M代表四种金属元素,金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为
| A.X>Z>Y>M | B.X>Y>Z>M | C.M>Z>X>Y | D.X>Z>M>Y |