银锌蓄电池是一种高能电池,它的两极材料分别为锌和氧化银,电解质溶液为KOH溶液,放电时它的正、负两极的电极反应式分别为:Zn+2OH--2e=Zn(OH)2,Ag2O+H2O+2e-=2Ag+2OH-,下列判断正确的是( )
| A.锌为负极,氧化银为正极; |
| B.锌为正极,氧化银为负极; |
| C.原电池工作时,负极区溶液pH增大; |
| D.原电池反应的化学方程式为:Zn+Ag2O+H2O=Zn(OH)2+2Ag |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
Zn(s)+2MnO2(s)+H2O(l)====Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是( )
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为2MnO2(s)+H2O(l)+2e-="===" Mn2O3(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g |
图4-17为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )
图4-17
| A.a电极是负极 |
| B.b电极的电极反应为:4OH--4e-====2H2O+O2↑ |
| C.氢氧燃料电池是一种具有应用前景的绿色电源 |
| D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
下列叙述正确的是( )
| A.铜锌原电池工作一段时间后,铜的质量增加 |
| B.钢铁的吸氧腐蚀负极反应为:Fe-2e====Fe2+ |
| C.电解AlCl3溶液可得到Al |
| D.电镀时应把镀件置于电解池的阳极 |
将甲、乙两铂片插入200 g 10% CuSO4溶液中进行电解,当阳极析出0.16 g气体时,求:
(1)阴极析出多少克铜?剩余CuSO4溶液中溶质的质量分数是多少?
(2)需要多少电荷量?
如图4-6所示,甲是刚浸过Na2SO4溶液的滤纸,A、B两铜片通过导线连接电源两极,在铜片间的滤纸上滴一滴KMnO4溶液,通电一段时间后,发现A、B间紫红色圆点向A移动了一段距离,则与A相连的是电源的 极,可发现滤纸的 极边沿附近有 色出现。
在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,最好选用下列物质中的( )
| A.NaOH | B.HCl |
| C.NaCl | D.CuSO4 |
关于如图4-10所示装置的叙述,正确的是( )

图4-10
| A.铜是阳极,铜片上有气泡产生 | B.铜片质量逐渐减少 |
| C.电流从锌片经导线流向铜片 | D.氢离子在铜片表面被还原 |
将纯锌片和纯铜片按图所示方式插入相同浓度的稀硫酸中一段时间,以下有关叙述正确的是( )
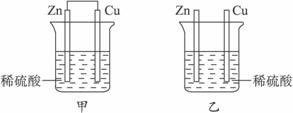
| A.甲装置中电能转化为化学能 | B.乙装置中电能转化为化学能 |
| C.甲装置中铜片表面有气泡产生 | D.乙装置中铜片表面有气泡生成 |
一个原电池总反应为:Zn+Cu2+ Zn2++Cu,该原电池材料及电解质可能是( )
Zn2++Cu,该原电池材料及电解质可能是( )
| |
正极 |
负极 |
电解质溶液 |
| A |
Zn |
Cu |
CuCl2 |
| B |
Cu |
Zn |
H2SO4 |
| C |
Cu |
Zn |
CuSO4 |
| D |
Fe |
Zn |
CuSO4 |
碱性电池具有容量大、放电电流大的特点,因此得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。下列说法错误的是( )
| A.电池工作时,锌失去电子 |
| B.电池负极的电极反应式为Zn-2e-+2OH-=Zn(OH)2 |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2 mol 电子,锌的质量理论上减小6.5g |
银锌蓄电池是一种高能电池,它的两极材料分别为锌和氧化银,电解质溶液为KOH溶液,放电时它的正、负两极的电极反应式如下:
Zn+2OH--2e=Zn(OH)2
Ag2O+H2O+2e=2Ag+2OH-
下列判断正确的是( )
| A.锌为负极,氧化银为正极 |
| B.锌为正极,氧化银为负极 |
| C.原电池工作时,负极区溶液pH增大 |
| D.原电池反应的化学方程式为:Zn+Ag2O+H2O=Zn(OH)2+2Ag |
锌锰干电池在放电时总反应方程式可以表示为:Zn(s)+2MnO2+2NH4+ Zn2++Mn2O3(s)+ 2NH3↑+H2O,在此电池放电时正极(碳棒)上发生反应的物质是( )
Zn2++Mn2O3(s)+ 2NH3↑+H2O,在此电池放电时正极(碳棒)上发生反应的物质是( )
| A.Zn | B.碳 | C.MnO2和NH4+ | D.Zn2+和NH3 |